Общая характеристика
Синдром Элерса–Данло (СЭД) – это гетерогенная группа наследственных нарушений соединительной ткани, характеризующаяся такими признаками дисплазии соединительной ткани, как гипермобильность суставов, гиперрастяжимость кожи, хрупкость сосудов, стрии, атрофические рубцы, грыжи, скелетно-мышечные нарушения.
Синонимы: Ehlers-Danlos Syndrome, гиперэластичность кожи, cutis hyperelastica, несовершенный десмогенез, синдром Черногубова-Элерса-Данлоса.
Синдром Элерса-Данло является самой частой дисплазией соединительной ткани. Частота встречаемости СЭД составляет по разным оценкам от 1:5000 до 1:250 000 в зависимости от формы и степени тяжести заболевания Чаще фиксируют легкие формы заболевания; стертые формы в детском возрасте диагностируются не всегда, обычно только при появлении специфических осложнений.
Патогенез СЭД обусловлен генетически-детерминированным нарушением синтеза или процессинга коллагена и других компонентов экстрацеллюлярного матрикса. Это приводит к нарушению целостности соединительной ткани, что делает её гиперрастяжимой, непрочной и хрупкой. Заболевание может быть вызвано патогенными вариантами в одном из генов: ADAMTS2, AEBP1, B3GALT6, B4GALT7, C1R, C1S, CHST14, COL1A1, COL1A2, COL3A1, COL5A1, COL5A2, COL12A1, DSE, FKBP14, FLNA, PLOD1, PRDM5, SLC39A13, THBS2, TNXB, ZNF469.
В 2017 г. была введена новая международная классификация СЭД, согласно которой выделено 13 типов синдрома, 12 из которых имеют четкие генетические корреляции [1], при этом проявления различных типов СЭД могут быть крайне гетерогенны и существенно отличаться от классических.
Выделены следующие типы синдрома Элерса-Данло:
-
Классический тип
-
Классикоподобный тип
-
Гипермобильный тип
-
Сосудистый (артериальный, экхимозный) тип
-
Кифосколиотический тип
-
Артрохалазисный тип
-
Сердечно-клапанный тип
-
Кожный (дерматоспараксисный) тип
-
Мышечно-контрактурный тип
-
Спондило-диспластический (прогероидный) тип
-
Периодонтический тип
-
Миопатический тип (миопатия Бетлема-2)
- Синдром хрупкости роговицы

Рис. 1. Джеймс Моррис (предположительно страдал синдромом Элерса-Данло). Фото опубликовано в журнале «Scientific America» в 1898 году.
Классический тип
Классический тип синдрома Элерса–Данло обусловлен патогенными вариантами в генах COL5A1 и COL5A2, которые кодируют α1 и α2-цепи коллагена типа V соответственно (более 90% случаев классического СЭД). В редких случаях данный тип СЭД может быть обусловлен патогенными варианты генов COL1A1 или COL1A2, кодирующих коллаген I типа. Наследуется аутосомно-доминантно, имеет популяционную распространенность 1:20 000. К большим клиническим критериям диагностики классического типа СЭД относят:
-
гиперрастяжимость кожи с наличием атрофических рубцов;
-
генерализованная гипермобильность суставов.
К малым клиническим критериям классического типа СЭД относят:
-
легкое образование синяков;
-
мягкая рыхлая кожа;
-
хрупкость кожи;
-
моллюскоидные псевдоопухоли (образования в области рубцов, расположенные над точками давления (например, в области локтя, пальцев);
-
подкожные сферические образования (небольшие сферические твердые образования, часто подвижные и пальпируемые, часто локализованы на предплечьях и голенях);
-
грыжи (или их наличие в анамнезе);
-
эпикантус («монгольская складка»);
-
осложнения гипермобильности суставов (растяжения связок, вывихи/подвывихи, плоскостопие);
-
семейный анамнез родственника первой степени родства, соответствующий клиническим критериям
Минимальные критерии, необходимые для постановки диагноза классического СЭД:
Большой критерий 1 (гиперрастяжимость кожи с наличием атрофических рубцов) +
большой критерий 2 (генерализованная гипермобильность суставов) и/или как минимум три малых критерия.
Подтверждающее молекулярно-генетическое тестирование обязательно для постановки окончательного диагноза классического СЭД.
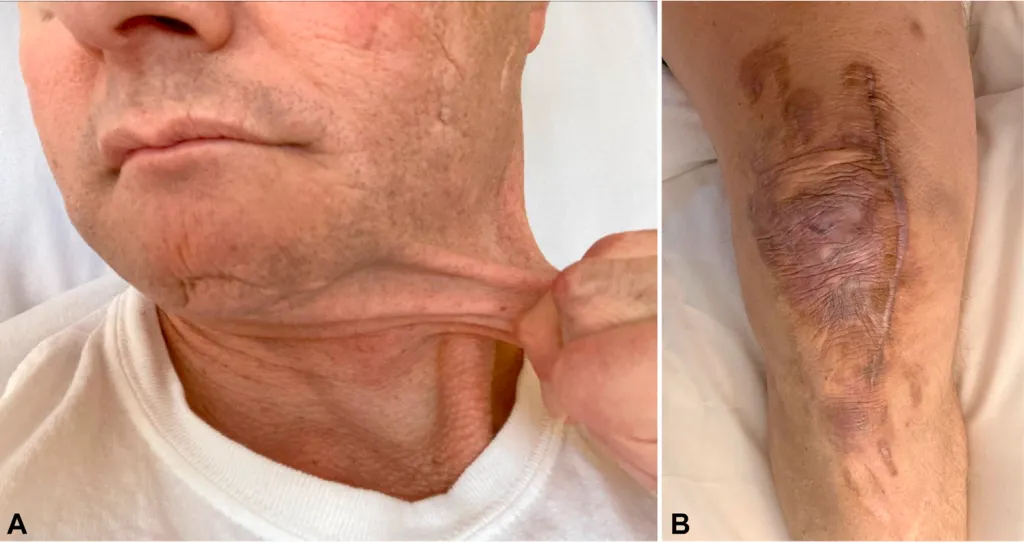
Рис. 2. Мужчина с классическим синдромом Элерса-Данлоа (патогенный вариант гена COL5A1). Отмечается (A) гиперрастяжимость кожи и (B) посттравматические рубцы с кожной атрофией («папирусная кожа») [7].
Классикоподобный тип
Классикоподобный тип синдрома Элерса–Данло обусловлен биаллельными патогенными вариантами в гене TNXB, кодирующего белок тенасцин-XB – гликопротеин внеклеточного матрикса (подтип 1) или в гене AEBP1, кодирующем карбоксипептидазаподобный аортальный протеин, ассоциированный с коллагеном внеклеточного матрикса (подтип 2); наследуются аутосомно-рецессивно. Кроме того, описан классикоподобный тип синдрома Элерса–Данло, подтип 3, ассоциированный с геном THBS2, кодирующем внеклеточный белок матрикса тромбоспондин II, данный подтип наследуется аутосомно-доминантно. Частота встречаемости не установлена, в литературе представлены данные о менее чем 40 пациентах. Большие критерии клинической диагностики классикоподобного СЭД включают следующие признаки:
-
гиперрастяжимая кожа с мягкой текстурой в отсутствие атрофических рубцов;
-
генерализованная гипермобильность суставов с вывихами/подвывихами (чаще плечевого и голеностопного суставов) или без таковых;
-
склонность к возникновению синяков / спонтанные экхимозы.
Малые критерии клинической диагностики классикоподобного СЭД включают:
-
деформации стоп: широкая передняя часть стопы, брахидактилия с избыточным количеством кожи; плоскостопие; вальгусная деформация большого пальца стопы;
-
отеки ног при отсутствии сердечной недостаточности;
-
легкая проксимальная и дистальная мышечная слабость;
-
аксональная полинейропатия;
-
атрофия мышц кистей и стоп;
-
акрогерия кистей рук, молоткообразные, клиновидные или короткие пальцы;
-
вагинальный/маточный/ректальный пролапс.
Также отмечается замедленное заживлением ран с аномальным атрофическим рубцеванием. К вариабельным проявлениям относятся желудочно-кишечные и мочеполовые нарушения, такие как разрыв кишечника, нарушение моторики кишечника, крипторхизм и грыжи; сосудистые осложнения, такие как пролапс митрального клапана и расширение корня аорты (с риском разрыва); скелетные аномалии.
Минимальные критерии, необходимые для постановки диагноза классикоподобного СЭД: все три больших критерия и семейный анамнез, соответствующий аутосомно-рецессивному типу наследования. Для постановки окончательного диагноза классикоподобного СЭД обязательно проведение подтверждающего молекулярно-генетического тестирования.
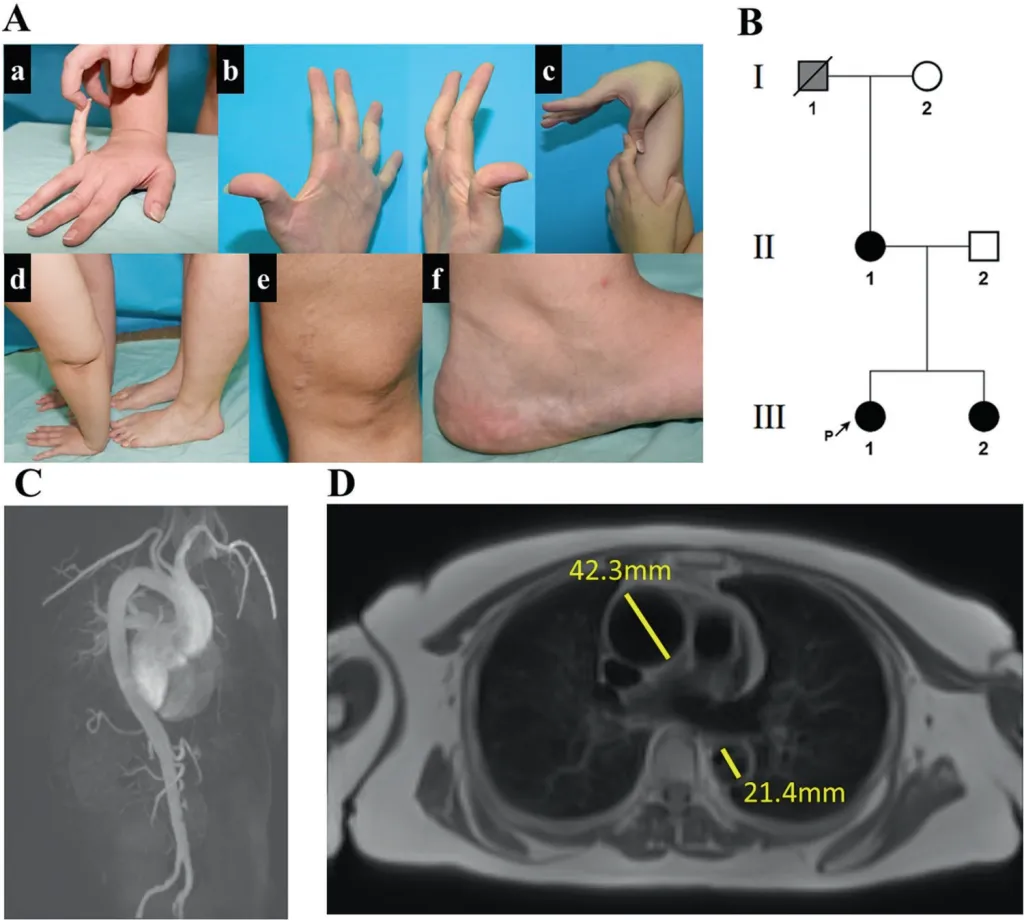
Рис. 3. Классикоподобный тип синдрома Элерса–Данло. A. (a–d) гипермобильность суставов (e) атрофические рубцы (f) пьезогенные папулы. B. Генеалогическое древо: черная заливка обозначает пораженных лиц (патогенный вариант в гене THBS2). C, D. МРТ грудной клетки и брюшной полости, демонстрирующая расширенную дугу аорты.
Гипермобильный тип
Гипермобильный тип синдрома Элерса–Данло. По-видимому, это самый частый тип синдрома Элерса–Данло (около 50% всех случаев СЭД), причем чаще (70% случаев) страдают женщины. Частота встречаемости составляет порядка 1:5000. Наследуется аутосомно-доминантно. Генетические причины данного типа точно не установлены. Он может быть связан с гаплонедостаточностью гена TNXB или изменением экспрессии других генов, контролирующих компоненты соединительной ткани, архитектонику экстрацеллюлярного матрикса, медиаторы воспаления и др. К большим критериям диагностики гипермобильного типа СЭД относят:
Критерий 1 (обязательный): гипермобильность суставов (≥5 баллов из 9 по шкале Бейтона);
Критерий 2: два или более из признаков A–C обязательно должны присутствовать (например: A и B; A и C; B и C; A и B и C).
Признак А: системные проявления заболевания соединительной ткани (всего должно не менее 5 признаков из перечисленных):
1. Необычно мягкая или бархатистая кожа;
2. Легкая гиперэластичность кожи;
3. Необъяснимые стрии, такие как стрии у подростков, мужчин или женщин допубертатного возраста без анамнестических указаний на значительное увеличение или уменьшения массы тела;
4. Двусторонние пьезогенные папулы на пятках;
5. Рецидивирующие или множественные абдоминальные грыжи (пупочная, паховая, бедренная)
6. Атрофические рубцы, затрагивающее как минимум два участка, без образования «папирусных» и/или гемосидерических рубцов, как это наблюдается при классическом СЭД;
7. Пролапс тазового дна, прямой кишки и/или матки у детей, мужчин или нерожавших женщин без анамнеза патологического ожирения или других известных предрасполагающих заболеваний;
8. Скученность зубов и высокое или узкое нёбо;
9. Арахнодактилия (положительный симптом Штейнберга или симптом Уокера с обеих сторон);
10. Соотношение размаха рук к росту ≥1,05;
11. Пролапс митрального клапана легкой или умеренной степени по ЭхоКГ;
12. Расширение корня аорты с Z-индексом > +2
Признак B: положительный семейный анамнез (наличие одного или более родственников первой степени родства соответствующих текущим диагностическим критериям гипермобильного СЭД).
Признак C: осложнения со стороны опорно-двигательного аппарата (должен быть хотя бы один признак их перечисленных):
1. Мышечно-скелетная боль как минимум в двух конечностях, повторяющаяся ежедневно в течение как минимум 3 месяцев;
2. Хроническая, распространенная боль в течение 3 месяцев;
3. Рецидивирующие вывихи суставов или явная нестабильность суставов при отсутствии травмы.
Критерий 3. Все следующие условия должны быть выполнены:
1. Отсутствие необычной хрупкости кожи, которая должна побудить к рассмотрению других типов синдрома Элерса-Данлоса;
2. Исключение других наследственных и приобретенных заболеваний соединительной ткани, включая аутоиммунные ревматологические заболевания.
3. Исключение альтернативных диагнозов, которые могут также включать гипермобильность суставов за счет мышечной гипотонии и/или слабости соединительной ткани. Альтернативные диагнозы и диагностические категории включают нервно-мышечные расстройства (например, миопатический СЭД или миопатия Бетлема), другие наследственные заболевания соединительной ткани (другие типы СЭД, синдром Лойса-Дитца, синдром Марфана) и скелетные дисплазии (например, несовершенный остеогенез).
Таким образом, диагноз гипермобильного типа синдрома Элерса–Данло в значительной степени является диагнозом исключения.
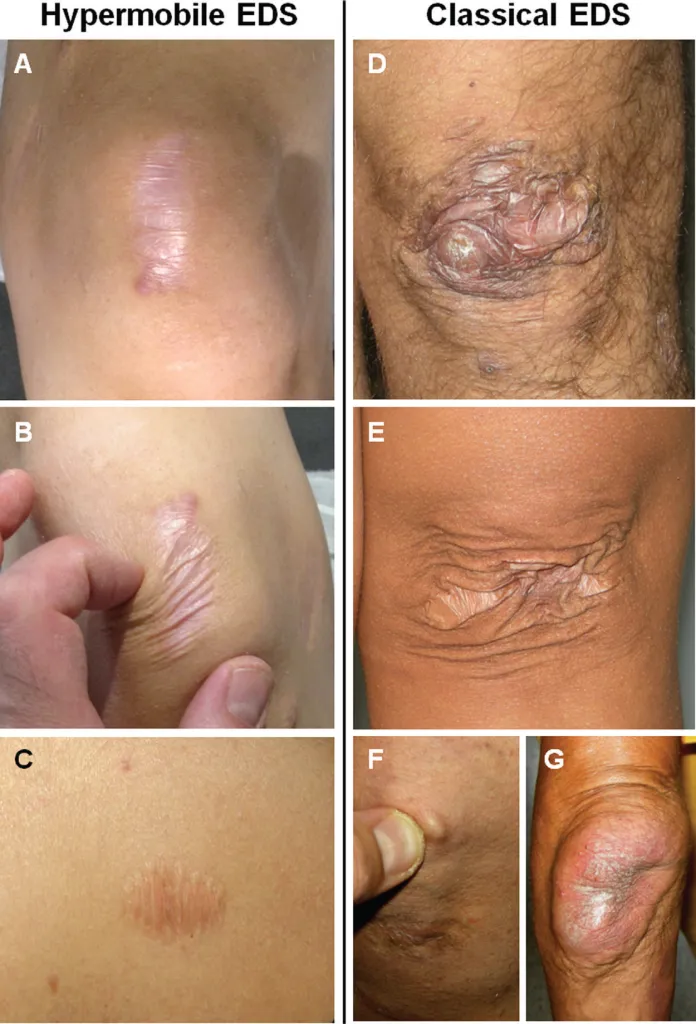
Рис. 4. Отличия кожных симптомов, наблюдаемые при гипермобильном и классическом типах синдрома Элерса-Данло.
Гипермобильный тип. (A) Посттравматический атрофический рубец у молодого человека. (B) Растягивание кожи выявляет легкую атрофию подлежащей дермы. (C) Рубец, вызванный задержкой заживления раны после иссечения меланоцитарного невуса у молодой женщины (C).
Классический тип. (D) Типичный «папирусный» гемосидериановый рубец после многократного повторного вскрытия раны и моллюскоидная псевдоопухоль у взрослого мужчины. (E) Папирусный рубец и cutis laxa у молодой женщины. (F) Подкожный сфероид. (G) Гигантская моллюскоидная псевдоопухоль в области локтя [1].
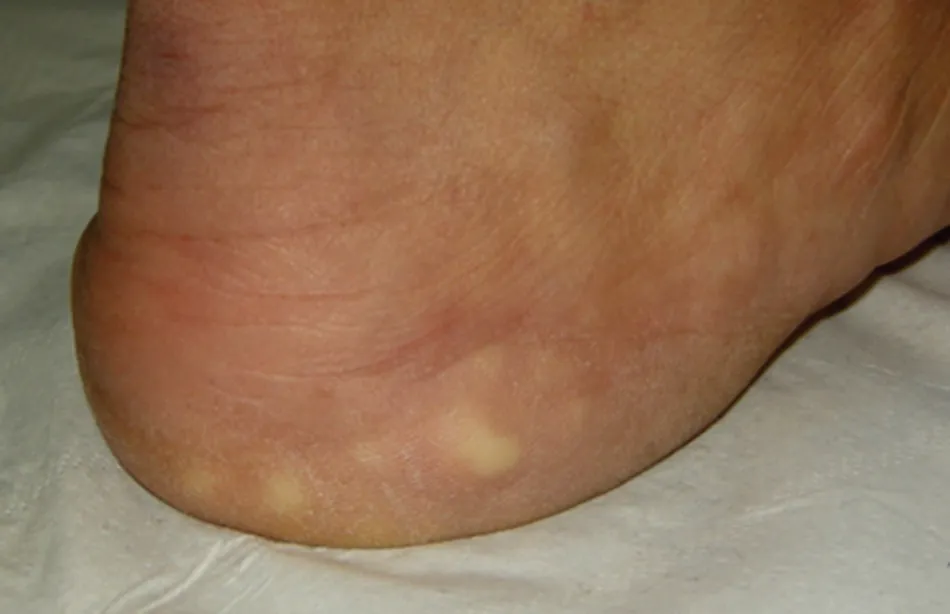
Рис. 5. Пьезогенные папулы представляют собой грыжи подкожной жировой ткани через фасцию. Часто они проявляются в виде бледых белых узелков только при нагрузке [1].
Сосудистый тип
Сосудистый (артериальный, экхимозный) тип синдрома Элерса–Данло обусловлен патогенными вариантами в гене COL3A1, кодирующем α1-цепь коллагена III типа (очень редко ─ патогенными вариантами гена COL1A1). Наследуется аутосомно-доминантно, крайне редко – аутосомно-рецессивно. Его частота 1:50 000–1:100 000 новорожденных. Это самый тяжелый по своей клинической симптоматике тип, отличается повышенной летальностью, он составляет 5–8% всех случаев СЭД. Большие клинические критерии диагностики сосудистого типа СЭД включают:
наличие близкого родственника с сосудистым типом СЭД (с подтвержденным патогенным вариантом гена COL3A1);
-
разрывы сосудов в молодом возрасте (до 40 лет);
-
спонтанная перфорация сигмовидной кишки (в отсутствие дивертикулов или других болезней кишечника);
-
разрыв матки в III триместре беременности (в отсутствие кесарева сечения в анамнезе);
-
образование фистулы каротидно-кавернозного синуса (в отсутствие травмы).
Малые критерии диагностики сосудистого типа СЭД включают:
-
синяки, не связанные с выявленной травмой и/или расположенные в необычных местах, например, на щеках или спине;
-
тонкая, полупрозрачная кожа с повышенной видимостью вен;
-
характерный внешний вид лица;
-
спонтанный пневмоторакс;
-
акрогерия;
-
косолапость;
-
врожденный вывих бедра;
-
гипермобильность мелких суставов;
-
разрыв сухожилий и мышц;
-
кератоконус;
-
рецессия десны и ранимость десен;
-
раннее начало варикозного расширения вен (до 30 лет и у нерожавших женщин)
Минимальные критерии, необходимые для постановки диагноза сосудистый тип СЭД: семейный анамнез заболевания, разрыв или расслоение артерий у лиц моложе 40 лет, необъяснимый разрыв сигмовидной кишки или спонтанный пневмоторакс при наличии других признаков, соответствующих сосудистому типу СЭД.
Кифосколиотический тип
Кифосколиотический тип синдрома Элерса–Данло обусловлен патогенными вариантами в гене PLOD1 или FKBP14, которые кодируют белки, участвующие в образовании пространственной структуры коллагена. Тип наследования аутосомно-рецессивный. Частота встречаемости предположительно составляет 1:100 000 живых новорожденных. Большие критерии клинической диагностики кифосколиотического типа СЭД включают:
-
врожденную мышечную гипотонию (симптомокомплекс «вялого ребенка»);
-
раннюю манифестацию кифосколиоза (чаще прогрессирующего, реже непрогрессирующего);
-
генерализованную гипермобильность суставов, вывихи/подвывихи (особенно коленных суставов).
Малые критерии клинической диагностики кифосколиотического типа СЭД включают:
-
гиперэластичность кожи;
-
легко образующиеся синяки на коже;
-
аневризма/разрыв артерии среднего размера;
-
остеопения/остеопороз;
-
голубые склеры;
-
грыжа (пупочная или паховая);
-
деформация грудной клетки;
-
марфаноидный тип телосложения;
-
косолапость;
-
нарушения рефракции (близорукость, гиперметропия).
Дополнительные критерии, специфичные для гена PLOD1:
-
хрупкость кожи (легкое образование синяков, рыхлая кожа, плохое заживление ран, атрофические рубцы);
-
хрупкость склер и глазных яблок или их разрыв;
-
микрокорнеа;
-
лицевые дисфорфии (низко расположенные ушные раковины, эпикант, антимонголоидный разрез глаз, синофриз, высокое небо);
Дополнительные критерии, специфичные для гена FKBP14:
-
врожденная тугоухость (сенсоневральная, кондуктивная или смешанная);
-
фолликулярный гиперкератоз;
-
атрофия мышц;
-
дивертикулы мочевого пузыря
Минимальные критерии, необходимые для постановки диагноза кифосколиотического типа СЭД: большой критерий 1 (врожденная мышечная гипотония) и большой критерий 2 (врожденный или ранний кифосколиоз) + большой критерий 3 (гипермобильность суставов) и/или три малых критерия (общие или специфические для гена критерии).
Подтверждающее молекулярно-генетическое тестирование является обязательным для постановки окончательного диагноза кифосколиотического типа СЭД.
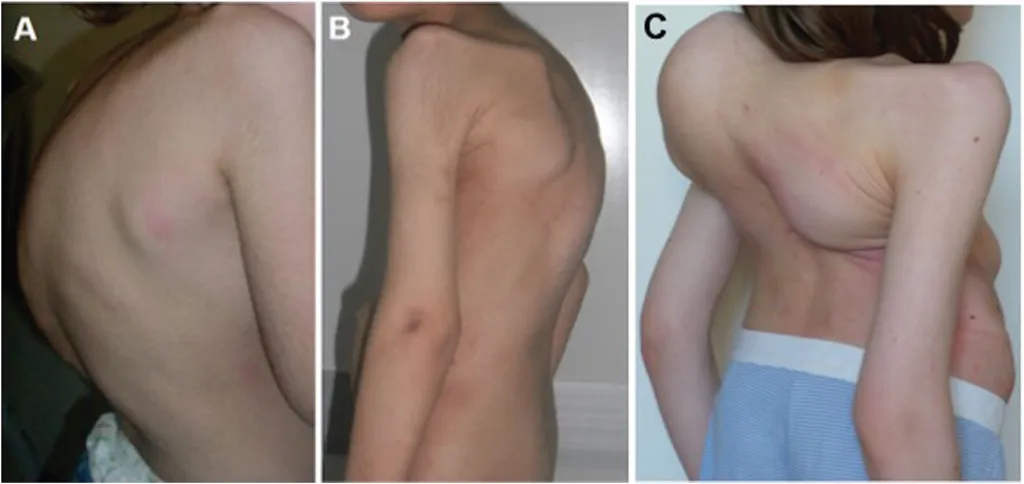
Рис. 6. Кифосколиотический тип синдрома Элерса–Данло у разных пациентов [15].
Артрохалазисный тип
Артрохалазисный тип синдрома Элерса–Данло обусловлен гетерозиготными патогенными вариантами в генах генов COL1A1 или COL1A2, ограниченными экзонами/интронами 5 и 6. Указанные гены кодируют α1 - и α2 -цепи коллагена I типа соответственно. Наследуется аутосомно-доминантно. Частота не установлена; в литературе сообщается о более 30 больных, диагноз которых доказан молекулярно-генетически. К большим диагностическим клиническим критериям артрохалазисного типа СЭД относят:
-
врожденный двусторонний вывих шейки бедренной кости;
-
генерализованную гипермобильность суставов, вывихи/подвывихи суставов;
-
гиперрастяжимость кожи.
К малым диагностическим клиническим критериям артрохалазисного типа СЭД относят:
-
гипотонию мышц;
-
кифосколиоз;
-
умеренную остеопения;
-
хрупкость тканей, включая атрофические рубцы;
-
легко образующиеся синяки на коже.
Минимальные критерии, необходимые для постановки диагноза артрохалазисного типа СЭД: большой критерий 1 (врожденный двусторонний вывих шейки бедренной кости): + либо большой критерий 3 (гиперрастяжимость кожи) или большой критерий 2 (генерализованная гипермобильность суставов с множественными вывихами/подвывихами) и как минимум два малых критерия
Подтверждающее молекулярно-генетическое тестирование обязательно для постановки окончательного диагноза артрохалазисного типа СЭД.
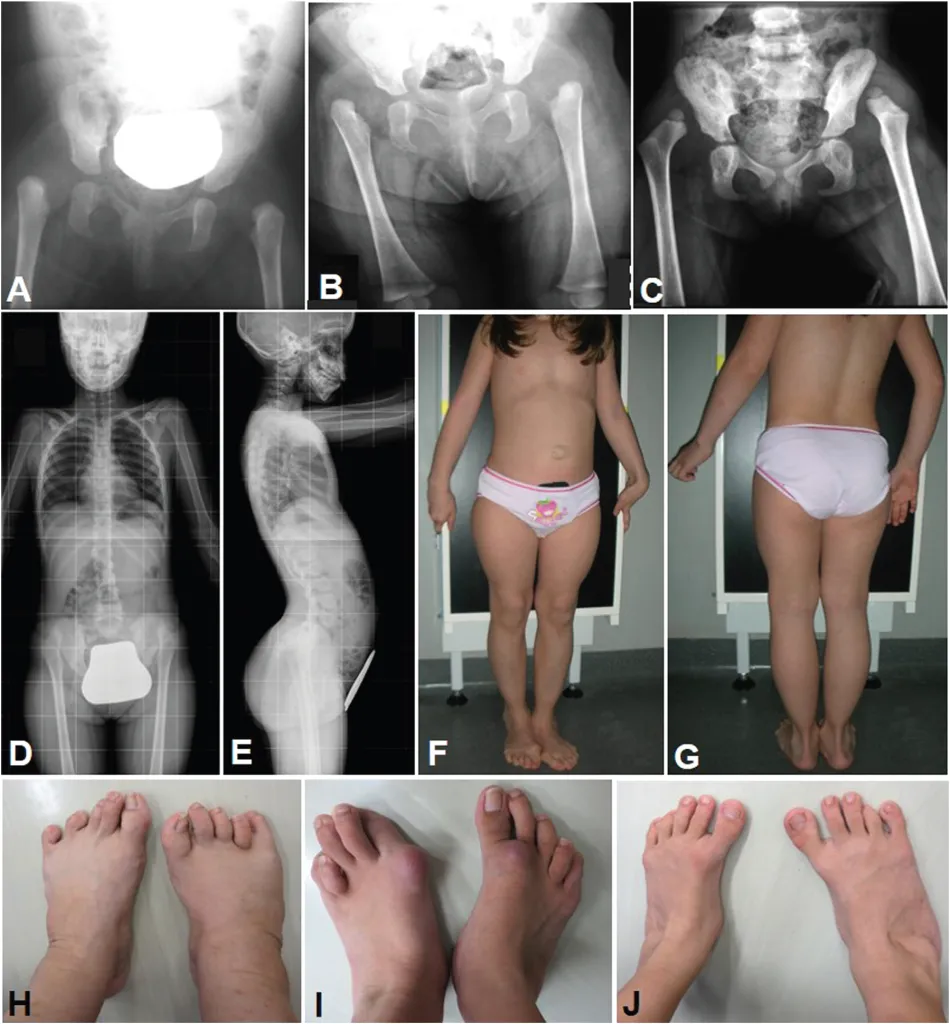
Рис. 7. Артрохалазисный тип синдрома Элерса–Данло. Девочка (A–G) с патогенным вариантом в гене COL1A2 и мать с двумя сыновьями (H–J) с патогенным вариантом в гене COL1A2. (A) Рентгенограммы тазобедренного сустава в возрасте 7 дней, показывающие врожденный двусторонний вывих бедра и деформации бедренной кости и вертлужной впадины. (B и C) Состояние вывиха бедра в возрасте 5 месяцев и 3 лет, соответственно. (D) Передняя рентгенограмма всего тела в возрасте 11 лет, показывающая безуспешное лечение вывиха бедра с помощью пояса и ортеза. (E) Левая боковая рентгенограмма всего тела в возрасте 11 лет, показывающая поясничный лордоз. (F и G) Пациент в возрасте 9 лет с пупочной грыжей, лордозом позвоночника и деформациями стоп. Деформации стоп у матери в возрасте 38 лет (H), ее первого сына в возрасте 14 лет (I) и ее второго сына в возрасте 5 лет (J) [15].
Сердечно-клапанный тип
Сердечно-клапанный тип синдрома Элерса–Данло обусловлен биаллельными патогенными вариантами гена COL1A2, ведущими к нарушению синтеза и полному отсутствию proα2 (I) пептидной цепи коллагена I типа. Частота не установлена; в литературе сообщается о единичных случаях заболевания. Большие критерии клинической диагностики сердечно-клапанного типа СЭД включают:
- поражение аортального или митрального клапанов сердца (может отсутствовать у детей младше 10 лет);
- изменения кожи (тонкая гиперрастяжимая с атрофическими рубцами, склонная к появлению синяков);
- гипермобильность суставов (генерализованная или ограниченная мелкими суставами).
Среди поражений сердца у больных встречаются недостаточность митрального/аортального клапанов, пролапс митрального/аортального клапанов с регургитацией, расширение корня аорты.
Малые критерии клинической диагностики сердечно-клапанного типа СЭД включают:
- паховая грыжа;
- деформация грудной клетки (особенно вогнутая грудная клетка);
- вывихи суставов;
- деформации стопы: плоскостопие, плосковальгусная деформация стопы, вальгусная деформация большого пальца стопы;
Минимальные критерии, позволяющие диагностировать сердечно-клапанного типа СЭД: большой критерий 1 (поражение клапанов сердца) и семейный анамнез, соответствующий аутосомно-рецессивному типу наследования + либо ещё один большой критерий, либо как минимум два малых критерия.
Подтверждающее молекулярно-генетическое тестирование является обязательным для постановки окончательного диагноза сердечно-клапанного типа СЭД.
Кожный (дерматоспараксисный) тип
Кожный или дерматоспараксисный тип синдрома Элерса–Данло обусловлен патогенными вариантами в гене ADAMTS2, кодирующем проколлаген-протеиназу. Наследуется аутосомно-рецессивно. В литературе имеются описания 15 больных, диагноз которых доказан молекулярно-генетически. Большие критерии клинической диагностики дерматоспараксисного типа СЭД включают:
- исключительная подверженность кожи повреждениям (включая врожденные или постнатальные разрывы);
- характерные черепно-лицевые особенности (экзофтальм с отечными веками и избытком кожи вокруг глаз, складка эпиканта, косо нисходящие глазные щели, голубые склеры, большие роднички и/или широкие черепные швы, замедленное закрытие родничков, гипоплазия подбородка);
- избыточная, «лишняя», вялая кожа на запястьях и в области лодыжек;
- выраженные ладонные складки;
- склонность к подкожным гематомам и геморрагиям;
- пупочная грыжа;
- постнатальная задержка роста;
- укорочение конечностей, кистей и стоп;
- перинатальные осложнения (переломы костей свода черепа, геморрагии, рыхлая пуповина, разрывы кожи, пневмоторакс).
Малые критерии клинической диагностики дерматоспараксисного типа СЭД включают:
- мягкая рыхлая текстура кожи;
- гиперэластичность кожи;
- атрофические рубцы;
- спонтанные разрывы внутренних органов (например, разрыв мочевого пузыря, разрыв диафрагмы, выпадение прямой кишки);
- задержка моторного развития;
- остеопения;
- гирсутизм;
- зубные аномалии;
- нарушения рефракции (близорукость, астигматизм), косоглазие.
Минимальные критерии, позволяющие диагностировать дерматоспараксисный тип СЭД:
большой критерий 1 (выраженная хрупкость кожи) и большой критерий 2 (характерные черепно-лицевые дисморфии) + либо ещё один большой критерий и/или три малых критерия.
Подтверждающее молекулярно-генетическое тестирование является обязательным для постановки окончательного диагноза дерматоспараксисного типа СЭД.
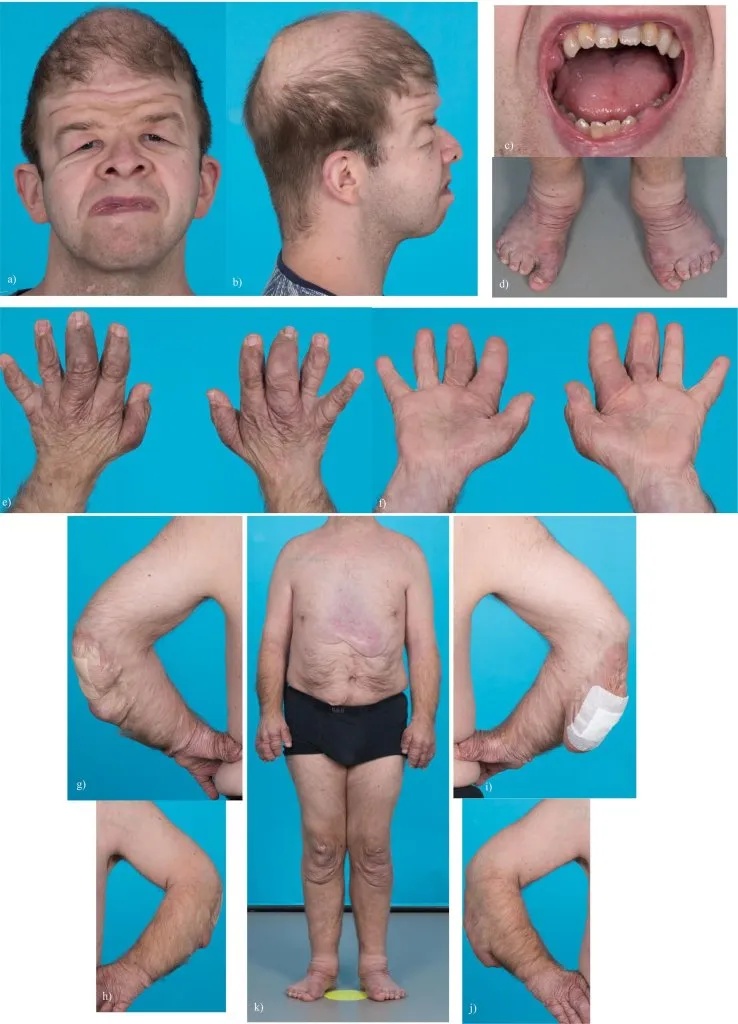
Рис. 8. Дерматоспараксисный тип синдрома Элерса-Данло у пациента 26 лет: (a) лицо анфас: складки кожи на лице, вдавленная и широкая переносица, складки эпиканта с избытком периорбитальной кожи/дерматохалазис, косо нисходящие глазные щели, ноздри, обращенные вперед; (b) лицо в профиль: низко расположенные, повернутые назад уши, низкая передняя и задняя линия роста волос, избыток кожи на лбу, «башенный череп»; (c) ротовая полость: неправильный прикус со скученностью зубов; (d) укороченные стопы и пальцы ног с чрезмерными кожными складками и двусторонним плоскостопием; (e) тыльная сторона кисти: чрезмерное количество кожи на пальцах; (f) ладонная сторона кисти: усиленное образование морщин на коже ладоней; (g) задняя сторона левого локтя: хронический бурсит с увеличенными кожными складками; (h) передний вид левого локтя; (i) правый локоть, вид сзади: хронический бурсит с чрезмерными кожными складками; (j) передняя сторона правого предплечия; (k) на снимке всего тела видны избыточные кожные складки и вены на груди [12].
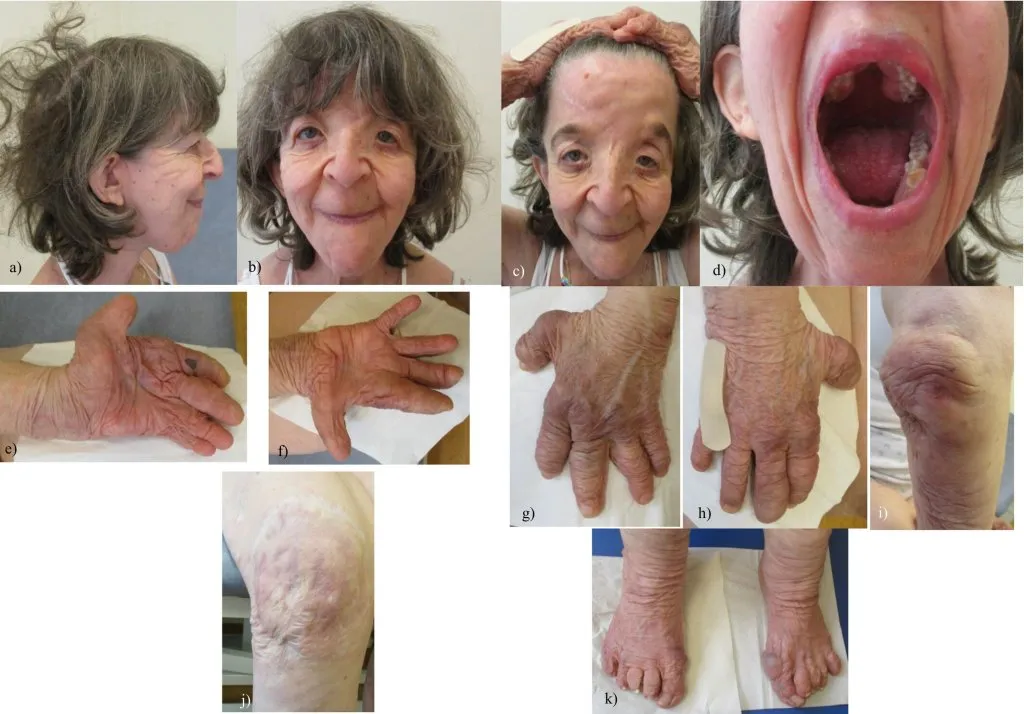
Рис. 9. Дерматоспараксисный тип синдрома Элерса-Данло у пациентки 42 лет: (a) лицо в профиль: клювовидный нос, гладкие, обвисшие мочки ушей, ретрогнатия, имплантат подбородка; (b) лицо анфас: длинный фильтр, складки эпиканта, косо нисходящие глазные щели, гипертелоризм, широкая переносица, дерматохалазис и усиленное образование морщин над скуловой дугой и носом, голубые склеры, выступающие носогубные складки; (c) лицо анфас с приподнятыми волосами: высокий лоб, атрофические рубцы, низко расположенные уши, заостренный подбородок; (d) ротовая полость: дугообразное небо, гипертрофия десен, нарушения прикуса с легкой скученностью зубов, изменение цвета зубов; (e, f) ладонная сторона кистей рук: усиленное образование складок на ладонях, укороченные пальцы, избыток кожи на пальцах и более выраженное смещение в локтевую сторону слева; (g, h) тыльная сторона кистей рук: избыток кожи на пальцах; (i) избыток кожи над правым локтем; (j) левое колено с большим расширенным атрофическим рубцом и избытком кожи; (k) правое колено с расширенным атрофическим рубцом; (l) тыльная сторона стоп: укороченные стопы и пальцы с избытком кожи и вальгусной деформацией большого пальца стопы [12].
Мышечно-контрактурный тип
Мышечно-контрактурный тип синдрома Элерса–Данло обусловлен патогенными вариантами в гене CHST14 (мышечно-контрактурный подтип 1, или дистальный артрогрипоз, синдром приведенного большого пальца и косолапости) или гена DSE (мышечно-контрактурный подтип 2). Указанные гены кодируют, соответственно, дерматан-4-сульфотрансферазу-1 и дерматансульфатэпимеразу-1 – ферменты, участвующие в биосинтезе гликозаминогликанов. Наследуется аутосомно-рецессивно. Частота не установлена. В литературе представлена характеристика более 40 больных. Большие критерии клинической диагностики мышечно-контрактурного типа СЭД включают:
- врожденные множественные контрактуры по типу приведения-сгибания, эквино-варусную косолапость;
- черепно-лицевые аномалии (большие роднички, гипертелоризм, короткие антимонголоидные глазные щели, короткий нос, гипоплазия колумелла, длинный фильтр, голубые склеры, низко расположенные ротированные ушные раковины, высокое небо, тонкая верхняя губа);
- гиперрастяжимость кожи, склонность к возникновению синяков, атрофические рубцы, выраженные складки на ладони.
Малые критерии клинической диагностики мышечно-контрактурного типа СЭД включают:
- рецидивирующие или хронические вывихи;
- деформации грудной клетки (плоская, вогнутая);
- деформации позвоночника (сколиоз, кифосколиоз);
- аномалии пальцев (конусовидные, тонкие, цилиндрические);
- прогрессирующая косолапость (вальгусная деформация, плоская деформация);
- большие подкожные гематомы;
- хронические запоры;
- дивертикулы толстой кишки;
- пневмоторакс / пневмогемоторакс;
- нефролитиаз / цистолитиаз;
- гидронефроз;
- крипторхизм у мужчин;
- косоглазие;
- нарушение рефракции (близорукость, астигматизм);
- глаукома.
Минимальные критерии, необходимые для постановки диагноза мышечно-контрактурного типа СЭД:
1) При рождении или в раннем детстве: большой критерий 1 (врожденные множественные контрактуры) + большой критерий 2 (черепно-лицевые аномалии).
2) В подростковом и взрослом возрасте: большой критерий 1 (врожденные множественные контрактуры) + большой критерий 3 (характерные кожные особенности).
Подтверждающее молекулярно-генетическое тестирование является обязательным для постановки окончательного диагноза мышечно-контрактурного типа СЭД.
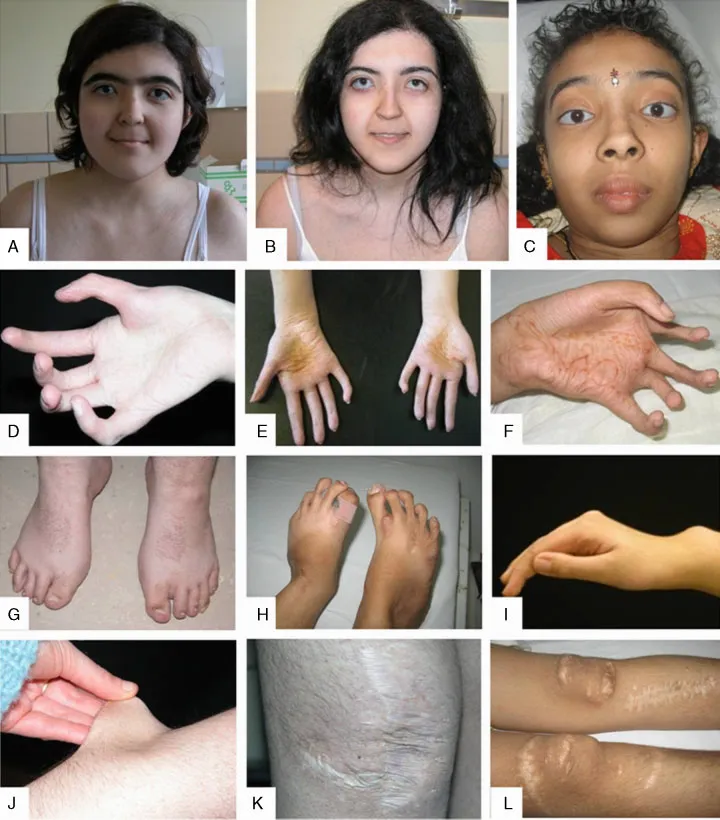
Рис. 10. Мышечно-контрактурный тип синдрома Элерса-Данло. А–С: Черепно-лицевые дисморфии с уплощенным профилем, гипоплазией скул, густыми бровями и синофрией, косо нисходящими глазными щелями, голубыми склерами, микрокорнеа, длинным фильтром, тонкой верхней губой и выступающей челюстью с заостренным подбородком. D– F: Кисти рук и стопы с характерными особенностями: конусовидные пальцы со сгибательными контрактурами и чрезмерным сморщиванием кожи ладоней. G: деформация стоп - короткая широкая стопа и короткие пальцы ног. H: удлиненные конусовидные пальцы ног с контрактурами, псевдоопухолью и атрофическими рубцами (рубцы по типу «папиросной бумаги»). I: вывих лучелоктевого сустава. J–L: Тонкая и гиперэластичная кожа и атрофические рубцы по типу «папиросной бумаги» [13].
Спондило-диспластический тип
Спондило-диспластический (прогероидный) тип синдрома Элерса–Данло обусловлен патогенными вариантами в генах B4GALT7 (подтип 1) или B3GALT6 (подтип 2), кодирующих, соответственно, галактозилтрансферазу-1 и -2, участвующих в синтезе гликозаминогликанов. Подтип 3 обусловлен патогенными вариантами гена SLC39A13, который кодирует трансмембранный переносчик, контролирующий транспорт цинка в цитозоль. Наследуется аутосомно-рецессивною. Частота не установлена. Описаны около 100 пациентов с тремя подтипами синдрома. Большие критерии клинической диагностики спондило-диспластического типа СЭД включают:
- низкорослость;
- мышечная гипотония (от тяжелой врожденной до легкой, поздно манифестирующей);
- искривление длинных трубчатых костей.
Малые критерии клинической диагностики спондило-диспластического типа СЭД включают:
- гиперэластичность кожи; мягкая рыхлая тонкая полупрозрачная кожа;
- плоскостопие;
- задержка двигательного развития;
- остеопения;
- задержка когнитивного развития.
Малые критерии, специфичные для гена B4GALT7:
- радиоульнарный синостоз;
- двусторонние контрактуры локтевых суставов или ограниченная подвижность локтевых суставов;
- гипермобильность суставов;
- поперечная ладонная борозда;
- характерные черепно-лицевые дисморфии (при биаллельных патогенных вариантах гена B4GALT7 могут наблюдаться: треугольное лицо, широко расставленные глаза, экзофтальм, узкий рот, низко расположенные уши, редкие волосы на голове, аномалии зубов, плоское лицо, широкий лоб, голубые склеры, расщелина нёба);
- характерные рентгенологические признаки (при биаллельных патогенных вариантах гена B4GALT7 могут наблюдаться: лучелоктевой синостоз, расширение метафизов, остеопения, подвывих или вывих головки лучевой кости, короткие ключицы с широкими медиальными концами);
- тяжелая гиперметропия;
- помутнение роговицы.
Малые критерии, специфичные для гена B3GALT6:
- прогрессирующий кифосколиоз (врожденный или с ранним началом);
- гипермобильность суставов (генерализованная или ограниченная дистальными суставами, с вывихами суставов);
- контрактуры суставов, особенно суставов кистей (врожденные или прогрессирующие);
- аномалии пальцев (арахнодактилия, тонкие, конусовидные, лопатовидные, с широкими дистальными фалангами);
- косолапость;
- характерные черепно-лицевые дисморфии (при биаллельных патогенных вариантах гена B3GALT6 могут наблюдаться: гипоплазия средней части лица, выступающий лоб, экзофтальм, голубые склеры, косо нисходящие глазные щели, вдавленная переносица, длинная верхняя губа, низко расположенные уши, микрогнатия, аномальное строение зубов, расщелина нёба, редкие волосы);
- изменение цвета зубов, дисплазия зубов;
- характерные рентгенологические признаки (при биаллельных патогенных вариантах гена B3GALT6 могут наблюдаться: платиспондилия, передний клювовидный выступ тела позвонка, короткая подвздошная кость, выступающий малый трохантер, дисплазия вертлужной впадины, расширение метафизов, метафизарная дисплазия головки бедренной кости, вывих головки лучевой кости, чрезмерная трубчатость костей (overtubulation), искривление длинных костей, генерализованный остеопороз, зажившие переломы; краниосиностоз и лучелоктевой дизостоз были зарегистрированы у одного пациента);
- остеопороз с множественными спонтанными переломами;
- аневризма восходящей аорты;
- гипоплазия легких, рестриктивное заболевание легких.
Малые критерии, специфичные для гена SLC39A13:
- экзофтальм, голубые склеры;
- морщинистые ладони;
- атрофия тенара и конусовидные пальцы;
- гипермобильность дистальных суставов;
- характерные рентгенологические признаки (при биаллельных патогенных вариантах гена SLC39A13 могут наблюдаться: легкая или умеренная платиспондилия, легкая или умеренная остеопения позвоночника, тонкая подвздошная кишка, плоские проксимальные эпифизы бедренных костей, короткие широкие шейки бедренных костей).
Минимальные критерии, необходимые для постановки диагноза спондило-диспластический тип СЭД: большой критерий 1 (низкий рост) + большой критерий 2 (мышечная гипотония) + характерные рентгенологические аномалии и как минимум три других малых критерия.
Подтверждающее молекулярно-генетическое тестирование является обязательным для постановки окончательного диагноза спондило-диспластический тип СЭД.
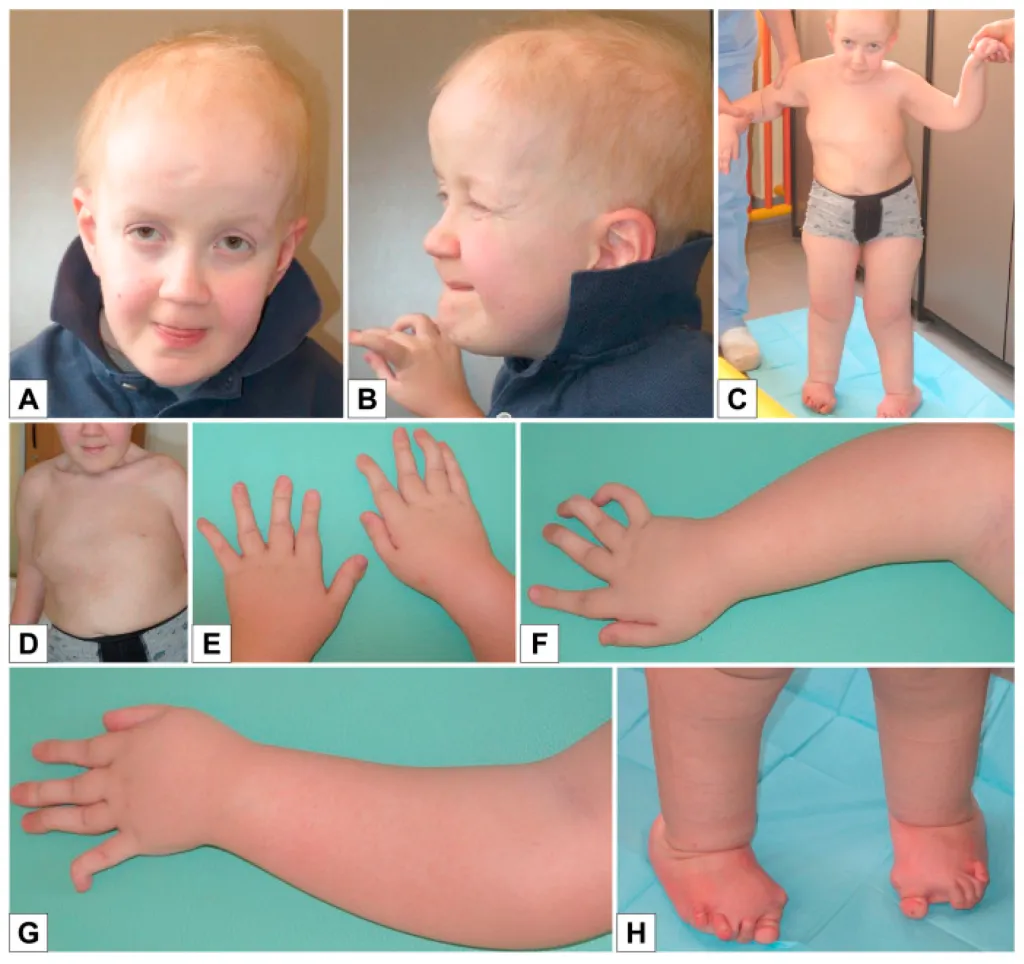
Рис. 11. Спондило-диспластический тип синдрома Элерса-Данло у пациента 12 лет (патогенный вариант в гене B3GALT6). A–C: Редкие волосы, высокий выступающий лоб, редкие брови, глубоко посаженные глаза, голубые склеры, гипоплазия колумеллы, большие уши; D–H: тонкая, бледная, чрезвычайно мягкая кожа, с выступающими венами на туловище и конечностях, ограниченное разгибание локтя, гиперэластичность кожи и гипермобильность дистальных суставов, особенно кистей рук, длинные и сужающиеся пальцы. Стопы: гипоплазия ногтей, короткие, перекрывающиеся пальцы ног, вальгусная деформация большого пальца стопы [14].
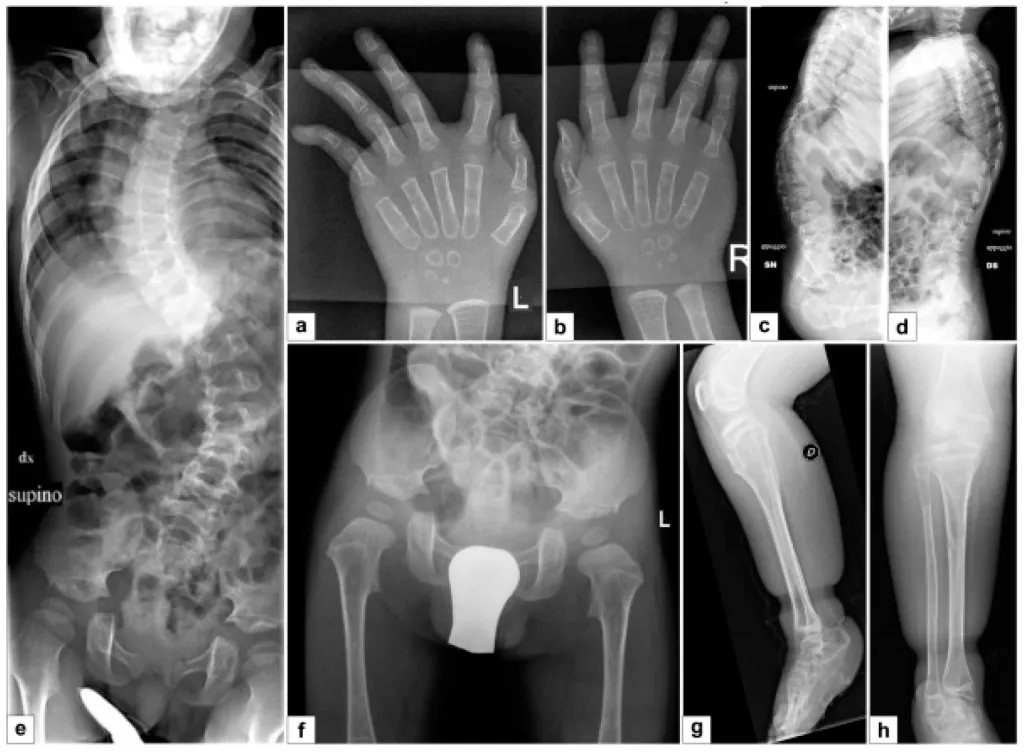
Рис. 12. Спондило-диспластический тип синдрома Элерса-Данло у пациента 12 лет (патогенный вариант в гене B3GALT6). А–Н: тяжелый кифосколиоз с ранним началом, остеопения, истончение пястных костей и фаланг [14].
Периодонтический тип
Периодонтический тип синдрома Элерса–Данло обусловлен патогенными вариантами в генах C1R и C1S, кодирующих субъединицы компонентов комплемента. Наследуется аутосомно-доминантно. Частота встречаемости не установлена. Сообщается о более 100 больных с данным типом. Большие критерии клинической диагностики периодонтического типа СЭД включают:
- тяжелый периодонтит с ранним началом (в детском или подростковом возрасте);
- отсутствие прикрепления десны;
- атрофия и гиперпигментация кожи голеней;
- аналогичные признаки у родственника первой степени родства.
Малые критерии клинической диагностики периодонтического типа СЭД включают:
- легкое образование синяков;
- гипермобильность суставов, преимущественно дистальных;
- гиперэластичность и хрупкость кожи, аномальные рубцы (широкие и/или атрофические);
- повышенная частота инфекций;
- грыжи;
- марфаноподобные черты лица;
- акрогерия;
- выраженная подкожная васкуляризация.
Минимальные критерии, необходимые для постановки диагноза периодонтического типа СЭД: большой критерий 1 (тяжелый периодонтит с ранним началом) или большой критерий 2 (отсутствие прикрепления десны) + по крайней мере два других больших критерия и один малый критерий.
Подтверждающее молекулярно-генетическое тестирование обязательно для постановки окончательного диагноза периодонтического типа СЭД.
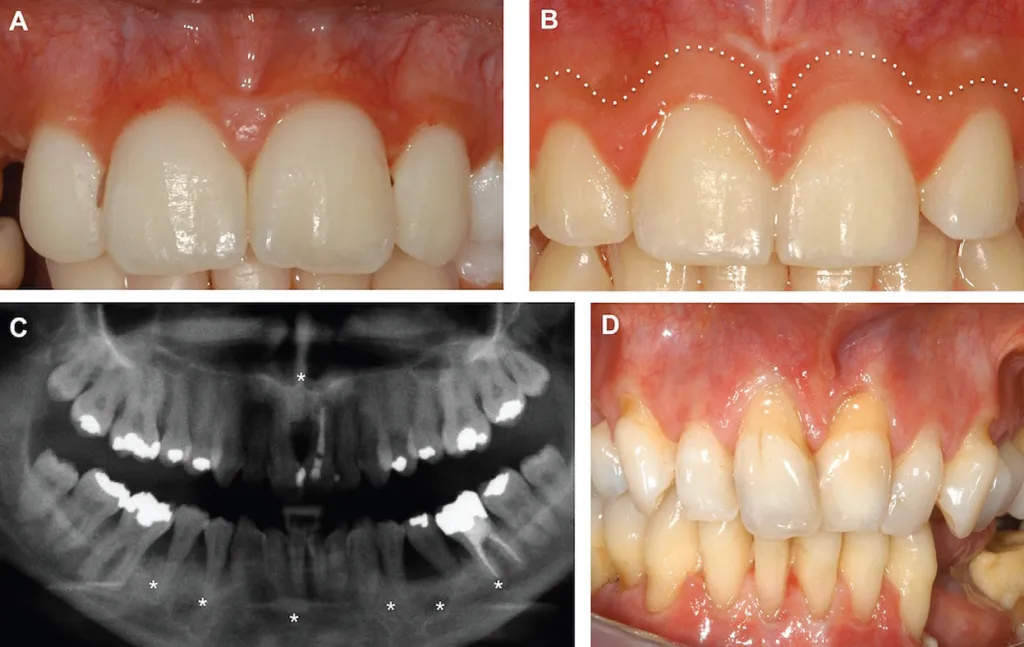
Рис. 13. Периодонтический тип синдрома Элерса–Данло. (A) У ребенка с периодонтическим типом СЭД кератинизированная десна отсутствует; слизистая оболочка полости рта распространяется до свободного края десны и межзубных сосочков и очень хрупкая. (B) Ткани десен здорового ребенка. Десна кератинизирована и плотно связана с подлежащей надкостницей посредством коллагеновых структур, выполняя защитную функцию во время жевания. Граница между десной и альвеолярной слизистой оболочкой — это слизисто-десневое соединение (пунктирная линия). Слизистая оболочка полости рта не кератинизирована и лишь слабо связана с надкостницей; поэтому она более хрупкая. (C) Стоматологический рентгеновский снимок пациента с пСЭД в возрасте 29 лет. Обратите внимание на выраженную потерю периодонтальной кости (звездочки). (D) Клиническая картина того же пациента в возрасте 30 лет. Премоляры на левой нижней челюсти за это время выпали без образования пародонтальных карманов, несмотря на хорошую гигиену полости рта. Обратите внимание на отсутствие кератинизированной десны и рецессию десен.
Миопатический тип (миопатия Бетлема-2)
Миопатический тип синдрома Элерса–Данло (миопатия Бетлема-2) обусловлен патогенными вариантами в гене COL12A1, который кодирует 3 α-цепи коллагена XII типа. Наследуется аутосомно-доминантно, в то же время описаны пациенты с биаллельными патогенными вариантами (аутосомно-рецессивное наследование). Частота встречаемости не установлена. В литературе сообщается о более 15 больных, диагноз которых доказан молекулярно-генетически. К большим критериям клинической диагностики миопатического типа СЭД относят:
- врожденную мышечную гипотонию и/или мышечную атрофию (отмечена положительная динамика с возрастом);
- контрактуры проксимальных суставов (коленные, тазобедренные, локтевые);
- гипермобильность дистальных суставов.
К малым критериям клинической диагностики миопатического типа СЭД относят:
- мягкая рыхлая кожа;
- атрофические рубцы;
- задержка двигательного развития;
- миопатия по данным биопсии мышц.
Минимальные клинические критерии, необходимые для постановки диагноза миопатического типа СЭД: большой критерий 1 (врожденная мышечная гипотония, улучшающаяся с возрастом) + либо ещё один большой критерий и/или: три малых критерия.
Подтверждающее молекулярно-генетическое тестирование обязательно для постановки окончательного диагноза миопатического типа СЭД.
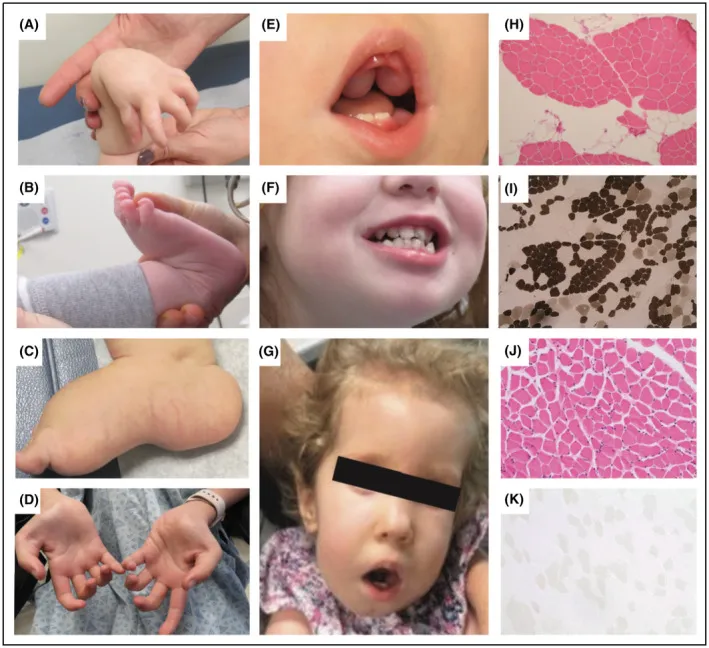
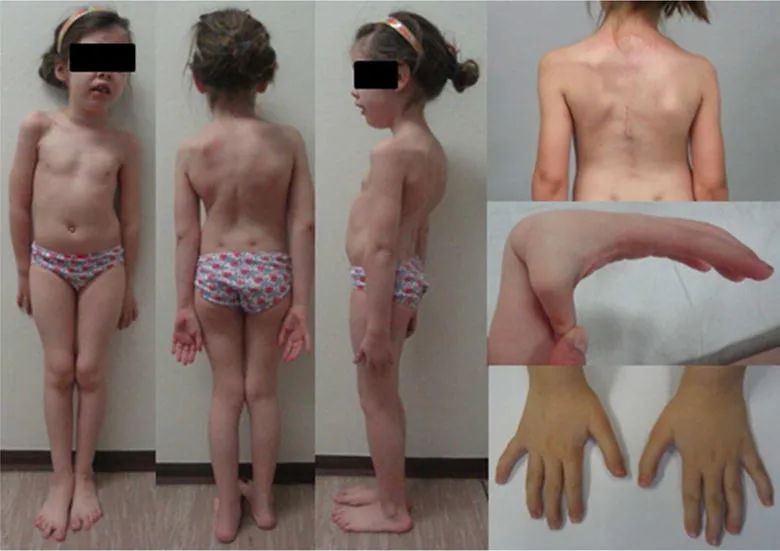
Рис. 15. Миопатический тип синдрома Элерса–Данло (миопатия Бетлема-2). У девочки 7 лет наблюдается легкая дисморфия черт лица (длинное, безэмоциональное лицо, открытый рот, микрогнатия, увеличенные диспластические уши), сколиоз, длинные пальцы рук и ног с широким «сандальным» промежутком и вальгусная деформация стоп. Показана спина пациентки после операции по поводу сколиоза в возрасте 8 лет. Наблюдается дистальная гипермобильность суставов с переразгибанием большого пальца относительно предплечья, а также длинные тонкие пальцы [18].
Синдром хрупкости роговицы
Синдром хрупкости роговицы (подтип синдрома Элерса–Данло) обусловлен патогенными вариантами в генах ZNF469 и PRDM5 (продукты этих генов оказывают регулирующее влияние на экспрессию ряда генов, кодирующих структуры внеклеточного матрикса). Наследуется аутосомно-рецессивно. Частота встречаемости не установлена. Известно о более 60 пациентах с данным заболеванием. Большие критерии клинической диагностики синдрома хрупкости роговицы включают:
тонкая роговица (толщина менее 400 мкм) с разрывами или без таковых;
прогрессирующий кератоконус с ранним началом;
прогрессирующий кератоглобус с ранним началом;
- голубые склеры.
Малые критерии клинической диагностики синдрома хрупкости роговицы включают:
энуклеация или рубцевание роговицы в результате предыдущего разрыва;
прогрессирующая потеря глубины стромы роговицы, особенно в центральной части роговицы;
высокая миопия с нормальной или умеренно увеличенной аксиальной длиной глаза;
отслойка сетчатки;
прогрессирующая тугоухость, часто со смешанная кондуктивная/сенсоневральная;
гиперэластичные барабанные перепонки;
дисплазия тазобедренного сустава;
мышечная гипотония в младенческом возрасте, обычно легкой степени;
сколиоз;
арахнодактилия;
гипермобильность дистальных суставов;
плоскостопие, вальгусная деформация большого пальца стопы;
легкие контрактуры пальцев (особенно 5-го)
мягкая, бархатистая полупрозрачная кожа.
Минимальные критерии, необходимые для диагностики синдрома хрупкости роговицы: большой критерий 1 (тонкая роговица с разрывами или без таковых; центральная толщина роговицы часто <100 мкм) + или по крайней мере один большой критерий и/или три малых критерия. Подтверждающее молекулярно-генетическое тестирование обязательно для постановки окончательного диагноза синдрома хрупкой роговицы.
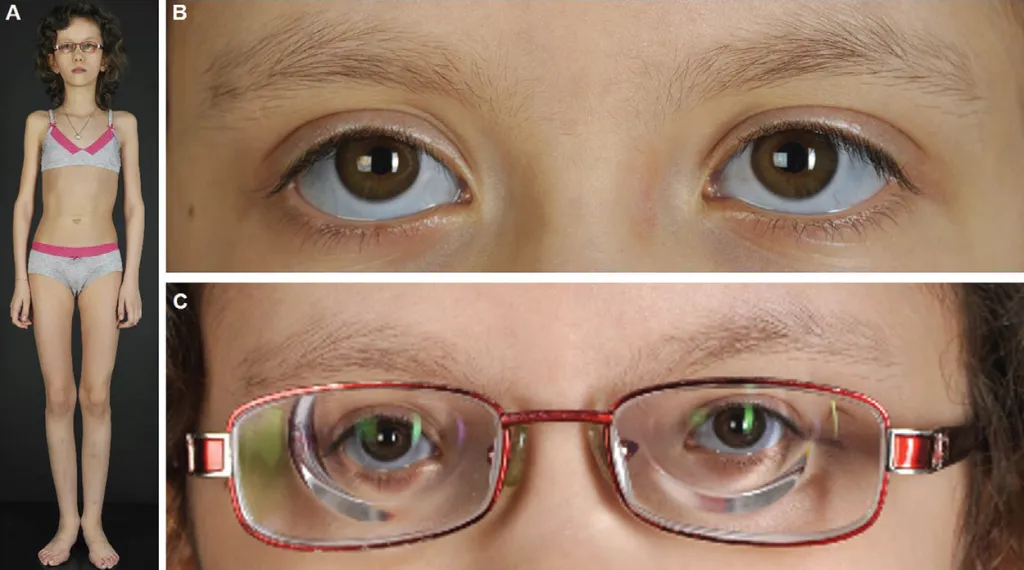
Рис. 16. Синдром хрупкой роговицы у пациентки 13 лет, гомозиготной по патогенному варианту в гене PRDM5: (A) Марфаноидный тип телосложения; бархатистая кожа, гематомы голени и двусторонняя вальгусная деформация большого пальца стопы, воронкообразная деформация грудной клетки. Плечи симметричные, позвоночник прямой. Лицо: вдавленная переносица и выступающий подбородок. (B) Голубые склеры. (C) Ношение защитных очков после успешной двусторонней пластики роговицы [15].
***
Помимо 13 типов синдрома Элерса–Данло, описанных в 2017 г. Международным консорциумом, в OMIM описаны вариант синдрома Элерса-Данлоса, ассоциированный с патогенными вариантами в гене FLNA ─ перивентрикулярная гетеротопия, характеризующаяся узловой гетеротопией головного мозга, гипермобильностью суставов и развитием дилатации аорты в раннем взрослом возрасте.
Молекулярно-генетическая диагностика синдрома Элерса-Данло
Диагностика синдрома Элерса-Данло входит в тест Исследование панели генов наследственной дисплазии соединительной ткани по результатам полноэкзомного секвенирования. Данная панель позволяет не только выполнять диагностику синдрома Элерса-Данло, но и проводить дифференциальную диагностику данного синдрома с другими наследственными дисплазиями соединительной ткани. В ряде случаев синдром Элерса-Данло имеет перекрестный фенотип с другими заболеваниям из этой группы, и дифференцировать их позволяет только молекулярно-генетическая диагностика.
Шкала Бейтона для оценки гипермобильности суставов
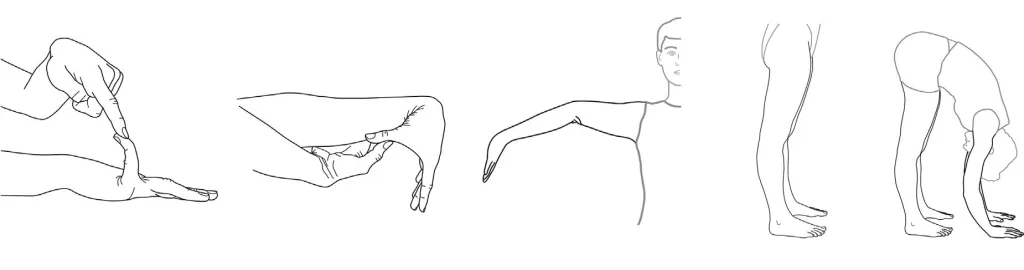
2. Пассивное прижатие большого пальца кисти к внутренней стороне предплечья (по
1 баллу справа и слева).
3. Переразгибание в локтевом суставе более 10° (по 1 баллу справа и слева).
4. Переразгибание в коленном суставе более 10° (по 1 баллу справа и слева)
5. Передний наклон туловища с касанием ладонями пола при прямых ногах (1 балл при
положительном результате)
Максимально возможное количество баллов — 9. Бейтон предложил считать гипермобильными лиц, у которых насчитывается 4 балла и более.

1) Malfait F, Francomano C, Byers P, et al. The 2017 international classification of the Ehlers-Danlos syndromes. Am J Med Genet C Semin Med Genet. 2017 Mar;175(1):8-26. PMID: 28306229
2) Zschocke J, Demirdas S, van Dijk FS. Genetic diagnosis of the Ehlers-Danlos syndromes. Med Genet. 2024 Dec 3;36(4):235-245. PMCID: PMC11610442
3) Николаева Е.А., Семячкина А.Н. Гено-фенотипическая характеристика синдрома Элерса-Данло, трудности идентификации типов заболевания и подходы к патогенетическому лечению. Российский вестник перинатологии и педиатрии. 2021;66(1):22-30. https://doi.org/10.21508/1027-4065-2021-66-1-22-30
4) Asta L, D'Angelo GA, Marinelli D, Benedetto U. Genetic Basis, New Diagnostic Approaches, and Updated Therapeutic Strategies of the Syndromic Aortic Diseases: Marfan, Loeys-Dietz, and Vascular Ehlers-Danlos Syndrome. Int J Environ Res Public Health. 2023 Aug 20;20(16):6615. doi: 10.3390/ijerph20166615
5) Tinkle B, Castori M, Berglund B, Cohen H, Grahame R, Kazkaz H, Levy H. Hypermobile Ehlers-Danlos syndrome (a.k.a. Ehlers-Danlos syndrome Type III and Ehlers-Danlos syndrome hypermobility type): Clinical description and natural history. Am J Med Genet C Semin Med Genet. 2017 Mar;175(1):48-69. PMID: 28145611
6) Forghani I, See J, McGonigle WC. Hypermobile Ehlers-Danlos Syndrome: Diagnostic Challenges and the Role of Genetic Testing. Genes (Basel). 2025 Apr 29;16(5):530. PMCID: PMC12111038
7) Doolan BJ, Lavallee M, Hausser I, Pope FM, Seneviratne SL, Winship IM, Burrows NP. Dermatologic manifestations and diagnostic assessments of the Ehlers-Danlos syndromes: A clinical review. J Am Acad Dermatol. 2023 Sep;89(3):551-559. PMID: 36764582
8) Malfait F. Vascular aspects of the Ehlers-Danlos Syndromes. Matrix Biol. 2018 Oct;71-72:380-395. doi: 10.1016/j.matbio.2018.04.013. PMID: 29709596
9) Ritelli M, Venturini M, Cinquina V, Chiarelli N, Colombi M. Multisystemic manifestations in a cohort of 75 classical Ehlers-Danlos syndrome patients: natural history and nosological perspectives. Orphanet J Rare Dis. 2020 Jul 31;15(1):197. PMCID: PMC7393722
10) Yew KS, Kamps-Schmitt KA, Borge R. Hypermobile Ehlers-Danlos Syndrome and Hypermobility Spectrum Disorders. Am Fam Physician. 2021 Apr 15;103(8):481-492. PMID: 33856167
11) В.В. Мордовцева, В.В. Гладько (2023). Синдром Черногубова-Элерса-Данлоса на стыке клинических специальностей. Вестник Медицинского института непрерывного образования, (1), 24-29.
12) Angwin C, Byers P, Dulfer E, Ghali N, Harris J, Hausser I, McElroy A, Sobey G, van Dijk FS. The Natural History of Dermatosparaxis Ehlers Danlos Syndrome: An Adult Case Series. Am J Med Genet A. 2025 Apr;197(4):e63957. PMID: 39641471
13) Malfait F, Syx D, Vlummens P, Symoens S, Nampoothiri S, Hermanns-Lê T, Van Laer L, De Paepe A. Musculocontractural Ehlers-Danlos Syndrome (former EDS type VIB) and adducted thumb clubfoot syndrome (ATCS) represent a single clinical entity caused by mutations in the dermatan-4-sulfotransferase 1 encoding CHST14 gene. Hum Mutat. 2010 Nov;31(11):1233-9. PMID: 20842734.
14) Caraffi SG, Maini I, Ivanovski I, et al. Severe Peripheral Joint Laxity is a Distinctive Clinical Feature of Spondylodysplastic-Ehlers-Danlos Syndrome (EDS)-B4GALT7 and Spondylodysplastic-EDS-B3GALT6. Genes (Basel). 2019 Oct 12;10(10):799. doi: 10.3390/genes10100799. PMCID: PMC6826576
15) Brady AF, Demirdas S, Fournel-Gigleux S, et al. The Ehlers-Danlos syndromes, rare types. Am J Med Genet C Semin Med Genet. 2017 Mar;175(1):70-115. PMID: 28306225
16) Hadar N, Porgador O, Cohen I. et al. Heterozygous THBS2 pathogenic variant causes Ehlers-Danlos syndrome with prominent vascular features in humans and mice. Eur J Hum Genet. 2024 May;32(5):550-557. PMCID: PMC11061164
17) McCarty RM, Saade D, Munot P et al. Clinical characterization of Collagen XII-related disease caused by biallelic COL12A1 variants. Ann Clin Transl Neurol. 2025 Mar;12(3):602-614. PMCID: PMC11920742
18) Punetha J, Kesari A, Hoffman EP, et al. Novel Col12A1 variant expands the clinical picture of congenital myopathies with extracellular matrix defects. Muscle Nerve. 2017 Feb;55(2):277-281. doi: 10.1002/mus.25232. Epub 2016 Nov 30. PMCID: PMC5236000
19) OMIM (Online Mendelian Inheritance in Man)