Синдром Марфана и марфаноподобные заболевания – это группа наследственных нарушений (дисплазий) соединительной ткани, характеризующаяся широким спектром сходных поражений соединительной ткани различных органов и систем. Ведущими проявлениями являются аневризма аорты, разнообразные скелетные аномалии и эктопия хрусталика. Марфаноподобные заболевания включают более 30 наследственных моногенных синдромов, имеющих один или более признаков, используемых как диагностический критерий синдрома Марфана. Среди прочих, к марфаноподобным заболеваниям относят синдром эктопии хрусталика, гомоцистинурию I типа, врожденную контрактурную арахнодактилию, синдром артериальной извитости.
Синдром Марфана
Синдром Марфана (СМ) – это одно из наиболее распространенных заболеваний из группы наследственных дисплазий соединительной ткани, которое встречается с частотой 1:3000 – 1:6000. Заболевание характеризуется широким спектром поражения соединительной ткани различных органов и систем. Ведущими проявлениями являются расширение аорты, расслоение аорты, эктопия хрусталика и разнообразные скелетные аномалии, вызванные чрезмерным ростом длинных костей. В 95% случаев синдром Марфана вызывается наличием патогенных или условно патогенных вариантов в гене FBN1, кодирующем фибриллин 1-го типа, основной структурный компонент внеклеточного матрикса (особенно в артериях и структурах глаза). Тип наследования – аутосомно-доминантный с высокой пенетрантностью и вариабельной экспрессивностью. Мужчины и женщины поражаются с одинаковой частотой. До 25% пациентов с синдромом Марфана имеют патогенные варианты de novo в гене FBN1. Уже в период новорожденности выявляются арахнодактилия («паучьи пальцы»), долихостеномелия (длинные тонкие конечности) и тенденция к увеличению длины тела. В дальнейшем больных отличает долихоцефалическая (удлиненная и узкая) форма черепа, узкое лицо, аркообразное нёбо, гипоплазия мышц и подкожной клетчатки, тенденция к гиперрастяжимости кожи, моторная неловкость движений. Характерны деформации грудной клетки (килевидная, воронкообразная), аномалии позвоночника (сколиоз, кифоз, ювенильный остеохондроз, нестабильность шейного отдела позвоночника), вывихи голеностопных суставов и плоскостопие. Практически у всех больных наблюдается поражение крупных сосудов и сердца. Особое диагностическое значение имеет расширение или аневризма аорты. Типичны патология органов зрения: миопия высокой степени, подвывих, сферичность, уменьшение размеров хрусталика, отслойка сетчатки. Нередко выявляются бедренные или паховые грыжи, варикозное расширение вен нижних конечностей, висцероптоз, эмфизема легких. Диагностика синдрома Марфана основывается на пересмотренных Гентских критериях (Loeys A. et al., 2010). Данные критерии предполагают определение патогенных вариантов в гене FBN1.
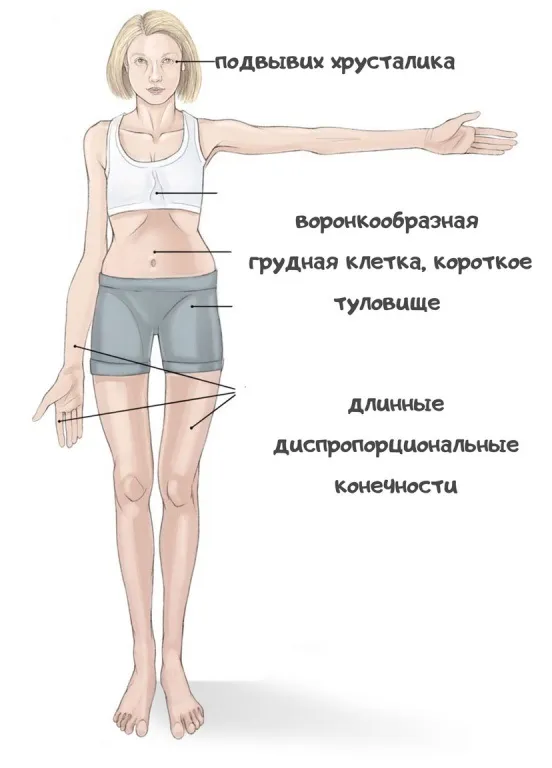
Рис 1. Синдром Марфана. Наиболее частые фенотипические признаки.
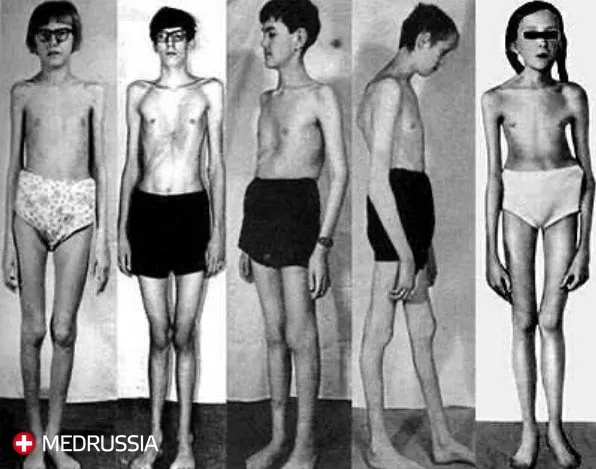
Рис 2. Скелетные аномалии при синдроме Марфана: высокий рост, длинные диспропорциональные конечности, короткое туловище, воронкообразная грудная клетка, сколиоз, кифоз.
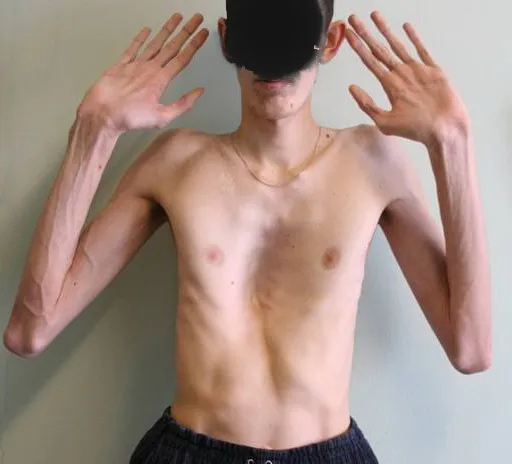
Рис. 3. Синдром Марфана у мужчины 17 лет. Отмечается воронкообразная деформация грудной клетки 3 степени асимметричной формы, арахнодактилия.
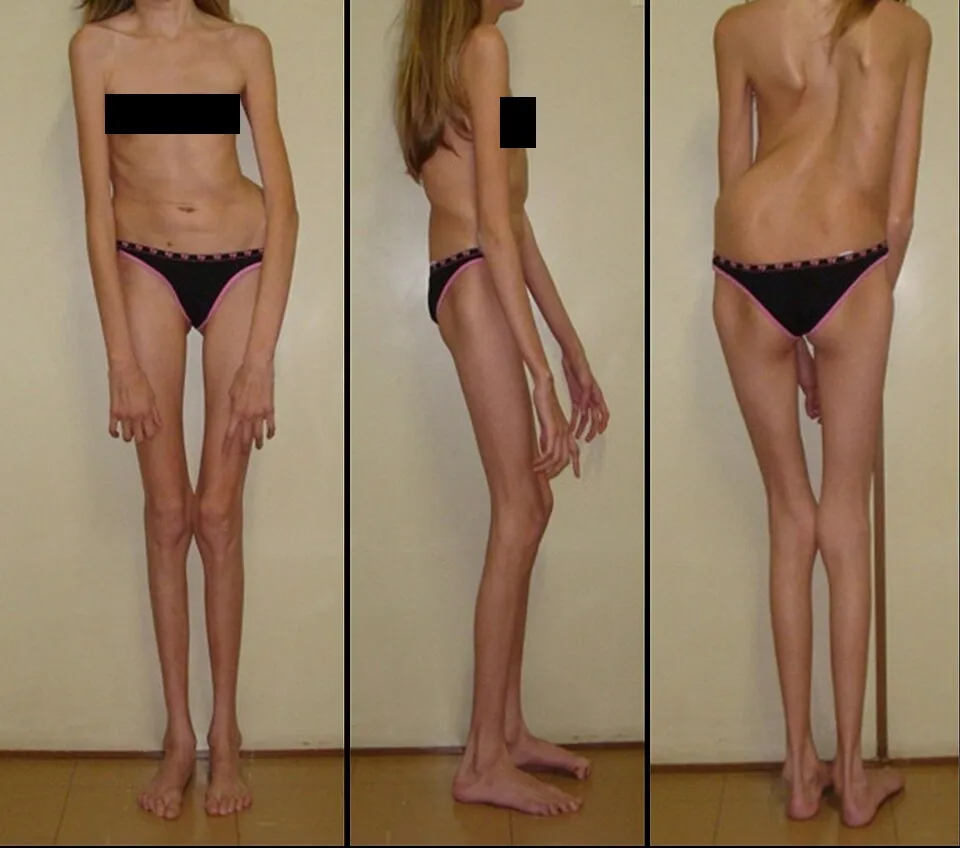
Рис. 4. Скелетные аномалии при синдроме Марфана: высокий рост, длинные диспропорциональные конечности, короткое туловище, сколиоз.
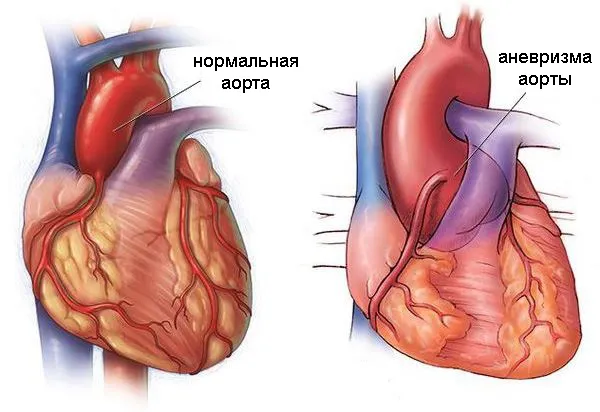
Рис. 5. Аневризма восходящей дуги аорты (справа)
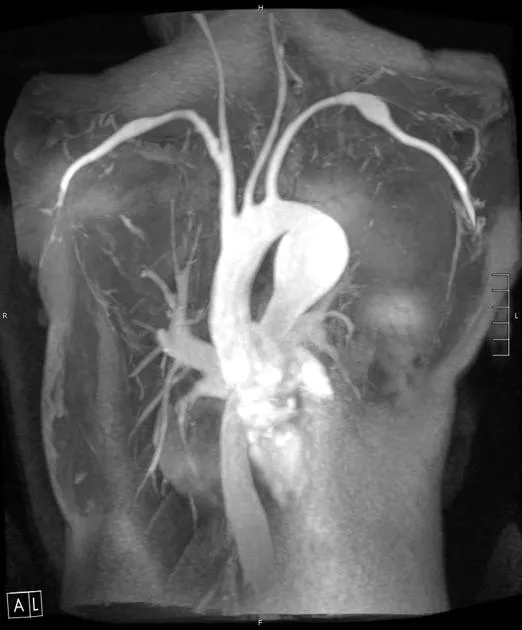
Рис. 6. Аневризма нисходящей грудной аорты диаметром 45 мм и длиной 50 мм у пациента с синдромом Марфана. Обе подключичные артерии также расширены (левая > правой).
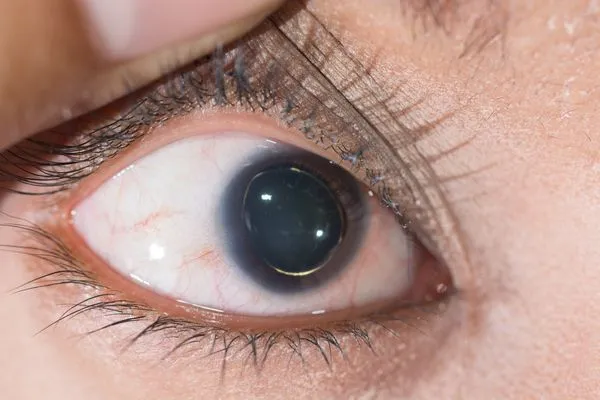
Рис 7. Вывих хрусталика при синдроме Марфана.
В рамках персмотренных Гентских критериев требования к диагностике синдрома Марфана различаются в зависимости от данных наследственного анамнеза.
Если семейный или наследственный анамнез не отягощен, диагноз синдрома Марфана устанавливается в следующих случаях:
- при наличии подтверждённого расширения корня аорты и эктопии хрусталика;
- при наличии расширения корня аорты и подтверждённых патогенных или условно патогенных вариантов в гене FBN1;
- при наличии эктопии хрусталика без вовлечения корня аорты с подтверждением патогенных или условно патогенных вариантов в гене FBN1;
- при сочетании расширения аорты и признаков системного вовлечения соединительной ткани ≥7 баллов (см. таблицу).
В случае отягощенного по синдрому Марфана семейного анамнеза этот диагноз может быть установлен, по следующим критериям:
-
семейный анамнез синдрома Марфана и эктопия хрусталика;
-
семейный анамнез синдрома Марфана и ≥7 баллов при оценке признаков системного вовлечения соединительной ткани;
-
семейный анамнез синдрома Марфана и расширение корня аорты.
Таблица 1. Оценка признаков системного вовлечения соединительной ткани в баллах
|
Признаки системного вовлечения соединительной ткани |
Баллы |
|---|---|
|
Симптом запястья и большого пальца |
3 |
|
Симптом запястья или большого пальца |
1 |
|
Килевидная деформация грудной клетки |
2 |
|
Воронкообразная деформация грудной клетки или асимметрия грудной клетки |
1 |
|
Вальгусная деформация стопы |
2 |
|
Плоскостопие |
1 |
|
Пневмоторакс |
2 |
|
Эктазия твердой мозговой оболочки |
2 |
|
Протрузия тазобедренного сустава |
2 |
|
Уменьшенное соотношение верхнего сегмента к нижнему + увеличенное отношение размаха рук к росту + нетяжелая степень сколиоза |
1 |
|
Сколиоз или торако-люмбальный кифоз |
1 |
|
Недоразгибание локтевого сустава |
1 |
|
Лицевые признаки (от 3/5), долихоцефалия, энофтальм, скошенные вниз глазные щели, гипоплазия скуловых костей |
1 |
|
Кожные стрии |
1 |
|
Миопия больше 3 диоптрий |
1 |
|
Пролапс митрального клапана (любой вид) |
1 |
Максимальное общее количество баллов = 20; количество баллов ≥7 – свидетельствует о системной вовлеченности в процесс соединительной ткани.
Оценку размеров аорты следует проводить при трансторакальной ЭхоКГ. При этом следует оценивать размеры аорты не только на уровне синусов Вальсальвы, но также определять размеры восходящего отдела аорты (что необходимо для проведения дифференциального диагноза). Особенно важно подчеркнуть, что нельзя пользоваться абсолютными значениями диаметра аорты, но следует проводить расчет Z-критерия, позволяющего учесть возраст и росто-весовые данные пациента. Методику расчета Z-критерия можно найти в специализированной литературе.
Аллельные варианты гена FBN1 могут вызывать MASS-синдром, неонатальный синдром Марфана, изолированную аутосомно-доминантную эктопию хрусталика, синдром марфаноидной прогероидной липодистрофии, акромикрическую дисплазию, гелеофизическую дисплазию 2 типа, синдром жесткой кожи (stiff skin syndrome), синдром Уэйла-Маркезани 2 типа.
MASS-синдром
MASS-синдром (MASS-фенотип, марфаноподобный синдром) – акроним, означающий раннюю близорукость/пролапс митрального клапана (Myopia/Mitral valve prolapse), дилатацию аорты (Aotic dilatation), изменения кожи (Skin) и костей скелета (Skeleton). Накопленные за последние десятилетия данные свидетельствуют о высокой вариативности признаков, сопутствующих MASS–фенотипу, который крайне трудно отличить от синдрома Марфана с неполным набором признаков. Именно поэтому критерии диагностики MASS–фенотипа согласно пересмотренным Гентским критериям существенно упрощены. Согласно этим рекомендациям MASS-фенотип может быть диагностирован у лиц старше 20 лет при пограничном расширении корня аорты (Z около 2.0, но не более), наличии хотя бы одного скелетного признака и признаков системного вовлечения соединительной ткани на 5 баллов и более. Так как расширение аорты может развиться и прогрессировать с возрастом, очевидна целесообразность динамического наблюдения за пациентами с MASS-синдромом для своевременного выявления аневризмы аорты.
Неонатальный синдром Марфана
Неонатальный синдром Марфана — это редкий и чрезвычайно тяжелый вариант заболевания, составляющий не более 14% от общего числа случаев, со средней продолжительностью жизни около 4 лет. Как и при классическом варианте, у большинства пациентов с неонатальной формой синдрома Марфана патогенные варианты выявляются в гене фибриллина FBN1. Ранняя неонатальная смертность при данной форме синдрома Марфана, в основном, связана с осложнениями со стороны сердечно-сосудистой системы (аневризма и расслоение аорты, тяжелая митральная недостаточность) и дыхательной системы (врожденная эмфизема, дыхательная недостаточность, ночные апноэ). Наиболее грозным симптомом неонатальной формы синдрома Марфана является тяжелая митральная недостаточность. Она выявляется у 82% детей, которым диагноз синдрома Марфана был поставлен в первые 3 месяца жизни, и часто приводит к развитию сердечной недостаточности и летальному исходу. К другим признакам неонатального синдрома Марфана относятся аномальный прогероидный (напоминающий преждевременное старение) и кахексический фенотип, выраженная арахнодактилия, долихоцефалия, дряблая кожа, сморщенные уши, «готическое» небо, микрогнатия или гипоплазия нижней челюсти, камптодактилия (постоянно согнутые пальцы), сгибательные контрактуры, деформации передней части грудной клетки, гипоплазия мышц, мегалокорнеа (увеличенная роговица) и эктопия хрусталика. Для диагностики неонатального синдрома Марфана предлагается использовать два клинических признака, которые редко встречаются при классическом синдроме Марфана, но часто встречаются при неонатальном синдроме Марфана: врожденную эмфизему и митральную и/или трикуспидальную регургитацию.
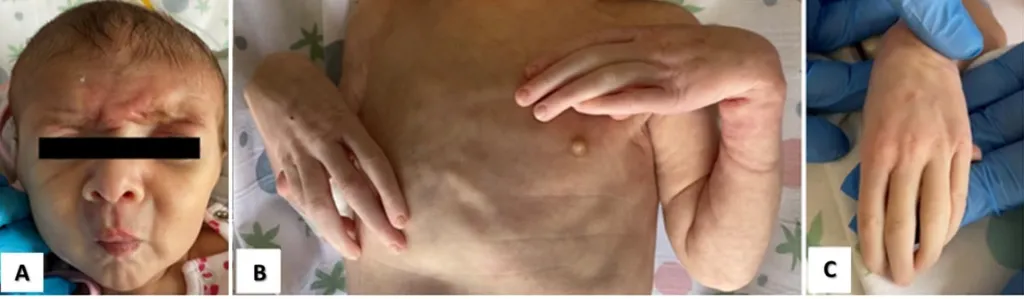
Рис. 8. Неонатальный синдром Марфана: А) «старческие» черты лица; Б) дистальный артрогрипоз рук; В) выраженная арахнодактилия кистей рук и положительный симптом Штейнберга (симптом большого пальца) левой руки [6].
Синдром марфано-прогероидной липодистрофии
Синдром марфано-прогероидной липодистрофии характеризуется врожденной липодистрофией, прогероидным обликом с характерными чертами лица, включая экзофтальм, косо нисходящие глазные щели, широкий, выступающий лоб (краниосиностоз), гипоплазию средней и нижней трети лица, клювовидный нос, ретрогнатию. Характерна тонкая, гиперпигментированная, морщинистая кожа. Отличительной особенностью являются частичные проявления синдрома Марфана, такие как ускоренный рост (при тяжелом дефиците веса), арахнодактилия, гипермобильность суставов пальцев, расширение корня аорты, пролапс митрального клапана, врожденный вывих хрусталика, близорукость, деформация грудной клетки, диафрагмальные и паховые грыжи, эктазия твердой мозговой оболочки и нормальное психомоторное развитие. Синдром марфано-прогероидной липодистрофии обычно вызывается патогенными вариантами со сдвигом рамки считывания (frameshift) в 64-м или 65-м экзонах гена FBN1.
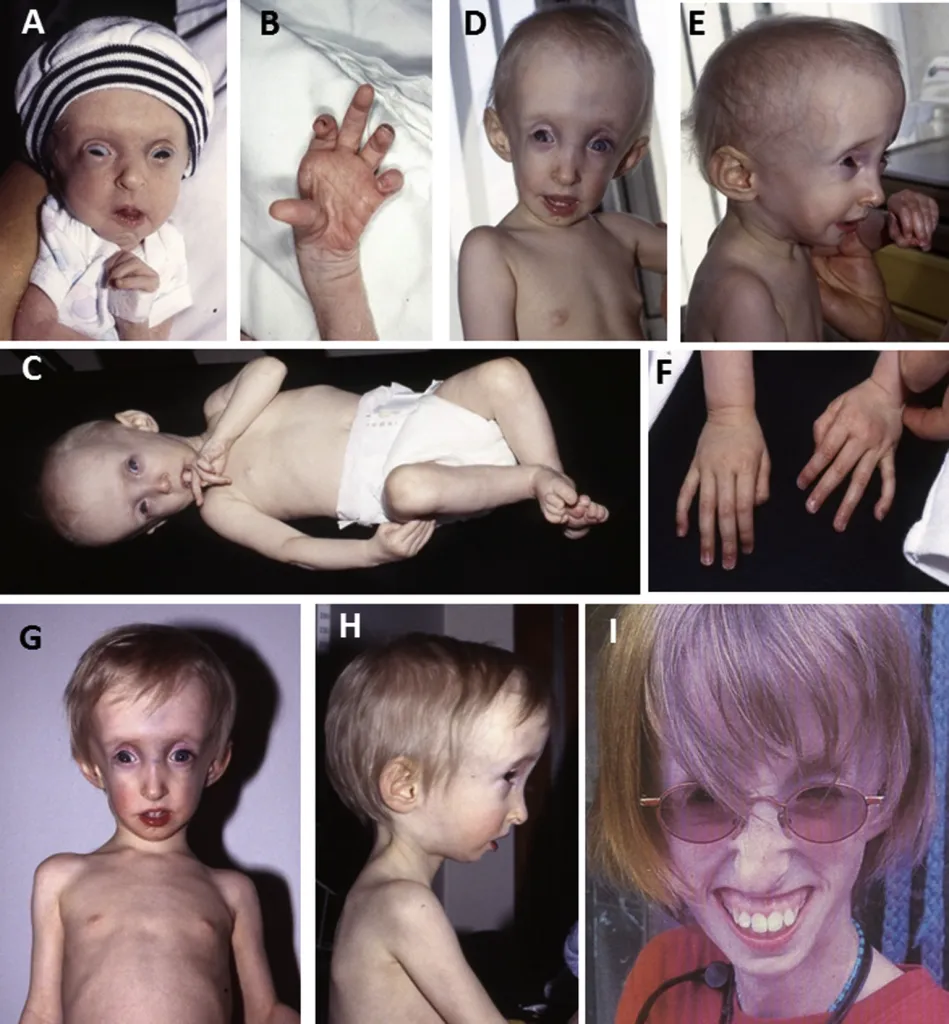
Рис. 9. Неонатальный прогероидный вариант синдрома Марфана с врожденной липодистрофией. Клинические особенности пациентки при рождении (A-B), в 6 месяцев (C), 8 месяцев (D-F), 21 месяц (G-H) и в 16 лет (I). Обращает на себя внимание относительная макроцефалия, гипоплазия лицевых костей, косо расположенные глазные щели, энтропион верхних век (A), выраженная гипермобильность пальцев (B), длинные узкие кисти (F), глубоко посаженные глаза, дефицит подкожной жировой ткани (C, G) [7].
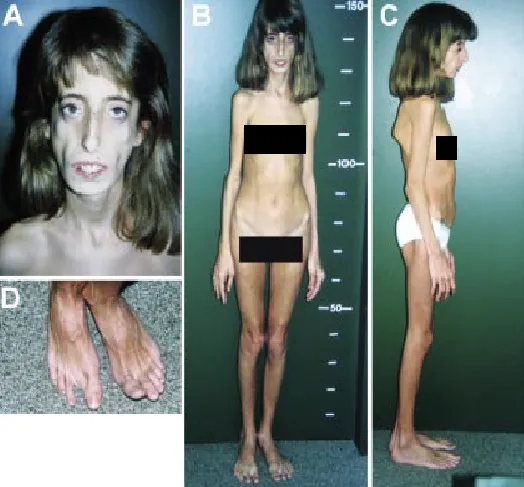
Рис. 10. Пациентка в возрасте 10 лет с синдромом Марфана и неонатальной прогероидной липодистрофией. Отмечается выраженное генерализованное отсутствие подкожной жировой ткани [8].
Синдром эктопии хрусталика
Синдром эктопии хрусталика (изолированная аутосомно-рецессивная эктопия хрусталика) ─ это наследственное заболевание соединительной ткани, которое вызывается патогенными вариантами в гене ADAMTSL4 и имеет некоторые черты синдрома Марфана, в частности, вывих хрусталика глаза, способный вызвать серьезные проблемы со зрением. У пациентов с синдромом эктопии хрусталика не наблюдается патологии сердца и сосудов, характерных для синдрома Марфана. Помимо эктопии хрусталика (встречается в 100% случаев) у больных с данным синдромом может выявляться следующая глазная патология:
-
эктопия зрачка (19%): зрачок расположен не по центру, а смещен в сторону;
-
трансиллюминация радужки (14%): истончение радужки, из-за чего она «просвечивает» при осмотре лампой;
-
иридодонез (13%): дрожание радужки при движении глаза из-за отсутствия опоры (смещенние хрусталика);
-
персистирующая зрачковая мембрана (13%): представляет собой остатки ткани, которая должна была исчезнуть еще до рождения; выглядит как нити в области зрачка;
-
ранняя катаракта (13%): помутнение хрусталика в молодом возрасте;
-
ригидный зрачок: зрачок плохо расширяется даже при использовании мидриатиков;
-
сферофакия: хрусталик имеет форму шара, а не линзы; он меньше в диаметре, но более выпуклый, что вызывает сильную близорукость;
-
коректопия: смещение зрачка от центральной оси, часто сочетается со смещением хрусталика в противоположную сторону;
-
колобома радужки/хрусталика: это врожденный дефект, характеризующийся отсутствием части ткани; проявляется грушевидным или щелевидным зрачком, часто сопровождается светобоязнью;
-
задние синехии: спайки (прирастание) радужки к передней поверхности хрусталика.
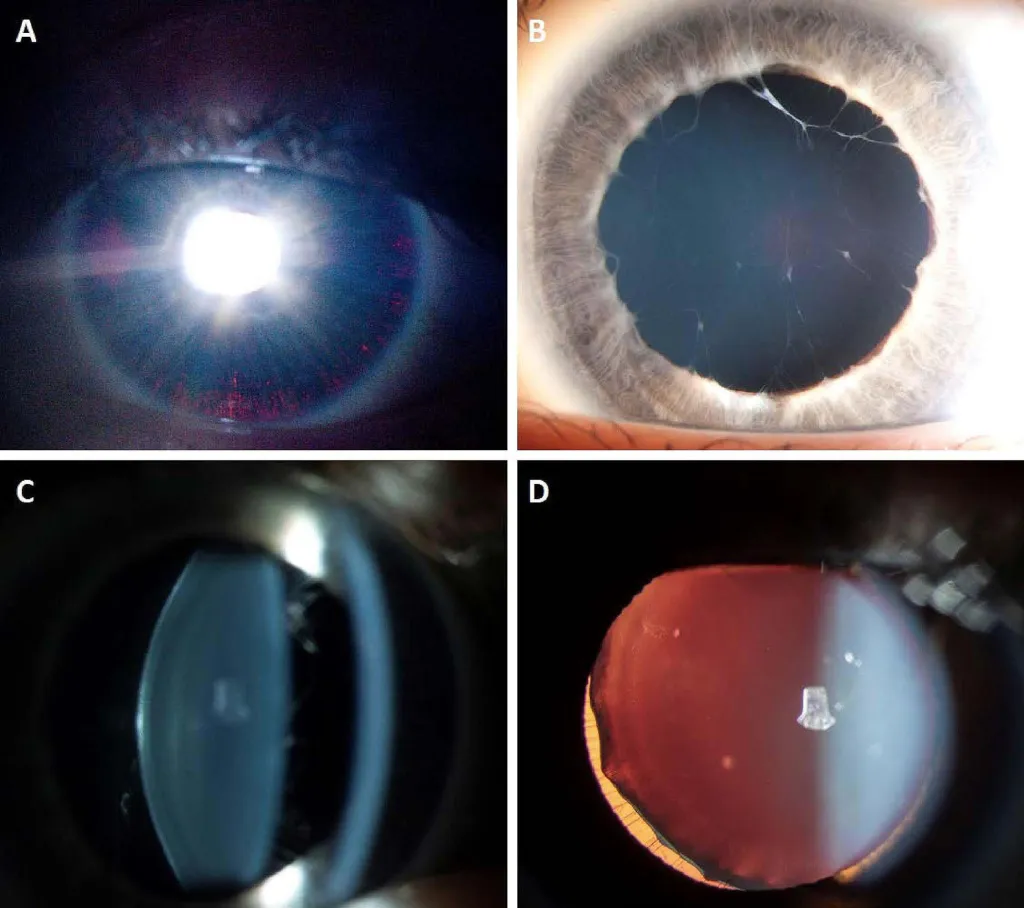
Рис. 11. Синдром эктопии хрусталика и сопутствующая глазная патология у пациентов с патогенными вариантами в гене ADAMTSL4. A: трансиллюминация радужной оболочки. B: персистирующая зрачковая мембрана. C: задняя чечевицеобразная деформация или сферофакия. D: эктопия хрусталика [10].
Гомоцистинурия I типа
Гомоцистинурия I типа (классическая гомоцистинурия, ГЦУ) ─ это редкое моногенное аутосомно-рецессивное заболевание из группы аминоацидопатий, связанное с нарушением преобразования метионина в цистеин вследствие дефицита печеночного фермента цистатион-β-синтетазы, вызванного наличием патогенных вариантов в гене CBS. Заболевание характеризуется повышенной концентрацией метионина в сыворотке крови и гомоцистеина в сыворотке крови и моче, снижением цистеина в сыворотке крови и моче. Повышение концентрации гомоцистеина приводит к нарушению сшивания сульфгидрильных групп в белках, таких как эластин, что объясняет развитие дисплазии соединительной ткани. Средняя частота классической ГЦУ по данным литературы составляет в среднем 1:100000-1:200000, варьируя от 1:1800 до 1:900000 в зависимости от этнической принадлежности. Тип наследования аутосомно-рецессивный.
Поражение органа зрения. Типичным симптомом классической ГЦУ, который часто появляется на втором году жизни является миопия, которая предшествует развитию дислокации или эктопии хрусталика. При заболевании происходит деструкция богатых фибриллином микрофибрилл цилиарной связки и нарушением ее структуры и функции. Степень смещения хрусталика варьирует от незаметного подвывиха до полного вывиха. Наиболее часто у пациентов с ГЦУ встречается подвывих хрусталика (ectopia lentis). Подвывих хрусталика может быть первым признаком болезни, описан случай манифестации в возрасте 4 недель у одного пациента. Сроки появления этого признака широко варьируют, но примерно на 2-м году жизни отмечают появление подвывиха хрусталика у многих пациентов, у более чем 50% нелеченых пациентов он обычно проявляется к возрасту 8 лет. Миопия, связанная с ослаблением хрусталика, приводит к пассивной сферической деформации (сферофакии). Частым осложнением эктопии хрусталика является острая глаукома, обусловленная смещением хрусталика в переднюю камеру глаза.
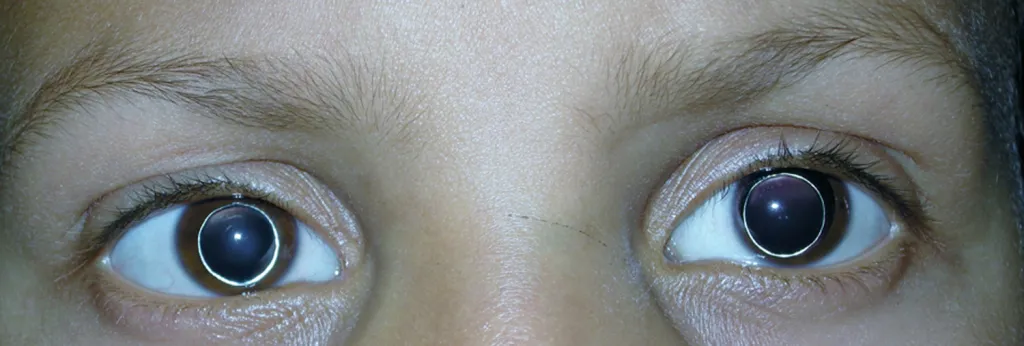
Рис.12. Двусторонняя эктопия хрусталика при гомоцистинурии I типа
Тромбозы. Вторым по частоте при классической форме ГЦУ является поражение сосудов, тромбозы и тромбоэмболические осложнения. Накопление гомоцистеина приводит к активации фактора Хагемана, способствуя процессу тромбообразования. Венозные тромбозы встречаются чаще, чем артериальные, и могут возникать в любом органе и системе, включая сосуды головного мозга, коронарные и легочные артерии. Тромбозы возникают преимущественно у пациентов подросткового и молодого возраста, являются главной причиной инфаркта миокарда или инсульта с формированием очаговой неврологической симптоматики. Почти у 50 % пациентов тромбозы отмечаются к возрасту 29 лет. В ряде случаев поражение сосудов может являться единственным симптомом заболевания, возникающим на 2-3 десятилетии жизни.
Поражения костной системы. Характерен марфано-подобный фенотип, представленный высоким ростом, долихостеномелией, арахнодактилией, сколиозом, деформацией грудной клетки по типу килевидной или воронкообразной, вальгусной деформацией конечностей, высоким сводом твердого неба, полой стопой, остеопорозом/остеопенией. Остеопороз наблюдается почти у половины пациентов ко второму десятилетию жизни.
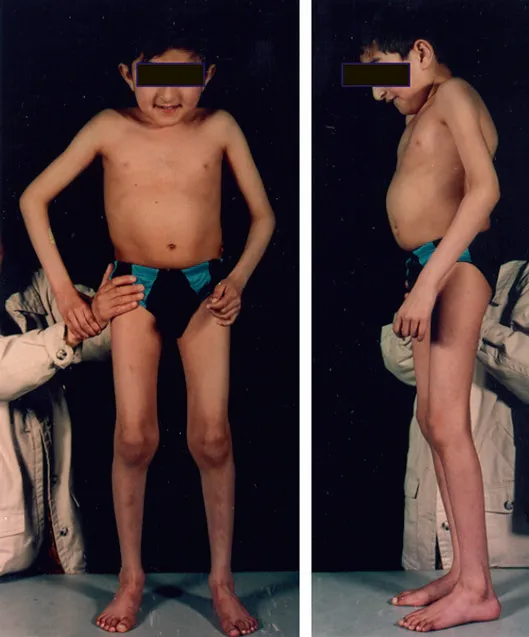
Рис. 13. Марфаноподобный фенотип у пациента с гомоцистинурией I типа [13].
Неврологические и психиатрические проявления. Наиболее частым клиническим проявлением поражения ЦНС является задержка психоречевого развития, умственная отсталость. Достаточно часто когнитивные нарушения могут являться первым симптомом заболевания. Интеллектуальные способности пациентов могут достаточно сильно различаться в зависимости от возраста начала терапии. На втором десятилетии жизни у пациентов часто возникают эпизоды депрессии, тревожность, обсессивно-компульсивные расстройства, психозы. Характерными для классической ГЦУ являются различные нарушения поведения. У отдельных пациентов психиатрические нарушения могут являться единственным симптомом заболевания. В 21% случаев у нелеченых пациентов с классической ГЦУ наблюдаются эпилептические приступы в раннем младенческом возрасте, наиболее часто ─ генерализованные тонико-клонические судороги. Другими неврологическими нарушениями являются различные экстрапирамидные нарушения, в частности, дистония и тремор. Очаговые неврологические нарушения соответствуют зоне поражения во время перенесенного острого нарушения мозгового кровообращения.
Другие проявления классической гомоцистинурии. Описаны случаи классической ГЦУ, протекающей с острым панкреатитом и хронической диареей, гипопигментацией кожи и волос. Могут быть грыжи передней брюшной стенки.
Классическая гомоцистинурия подразделяется на B6-чувствительную и B6-резистентную формы, для их диагностики проводится тест с пиридоксином (см. клинические рекомендации). Терапевтическая тактика различается для этих форм.
Синдром Билса (врожденная контрактурная арахнодактилия)
Синдром Билса (врожденная контрактурная арахнодактилия, Beals-Hecht syndrome) — это редкая моногенная аутосомно-доминантная наследственная дисплазия соединительной ткани из группы фибриллинопатий, обусловленное наличием патогенных вариантов в гене FBN2, кодирующем фибриллин 2. Частота синдрома Билса в популяции не установлена. Опубликован обзор литературы, в котором сообщается о 40 семейных случаях, насчитывающих 120 больных. Отмечается большое фенотипическое сходство данного заболевания с синдромом Марфана. Клиническая симптоматика синдрома Билса характеризуется высоким ростом больного, арахнодактилией кистей и стоп, контрактурами крупных и мелких суставов и измененной формой ушных раковин («мятое» ухо). Все перечисленные признаки формируются пренатально. Нередко контрактуры суставов с возрастом имеют тенденцию к обратному развитию. Наряду с перечисленными симптомами, примерно 15–20% больных, по данным литературы, имеют такие типичные для синдрома Марфана признаки, как аневризма аорты, подвывих хрусталиков, миопия различной степени выраженности. Встречаются также врожденные пороки сердца.
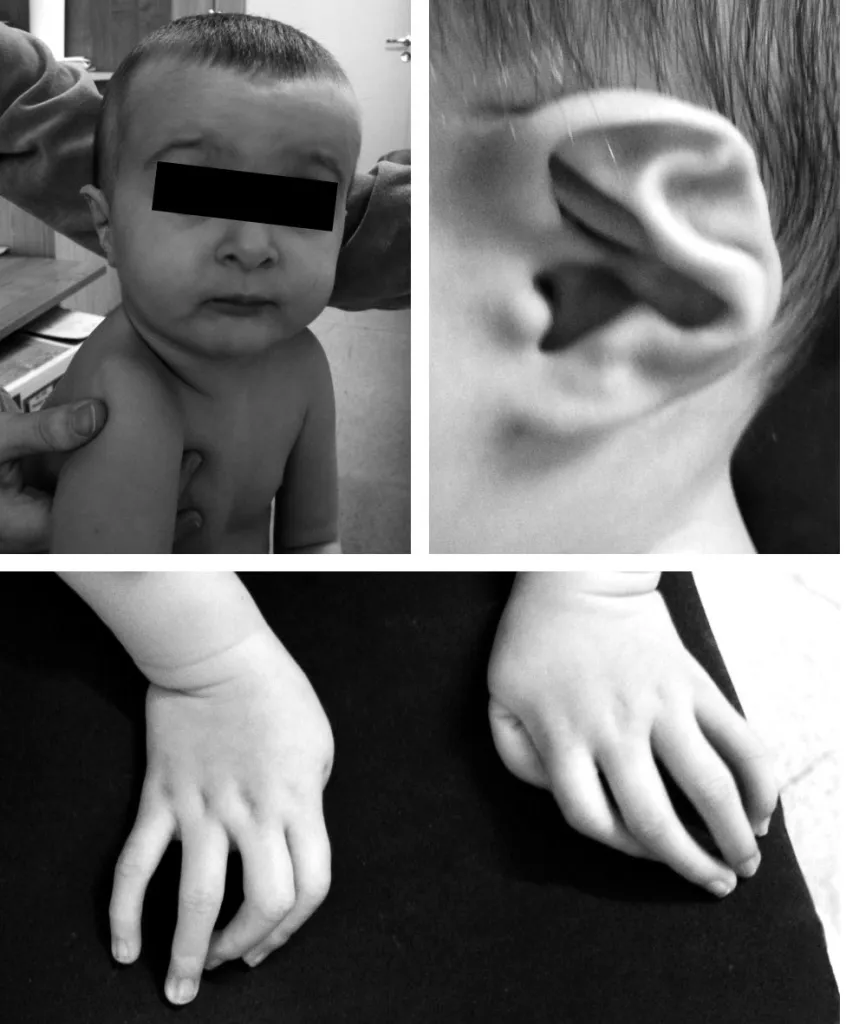
Рис. 14. Фенотип ребенка с синдромом Билса в возрасте один год: астеническое телосложение, узкий лицевой скелет, арахнодактилия, врожденные контрактуры мелких суставов, воронкообразная деформация грудной клетки, «мятое» ухо [14].
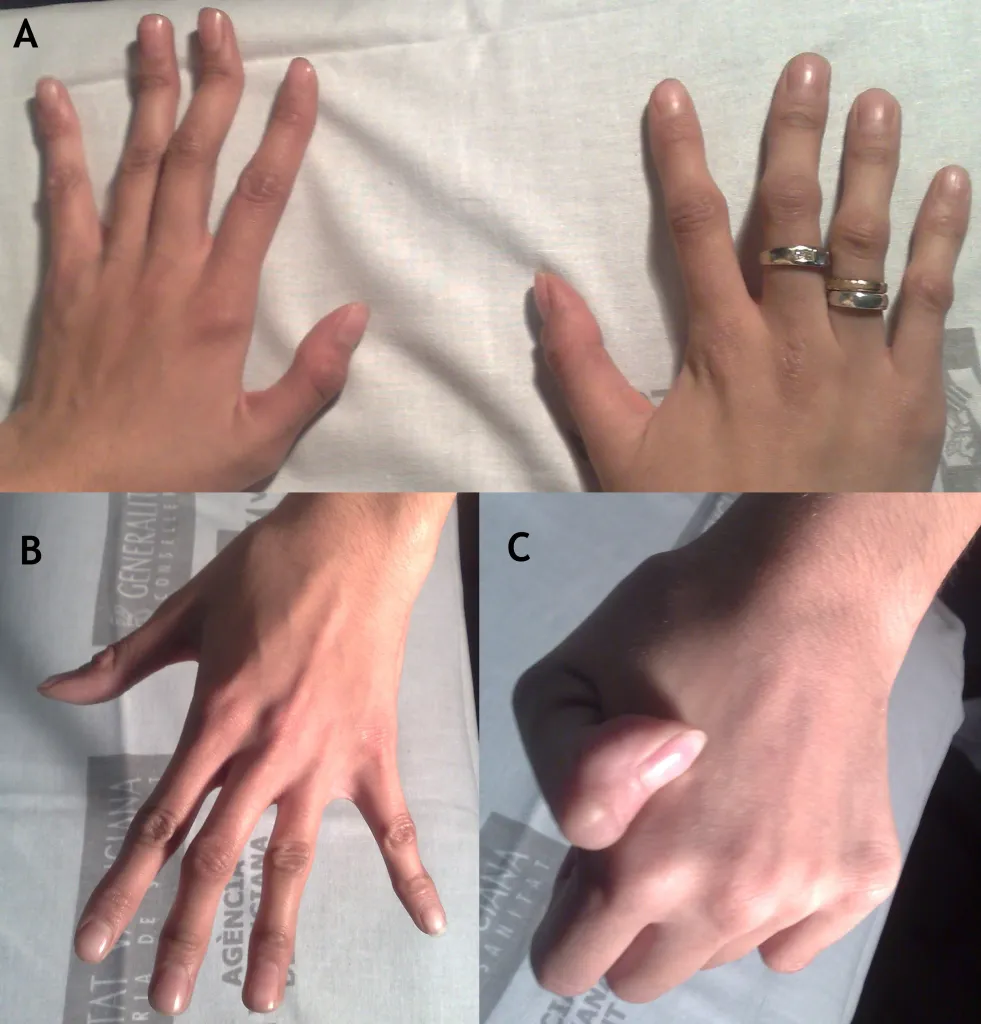
Рис. 15. Синдром Билса у пациентки 26 лет. (A, B) Типичная контрактурная арахнодактилия (C) гипермобильность суставов.
Наследственный синдром артериальной извитости
Наследственный синдром артериальной извитости (синдром извилистых артерий) ─ это редкое моногенное аутосомно-рецессивное заболевание соединительной ткани из группы марфаноподобных заболеваний, вызванное наличием патогенных вариантов в гене SLC2A10, кодирующем транспортер глюкозы GLUT10. Синдром встречается очень редко (<1:1 000 000). Фенотипические проявления характеризуются продолговатым лицом, микрогнатией, крючковатым носом, гипермобильностью суставов, повышенной растяжимостью кожи, арахнодактилией, воронкообразной или килевидной формой грудной клетки, грыжами и другими признаками соединительнотканной дисплазии. Может определяться фенотипическое сходство с синдромом Марфана, Элерса-Данло, Луиса-Дитца, эластолизисом (cutis laxa).
Главным проявлением синдрома артериальной извитости является извитость крупных и средних артериальных сосудов, которая приводит к образованию стенозов и аневризм соответствующих сосудистых бассейнов. Наиболее типична (более 90 %) комбинация в виде удлинения дуги аорты и извитости брахиоцефальных артерий. Извилистая аорта может привести к образованию гигантской аневризмы. Множественные аневризмы мозговых сосудов приводят к синкопальным состояниям и церебральной дисфункции, ишемическим инсультам. Часто (у 60% пациентов) определяются множественные стенозы легочной артерии. У детей с извилистой легочной артерией наблюдается тяжёлая лёгочная гипертензия, часто наблюдается значительная обструкция выходного тракта правого желудочка и дисфункция ЛЖ. Во всех случаях синдрома извилистых артерий наблюдается гипертрофия миокарда желудочков, она может быть связана с удлиненными также извилистыми коронарными артериями. При наличии сужения коронарных артерий может возникнуть картина ишемии миокарда.
Таблица 2. Основные симптомы синдрома извилистых артерий.
|
Орган или система |
Проявления |
|---|---|
|
Лицо |
Продолговатое лицо, длинный фильтр, микрогнатия |
|
Глаза |
Косо нисходящие глазные щели, блефарофимоз, гипертелоризм, кератоконус (редко) |
|
Нос |
Крючковатый нос |
|
Рот |
Высокое небо |
|
Сердце |
Гипертрофия желудочков |
|
Сосуды |
Артериальная извилистость (большие и средние артерии, в том числе аорта), удлинение артерий (больших и средних артерий, в том числе аорты), аневризмы артериальных сосудов, стеноз аорты, стеноз легочной артерии, фрагментация внутренней эластической мембраны артериальных сосудов, разрывы эластических волокон артериальных сосудов, повышенный риск тромбоза, гипертония. |
|
Грудная клетка |
Воронкообразная грудная клетка, килевидная грудная клетка |
|
Диафрагма |
Диафрагмальная грыжа, грыжа пищеводного отверстия диафрагмы, скользящая грыжа, грыжа желудка
|
|
Живот |
Паховая грыжа, пупочная грыжа |
|
ЖКТ |
Дивертикулит, грыжа пищеводного отверстия диафрагмы, некроз кишечника в связи с тромбозом |
|
Суставы |
Гиперподвижность суставов, контрактуры суставов |
|
Конечности |
Арахнодактилия |
|
Кожа |
Перерастяжимость кожи, мягкая рыхлая кожа |
|
ЦНС |
Ишемический инсульт, умственная отсталость (редко), гипотония (редко) |
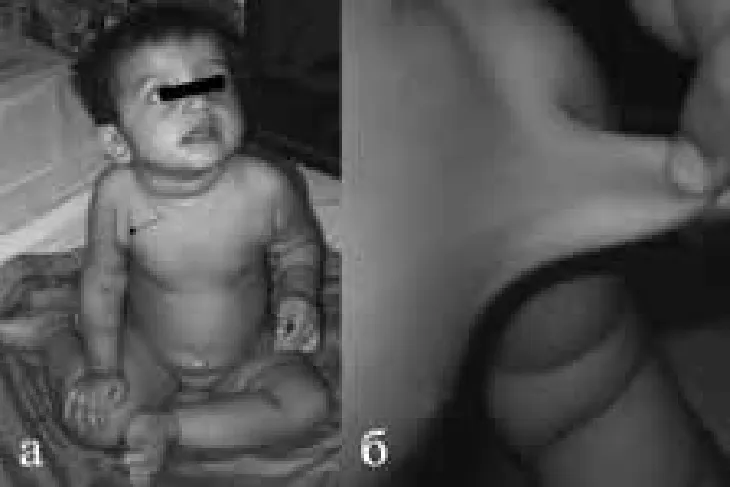
Рис. 16. Девочка в возрасте одного года с синдромом извилистых артерий. а — внешний вид; б — повышенная растяжимость кожи.
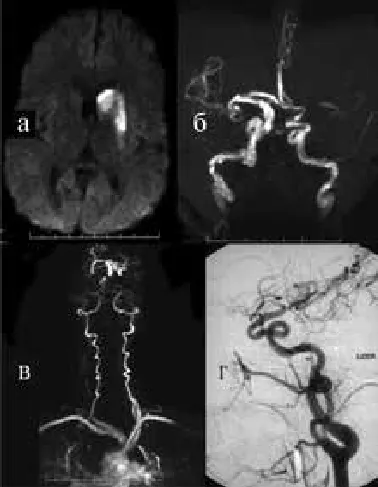
Рис.17. Результаты обследования ребенка с синдромом извилистых артерий. (а) По данным КТ определяется острый левосторонний подкорковый ишемический инсульт. (б) На МРТ виллизиева круга определяется окклюзия левой средней мозговой артерии и извитость внутренней сонной артерии. (в) На МРТ шеи видна выраженная извитость позвоночных артерий. (г) Ангиография подтверждает извитость левой внутренней сонной артерии.
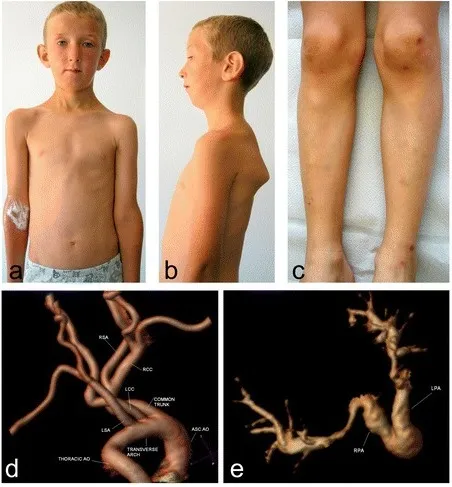
Рис. 18. Наследственный синдром артериальной извитости. У пациента отмечается легкая скафоцефалия, гипотелоризм, большие уши, удлиненное лицо, микроретрогнатия, крыловидные лопатки, сколиоз (a,b), вальгусная деформация коленных суставов, легкое образование синяков, небольшой атрофический рубец над левым коленом (c), извилистость дуги аорты и брахиоцефальных сосудов (d), выраженная извилистость внутрипаренхимальных артерий (e) [17].
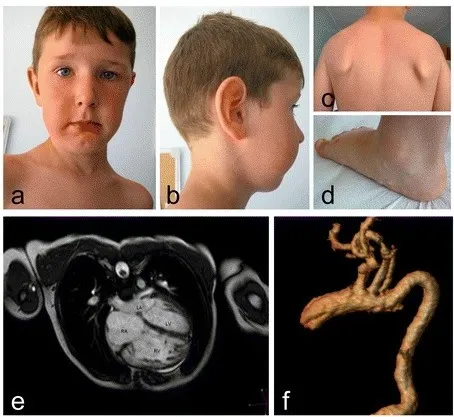
Рис. 19. Наследственный синдром артериальной извитости. У пациента отмечается легкая скафоцефалия, эпикантус, гипотелоризм, большие уши, удлиненное лицо, микроретрогнатия (a,b), крыловидные лопатки, сколиоз (c), плоскостопие, пьезогенные папулы (d), гипертрофия правого желудочка с компрессией левого желудочка (e), выраженная извилистость внутрипаренхимальных артерий (f) [17].
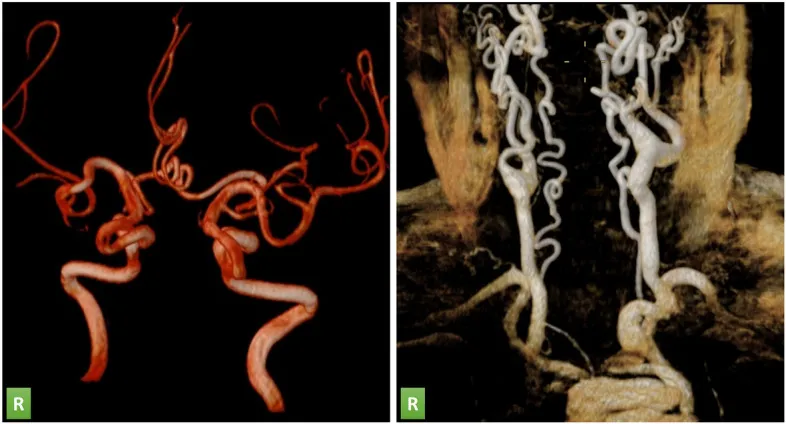
Рис. 20. Наследственный синдром артериальной извитости. Трехмерная реконструкция внутричерепных (слева) и надаортальных (справа) сосудов по данным МРТ-ангиографии пациента с аортальным стенозом. Отмечается выраженная извилистость сосудов при отсутствии расслоения, аневризматических поражений или гемодинамически значимых стенозов [18].
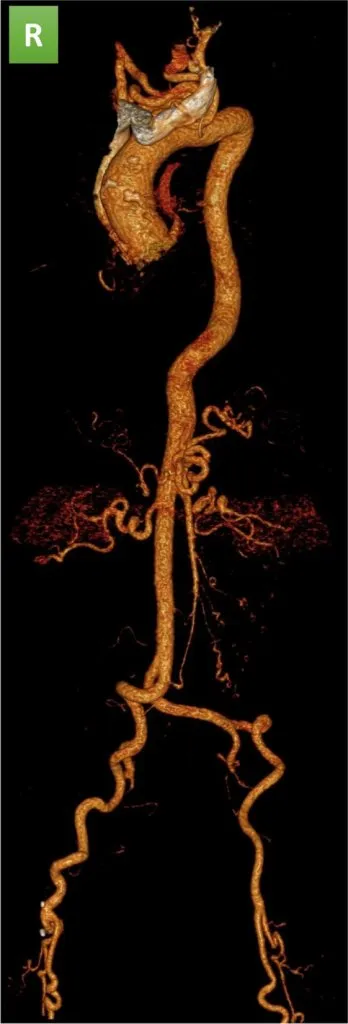
Рис. 21. Наследственный синдром артериальной извитости. Трехмерная реконструкция ангио-КТ грудной и брюшной аорты пациента с аортальным стенозом, демонстрирующая извилистость грудных и брюшных сосудов без стенозов [18].
Важно понимать, что синдром извилистых артерий встречается также и при других наследственных дисплазиях соединительной ткани, помимо наследственного синдрома артериальной извитости:
-
синдром Марфана (извитость аорты ассоциирована с более высоким риском ее расслоения);
-
синдром Луиса-Дитца (чаще всего встречается извилистость артерий головы и шеи, однако она может быть и генерализованной);
-
синдром аневризмы-остеоартроза (характерна извилистость мозговых, грудных и брюшных артерий, ранние расслоения);
-
эластолизис (cutis laxa) 1B (характерны аневризмы аорты, извитость и стеноз артерий; у младенцев может встречаться летальная извитость сосудов шеи и головного мозга);
-
болезнь Менкеса (описана выраженная извитость цереброваскулярных сосудов).
Провести дифференциальную диагностику данных заболеваний позволяет только расширенное молекулярно-генетическое исследование.
Молекулярно-генетическая диагностика синдрома Марфана и марфаноподобных заболеваний
Диагностика синдрома Марфана и марфаноподобных заболеваний входит в тест Исследование панели генов наследственной дисплазии соединительной ткани по результатам полноэкзомного секвенирования. Данная панель позволяет не только выполнять диагностику синдрома Марфана и марфаноподобных заболеваний, но и проводить дифференциальную диагностику данного синдрома с другими наследственными дисплазиями соединительной ткани. В ряде случаев синдром Марфана имеет перекрестный фенотип с другими заболеваниям из этой группы, и дифференцировать их позволяет только молекулярно-генетическая диагностика.
1) Milewicz DM, Braverman AC, De Backer J, Morris SA, Boileau C, Maumenee IH, Jondeau G, Evangelista A, Pyeritz RE. Marfan syndrome. Nat Rev Dis Primers. 2021 Sep 2;7(1):64. PMCID: PMC9261969
2) Du Q, Zhang D, Zhuang Y, Xia Q, Wen T, Jia H. The Molecular Genetics of Marfan Syndrome. Int J Med Sci. 2021 May 27;18(13):2752-2766. PMCID: PMC8241768
3) Pollock L, Ridout A, Teh J, Nnadi C, Stavroulias D, Pitcher A, Blair E, Wordsworth P, Vincent TL. The Musculoskeletal Manifestations of Marfan Syndrome: Diagnosis, Impact, and Management. Curr Rheumatol Rep. 2021 Nov 26;23(11):81. PMCID: PMC8626407
4) Румянцева В.А., Рогожина Ю.А., Котлукова Н.П., Заклязьминская E.В. Неонатальная форма синдрома Марфана — клиническое описание и комплексный подход к диагностике и лечению. Российский кардиологический журнал. 2014;(5):55-60.
5) Akram H, Aragon-Martin JA, Chandra A. Marfan syndrome and the eye clinic: from diagnosis to management. Ther Adv Rare Dis. 2021 Nov 9;2:26330040211055738. PMCID: PMC10032431
6) Pugnaloni F, De Rose DU, Digilio MC, Magliozzi M, Braguglia A, Valfrè L, Toscano A, Dotta A, Di Pede A. Neonatal Marfan syndrome: a case report of a novel fibrillin 1 mutation, with genotype-phenotype correlation and brief review of the literature. Ital J Pediatr. 2024 Sep 18;50(1):183. PMCID: PMC11411867
7) Jacquinet A, Verloes A, Callewaert B, Coremans C, Coucke P, de Paepe A, Kornak U, Lebrun F, Lombet J, Piérard GE, Robinson PN, Symoens S, Van Maldergem L, Debray FG. Neonatal progeroid variant of Marfan syndrome with congenital lipodystrophy results from mutations at the 3' end of FBN1 gene. Eur J Med Genet. 2014 Apr;57(5):230-4. PMID: 24613577
8) Graul-Neumann LM, Kienitz T, Robinson PN, Baasanjav S, Karow B, Gillessen-Kaesbach G, Fahsold R, Schmidt H, Hoffmann K, Passarge E. Marfan syndrome with neonatal progeroid syndrome-like lipodystrophy associated with a novel frameshift mutation at the 3' terminus of the FBN1-gene. Am J Med Genet A. 2010 Nov;152A(11):2749-55. PMID: 20979188
9) Чижонкова Е.А., Аветисов К.С., Аветисов С.Э. Наследственно обусловленные варианты эктопии хрусталика: диагностика и хирургическое лечение. Вестник офтальмологии. 2023;139(1):129‑136.
10) Knight LSW, Mullany S, Taranath DA, Ruddle JB, Barnett CP, Sallevelt SCEH, Berry EC, Marshall HN, Hollitt GL, Souzeau E, Craig JE, Siggs OM. The phenotypic spectrum of ADAMTSL4-associated ectopia lentis: Additional cases, complications, and review of literature. Mol Vis. 2022 Sep 4;28:257-268. PMCID: PMC9514546
11) Нарушение обмена серосодержащих аминокислот (гомоцистинурия). Клинические рекомендации МЗ РФ. 2025 г. https://cr.minzdrav.gov.ru/view-cr/483_3
12) Бучинская Н.В., Исупова Е.А., Костик М.М. Гомоцистинурия: литературный обзор и описание клинического случая. Вопросы современной педиатрии. 2019;18(3):187-195. https://doi.org/10.15690/vsp.v18i3.2036
13) Walter, J.H., Blom, H.J. (2019). The Homocystinurias. In: Oohashi, T., Tsukahara, H., Ramirez, F., Barber, C., Otsuka, F. (eds) Human Pathobiochemistry. Springer, Singapore. https://doi.org/10.1007/978-981-13-2977-7_8
14) Семячкина А.Н., Близнец Е.А., Воинова В.Ю., Боченков С.В., Харабадзе М.Н., Николаева Е.А., Поляков А.В. Синдром Билса (врожденная контрактурная арахнодактилия) у детей: клиническая симптоматика, диагностика, лечение и профилактика. Российский вестник перинатологии и педиатрии. 2016;61(5):47-51.
15) Белозеров Ю.М. (2013). Наследственный синдром извилистых артерий. Российский вестник перинатологии и педиатрии, 58 (4), 20-23.
16) Nanayakkara DNP, Hartley R, Wijesinghe HE, Ganeshan A. Arterial tortuosity syndrome. BMJ Case Rep. 2025 Aug 4;18(8):e266518. PMID: 40759497
17) Ritelli M, Chiarelli N, Dordoni C, Reffo E, Venturini M, Quinzani S, Monica MD, Scarano G, Santoro G, Russo MG, Calzavara-Pinton P, Milanesi O, Colombi M. Arterial Tortuosity Syndrome: homozygosity for two novel and one recurrent SLC2A10 missense mutations in three families with severe cardiopulmonary complications in infancy and a literature review. BMC Med Genet. 2014 Nov 6;15:122. PMCID: PMC4412100
18) Cotti Piccinelli S, Premi E, Bonacina S, Gilberti N, Vergani V, Gamba M, Spezi R, Delrio I, Bernier M, Costa A, Ravanelli M, Colombi M, Gasparotti R, Padovani A, Magoni M. Arterial tortuosity syndrome causing recurrent transient ischemic attacks in young adult: a case report. BMC Neurol. 2021 Nov 30;21(1):464. PMCID: PMC8630900
19) Ciurică S, Lopez-Sublet M, Loeys BL, Radhouani I, Natarajan N, Vikkula M, Maas AHEM, Adlam D, Persu A. Arterial Tortuosity. Hypertension. 2019 May;73(5):951-960. PMID: 30852920