Определение и эпидемиология
Аутоиммунная гемолитическая анемия (АИГА) - заболевание, при котором происходит повышенная деструкция эритроцитов антиэритроцитарными аутоантителами различных классов иммуноглобулинов с участием или без участия компонентов комплемента. Заболевание может быть первичным (идиопатическим) или вызванным основным заболеванием (вторичным), включая аутоиммунную патологию, инфекции, лекарства или новообразования. На клиническое течение болезни, а также на выбор терапии влияет тип вовлеченных в патогенез АИГА антител.
Распространенность АИГА относительно высока и оценивается как 17 на 100 000, при этом заболеваемость АИГА у детей и подростков гораздо ниже - 0,2–1,0 на миллион в год. Первичные АИГА и синдром Эванса чаще выявляются у женщин и детей. Вторичные АИГА возникают при системной красной волчанки (СКВ) в основном у женщин, и в основном у мужчин при хроническом лимфоцитарном лейкозе (ХЛЛ). Заболеваемость болезни холодовых агглютининов оценивается как один случай на миллион в год, с преобладанием поражения женщин, преимущественно в странах с северным климатом.
Патогенез АИГА
Гемолиз инициируется связыванием аутоантител с мембраной эритроцитов. Разрушение эритроцитов может происходить непосредственно в крови (внутрисосудистый гемолиз) или с помощью макрофагов в селезенке и/или печени (внесосудистый гемолиз) (рис. 1). Подклассы иммуноглобулинов IgG, IgA и IgM могут связывать комплемент. Макрофаги могут распознавать опсонизированные эритроциты через рецепторы, специфичные для Fc фрагмента IgG и C3d. Эритроциты, покрытые IgG или комплементом, разрушаются в селезенке и печени, покрытые IgG - в селезенке, и покрытые IgM - в печени.
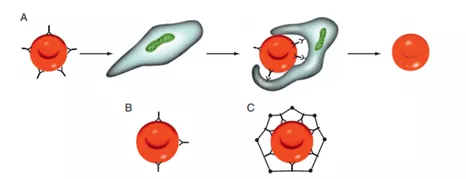
Рисунок 1. Механизм экстраваскулярного гемолиза при АИГА (A) Макрофаг встречается с покрытым IgG эритроцитом и связывается с ним через Fc-рецепторы. Пойманный в ловушку эритроцит теряет элементы своей мембраны. Дискоидный эритроцит превращается в сферу. (B) Эритроциты, в меньшей степени покрытые IgG (и поэтому неспособные активировать каскад комплемента) преимущественно удаляются в циркуляции селезенки. (C) Эритроциты с большей степенью покрытия IgG, который взаимодействует C3b (черный круг на картинке), может быть удален как селезенкой, и печенью.
Тепловая аутоиммунная гемолитическая анемия
От 70% до 80% случаев аутоиммунной гемолитической анемии (АИГА) являются тепловой АИГА (ТАИГА). Антитела к эритроцитам при ТАИГА представляют собой в основном поликлональные IgG (IgG1–4), которые имеют низкую способность активировать систему комплемента. Прямая проба Кумбса (тест 01.02.15.890), он же DAT (direct antiglobulin test - DAT), при ТАИГА положительна либо с IgG (37%), либо с IgG + C3d (43%). Реже выявляются антиэритроцитарные антитела к C3d (когда количество IgG на эритроцитах небольшое). Пациенты с антителами IgG могут также иметь антитела IgA, но выявление антител IgA без антител IgG являются очень редкой причиной ТАИГА. Аутоантитела при ТАИГА часто направлены против резус-антигенов, но также против других антигенов группы крови (не-Rh-связанных аутоантител), таких как белок полосы 3 или гликофорин А. Антитела фиксируются и плотно связываются с эритроцитами при 37° C. Поэтому в сыворотке обнаруживается лишь небольшое количество антител. Покрытые антителами эритроциты удаляются из кровотока селезеночными (в меньшей степени также печеночными) макрофагами через рецепторы FcγRIII. IgG3 и IgG1 обладают наибольшим сродством к Fc-рецепторам макрофагов. Эритроциты, которые только частично фагоцитируются макрофагами, становятся сфероцитами, которые удаляются селезенкой из-за их жесткой структуры. Разрушение эритроцитов также может быть вызвано другими механизмами, такими как антитело-зависимая цитотоксичность.
ТАИГА, ассоциированная с IgM аутоантителами, является очень редкой причиной АИГА. Этот тип АИГА можно заподозрить, если агглютинация эритроцитов происходит при комнатной температуре. Результат Пробы Кумбса является положительным в 64% с C3d и в 24% с IgG. Используя чувствительные методы, IgM на эритроцитах может быть обнаружен в 71%. ТАИГА, ассоциированная с IgM, часто выявляется на фоне неходжкинской лимфомы и является тяжелым, часто смертельным и рефрактерным к стероидам и спленэктомии осложнением.
Холодовая аутоиммунная гемолитическая анемия
Первычные и вторичные холодовые аутоиммунные гемолитические анемии (ХАИГА) обычно ассоциированы с моноклональным IgM. Антиэритроцитарные антитела класса IgM имеют два сайта связывания для C1q и обладают высокой способностью связывать комплемент. Мишенями данных антител являются полисахариды (I, IT, I, Pr антигены). «i» антиген представляет собой неразветвленный полисахарид в пуповинной крови, и «I» антиген представляет собой сходную, но разветвленную молекулу, экспрессируемую на эритроцитах у взрослых. Антитела при ХАИГА связываются с эритроцитами при низких температурах и вызывают их лизис при температуре выше 22°С. Проба Кумбса обычно положительна только с C3d. Когда холодовые агглютинины присутствуют в высоком титре, они могут напрямую активировать систему комплемента и приводят к внутрисосудистому гемолизу с гемоглобинурией. Обычно эритроциты, покрытые комплементом, удаляются макрофагами печени.
Пароксизмальная холодовая гемоглобинурия (ПХГ) ассоциирована с антителами Доната-Ландштейнера (аДЛ). Это редкие, обычно поликлональные холодовые IgG антитела против P-антигена (гликосфинголипид глобозид), которые связываются с эритроцитами при 4 ° С. Клетки лизируются при более высоких температурах. Проба Кумбса положительная с C3d. Диагноз устанавливается с помощью определения аДЛ. Отличительной клинической чертой ПХГ является быстрая, немедленная, но иногда и отсроченная гемоглобинурия после холодового воздействия даже у пациентов с низкими титрами антител. В прошлом это было связано с вторичным или третичным сифилисом. Теперь можно выделить два основных клинических варианта: (1) острая, тяжелая форма (часто связанная с гемоглобинурией) ИГА после (респираторных) инфекций у детей и (2) редкая хроническая АИГА у лиц с различными основными заболеваниями, в том числе неходжскинскими лимфомами. Пациенты с хроническим ПХГ плохо отвечают на стероиды и спленэктомию.
Таблица 1. Характектеристики антиэритроцитарных аутоантител
|
|
Ig |
Клональ-ность | Специфич-ность |
Гемолиз |
Место разрушения эритроцитоа |
|---|---|---|---|---|---|
| Тепловая АИГА |
IgG, IgA |
Поли- |
Rh-антиген, не-Rh-антиген |
Внесосудистый |
Селезенка (печень) |
|
Холодовая АИГА |
IgM |
Моно- |
Anti-i, -IT,-l, -Pr |
Внутрисосудистый |
Печень |
|
Пароксизмальная холодовая гемолитическая анемия |
IgG |
Поли- |
Р антиген |
Внутрисосудистый |
- |
Смешанная тепловая и холодовая АИГА
Клинические проявления
Симптомы аутоиммунной гемолитической анемии зависят от типа антиэритроцитарых антител, манифестации и тяжести анемии. У пациентов с ТАИГА дебют заболевания в основном постепенный или подострый, и симптомы (усталость,снижение физической активности и одышка) относятся только к анемии. Тем не менее, пациенты спостинфекционными или вызванными лекарственными средствами АИГА или пациенты с холодовыми агглютининами или антителами Доната-Ландштейнера часто манифестируют с тяжелыми симптомами, такими как недомогание,лихорадка, желтуха, боли в животе, одышка и гемоглобулинурия. Течение заболевания у таких пациентов может быть молниеносным и даже смертельным.Хроническая ХАИГА характеризуется такими симптомами, какхолодовая чувствительность,акроцианоз, онемение конечностей и ретикулярное ливедо. Анемияухудшается после воздействия холода или при развитии острофазных реакций.Во время клинического осмотра кожные покровы могут быть субиктеричными. Лимфаденопатия, спленомегалия или любая другая органомегалия встречаются редко.Пациенты с ТАИГА имеют повышенный риск венозной тромбоэмболии, иногда связанной с волчаночным антикоагулянтом. У пожилых пациентов с АИГА повышен риск сердечно-сосудистых осложнений.
Лабораторная диагностика АИГА
Первым шагом в диагностике причины анемии является лабораторный скрининг феномена гемолиза. Этот диагноз устанавливается по наличию следующих лабораторных маркеров: нормоцитарная или макроцитарная анемия (гемоглобин у мужчин <13,0–14,0 г/дл; у женщин <12,0 г/дл), ретикулоцитоз (скорректированное количество ретикулоцитов > 2% или абсолютное количество ретикулоцитов >100 000 кл/мкл до 120 000 кл/мкл), низкий гаптоглобин (менее 0,3 г/л), повышенная лактатдегидрогеназа (ЛДГ) и повышенный неконъюгированный (непрямой) билирубин.
Гаптоглобин представляет собой α2-глобулин, который связывает гемоглобин. Он удаляет гем из эритроцитов и защищает организмы от неблагоприятного воздействия циркулирующего гемоглобина. Комплекс гемоглобин-гаптоглобин разрушается в печени. Непрямой билирубин обычно составляет не более 5 мг/дл, за исключением случаев ассоциированного заболевания печени (Эпштейна-Барр-ассоциированная гемолитическая анемия). Дополнительными показателями являются повышенные уровни уробилиногена в моче и сфероцитах в мазок периферичсекой крови. Лейкоэритробластоз происходит только в случае острой АИГА, но микроангиопатическая гемолитическая анемия должна всегда исключаться в таких случаях. В исследовании костного мозга обычно нет необходимости, за исключением пациентов в подозрением на вторичную гемолитическую анемию в частности, при лимфоме.
Все 5 лабораторных диагностических признаков не всегда выявляются по следующим причинам. Ретикулоцитоз часто (в ≈25%) отсутствует в начале развития АИГА, который появляется у большинства этих пациентов через 1 неделю. У других пациентов (особенно при вторичных АИГА) отсутствие ретикулоцитоза может быть связано с нарушением эритропоэза и вызвано инфильтрацией костного мозга или ингибированием эритропоэза острофазной реакцией. Если количество ретикулоцитов очень мало, следует подозревать парвовирусную (или HHV6) инфекцию. Уровни гаптоглобина могут быть нормальными или даже увеличенными, особенно у пациентов со злокачественными или аутоиммунными заболеваниями, потому что гаптоглобин является белком острой фазы. Гаптоглобин может быть ложноотрицательным у пациентов с гаплотипом H0H0 и у пациентов с тяжелым заболеванием печени. Как повышенный билирубин, так и повышенный уровень ЛДГ имеют ограниченную специфичность для АИГА.
Следующим шагом является выяснение, является ли гемолитическая анемия аутоиммунной. Для этого используются скрининговая проба с полиспецифическими агглютининами (Полиспецифические агглютинины - прямая проба Кумбса (DAT-screen) тест 01.02.15.890).В этом тесте эритроциты пациентов инкубируются в пробирке с полиспецифическими антителами к IgG, IgM, IgA и компонентам комплемента (C3d). Если эритроциты агглютинируют, результат теста положительный.
В непрямой пробе Кумбса сперва инкубируют плазму или сыворотку пациента эритроцитами, и (после промывания) эритроцит-связанный IgG обнаруживается при инкубации в пробирке с полиспецифическими антителами к IgG и комплементом (C3d). Непрямая проба Кумбса обычно не требуется для диагностики АИГА, кроме случаев, когда есть подозрение на лекарственно-зависимые антитела. Степень тяжести заболевания не коррелирует с выраженностью агглютинации в пробе Кумбса, а скорее с подклассом иммуноглобулина IgG (IgG1 или IgG3). Результат скрининговой прямой пробы Кумбса не является надежным маркером эффективной терапии, потому что пациенты с ремиссией могут оставаться Кумбс-положительными, и результаты пробы Кумбса имеют ограниченное значение для прогнозирования длительности ремиссии.
Следующий этап тестирования является подтверждающим, когда пробу Кумбса проводят проводят с моноспецифическими антителами на IgG, IgM, IgA и компонентам комплемента C3d и С3с (Моноспецифические агглютинины - проба Кумбса подтверждение - confirmatory DAT, тест 01.02.15.895), чтобы узнать, тепловые или холодовые антитела является причиной гемолиза. Если результат пробы Кумбса положительный только с IgG или с IgG и C3d, то диагноз скорее всего теплова аутоиммунная гемолитическая анемия, если же агглютинация проявилась только при реакции с C3d, это более характерно для холодовой аутоиммунной гемолитической анемии.
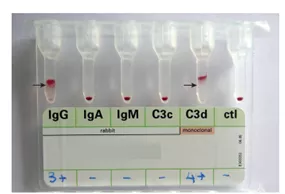
Рисунок 2. Результат прямой пробы Кумбса подтверждение (тест 01.02.15.895) на гель-картах, с позитивным результатом на анти-IgG и анти-с3d антитела
Дифференциальный диагноз тепловой и холодовой гемолитической анемии крайне важен для выбора терапии пациентов. Если подозревается ХАИГА, очень важно, чтобы материал был доставлен при температуре 37 °С для получения достоверных результатов. Анализ на холодовую гемолитическую анемию, или болезнь холодовых агглютининов, позволяет обнаружить антиэритроцитарные антитела против I/i-антигенов на поверхности мембран эритроцитов, приводящие к агглютинации эритроцитов при температуре <37оС (чаще IgM, C3d-,C3c-компоненты комплемента). Положительный результат выявления холодовых агглютининов (тест 01.02.15.900) подтверждает наличие болезни холодовых агглютининов.
Если результат пробы Кумбса отрицательный при очевидном гемолизе, гемолитическая анемия определяется как Кумбс-негативная. Тем не менее, аутоиммунная гемолитическая не может быть полностью исключена, так как около 5% (от 2% до 11%) пациентов с АИГА Кумбс-отрицательные. Если у пациента наблюдается характерная картина АИГА, несмотря на отрицательный результат скрининговой пробы Кумбса/DAT-screen тест 01.02.15.890, необходимы дообследование более чувствительные количественные тесты для определения IgG на эритроцитах (Моноспецифические агглютинины - проба Кумбса подтверждение - confirmatory DAT, тест 01.02.15.895). Порог позитивности обычной пробы Кумбса составляет 100–200 молекул IgG на эритроцит, но у некоторых пациентов с АИГА уровень IgG меньше. Связь между количеством эритроцитов IgG и гемолизом не уставлена, нет «порога гемолиза», и причины для расхождений между активностью антиэритроцитарных антител in vitro и in vivo неизвестны. Проведение теста в элюате эритроцитов, когда антитела более сконцентрированы, может быть информативно. Другой причиной ложноотрицательных результатов пробы Кумбса является низкая аффинность антиэритроцитарных антител. Часто вторичные АИГА, а также АИГА, индуцированные аналогами нуклеозидов, бывают Кумбс-отрицательными. Также важно отметить, что положительная проба Кумбса выявляется от 1 до 3 случая среди10000 здоровых доноров и 10% госпитализированных пациентов без анемии или признаков гемолиза. Положительная проба Кумбса отмечается у 30-40% случаев больных с системной красной волчанкой и входит к диагностичекие критерии этого заболевания. Обычно гемолитическая анемия у больных с системной красной волчанкой сопровождается многоростковой цитопений и появлением других антител к форменным элементам крови, в частности антител к лимфоцитам (тест 01.02.15.925).
На последнем этапе диагностики необходимо определить, является ли аутоиммунная гемолитическая анемия первичной или представляет собой осложнение основного заболевания (вторичная АИГА). Решение о том, какие диагностические процедуры следует использовать для этой цели, зависит в основном от типа АИГА (ТАИГА или ХАИГА). Такое обследование доложно включать анамнез и осмотр больного, лабораторные анализы и данные инструментальных методов. У детей и более молодых пациентов с ТАИГА необходимо исключать инфекционную патологию и тщательно изучить список всех недавних лекарств. Потеря веса, лихорадка и артрит указывают на онкологические процессы или системные аутоиммунные заболевания, прежде всего системную красную волчанку. Лимфаденопатия и спленомегалия обычно не относятся к клинической картине первичной ТАИГА, и при их обнаружении следует исключить лимфому (особенно часто лимфому маргинальной зоны селезенки).
Лабораторное обследование должно включать исследование белков острой фазы, углубленное гематологическое обследование, исследования маркеров инфекционных и аутоиммуных заболевания, например скрининг системных заболеваний соединительной ткани (тест 01.02.15.245). УЗИ брюшной полости целесообразно во всех случаях для исключения спленомегалии, тератомы яичников (у женщин), лимфаденопатии или одиночной экстранодальной лимфомы. При ХАИГА и лихорадке в анамнезе рекомендуется выполнить рентгенография. Количественное определение сывороточных иммуноглобулинов и иммунофиксация иммуноглобулинов необходимы для исключения лимфомы (Скрининг парапротеинов в сыворотке с помощью иммунофиксации с поливалентной антисывороткой, тест 01.02.15.421) Другие анализы, в том числе выявления метаболических нарушений, функциональные тесты почек и печени, исключение латентного туберкулеза необходимы, чтобы избежать осложнений стероидов (ТАИГА) или ритуксимаб (ТАИГА И ХАИГА).
1) Dacie SJ: The immune haemolytic anaemias: a century of exciting progress in understanding. Br J Haematol 114:770, 2001.
2) Packman CH: Hemolytic anemia due to warm autoantibodies. Blood Rev 22:17, 2008.
3) Garratty G: Immune hemolytic anemia-a primer. Semin Hematol 42:119,2005.
4) Petz LD: Immune hemolysis associated with transplantation. Semin Hematol 42:145, 2005.
5) Pirofsky B: Clinical aspects of autoimmune hemolytic anemia. Semin Hematol 13:251, 1976.
6) Berentsen S, Ulvestad E, Langholm R, et al: Primary chronic cold agglutinin disease: a population based clinical study of 86 patients. Haematologica 91:460, 2006.
7) King KE, Ness PM: Treatment of autoimmune hemolytic anemia. Semin Hematol 42:131, 2005.
8) Lechner K, Jäger U: How I treat autoimmune haemolytic anemias in adults. Blood 116:1831, 2010.
9) Aladjidi N, Leverger G, Leblanc T, et al: New insights into childhood autoimmune hemolytic anemia: a French national observational study of 265 children. Haematologica 96:655, 2011.
10) Michel M, Chanet V, Dechartres A, et al: The spectrum of Evans syndrome in adults: new insight into the disease based on the analysis of 68 cases. Blood 114:3167, 2009.
11) Brodsky RA: Complement in hemolytic anemia. Blood 126:2459, 2015.
12) Berentsen S: Role of complement in autoimmune hemolytic anemia. Transfus Med Hemother 42:303, 2015.
13) Garratty G: The James Blundell Award Lecture 2007: Do we really understand immune red cell destruction? Transfusion Med 18:321, 2008.
14) Arndt PA, Leger RM, Garratty G: Serologic findings in autoimmune hemolytic anemia associated with immunoglobulin M warm autoantibodies. Transfusion 49:2352, 2009.
15) Sokol RJ, Booker DJ, Stamps R, et al: Autoimmune hemolytic anemia caused by warm-reacting IgM-class antibodies. Immunohematol 14:53, 1998.
16) Barcellini W: New insights in the pathogenesis of autoimmune hemolytic anemia. Transfus Med Hemother 42:287, 2015.