Железодефицитная анемия
Определение
Железодефицитная анемия (ЖДА) – это приобретенное заболевание, характеризующееся снижением содержания железа в сыворотке крови, костном мозге и тканевых депо, в результате чего нарушается образование гемоглобина и эритроцитов, развивается гипохромная микроцитарная анемия и трофические расстройства в тканях. Дефицит железа в организме может быть вызван нарушением поступления, усвоения или повышенными потерями данного микроэлемента.
Диагностическими критериями анемии, по данным ВОЗ, являются показатели гемоглобина ниже 130 г/л у мужчин всех возрастов, для небеременных женщин репродуктивного возраста менее 120 г/л, для беременных — менее 110 г/л. Эти стандарты ВОЗ используются врачами большинства стран в целях профессиональной согласованности.
Эпидемиология
ЖДА является одним из самых распространенных заболеваний в мире. Экспертами ВОЗ было показано, что анемия чаще встречается в развивающихся странах и наиболее подвержены анемии такие группы населения, как женщины репродуктивного возраста, беременные женщины, дети раннего возраста и пожилые люди. По данным ВОЗ, железодефицитной анемией болеют около 2 млрд человек в мире, а латентный дефицит железа отмечается у 3,6 млрд населения.
Выраженный дефицит железа отмечается у каждой третьей женщины репродуктивного возраста и у каждой второй беременной, являясь важной причиной хронической усталости и плохого самочувствия, и третьей по распространенности причиной временной потери трудоспособности у женщин в возрасте 15–44 лет. Основными причинами развития ЖДА у женщин служат тяжелые менструальные кровотечения, беременность, роды (особенно повторные) и лактация. Важнейшей по значимости медицинской и социальной проблемой является анемия у беременных, которая, по данным ВОЗ, выявляется у 24–30% женщин в экономически развитых странах и более чем у 50% женщин в странах с низким уровнем экономики.
Согласно публикации «Здравоохранение в России: статистический сборник (2021)» в 2020 г. анемия (все виды анемии) зарегистрирована у 1406,8 тыс. человек, из них у 438,9 тыс. человек диагноз анемии установлен впервые. Данные обследования более 8 тыс. взрослых пациентов амбулаторного звена показали, что у женщин анемия встречалась в 12–13% случаев, причем у женщин в возрасте 40–49 лет частота достигала 21–22%, у мужчин – 2,8–5,6% с пиком до 21% в возрасте 60—69 лет. Основными причинами высокой распространенности анемии, включая ЖДА, в России эксперты считают алиментарный фактор, в том числе недостаточное потребление железа с пищей, и низкую осведомленность населения об этом заболевании.
По данным Росстата от 2021 г. анемия (без уточнения этиологии) определяется у 35,5 % беременных женщин, без существенного снижения частоты заболевания за последние годы, в то время как распространенность анемии у детей раннего возраста в России ниже общепопуляционной и составляет около 0,8 %. У лиц пожилого и старческого возраста анемия регистрируется, по разным оценкам, с частотой 23 – 46 % и наиболее характерна для пациентов старше 80 лет. В этиологической структуре анемий у пожилых пациентов преобладают дефицитные состояния.
В структуре анемий ЖДА являются наиболее частой анемией.
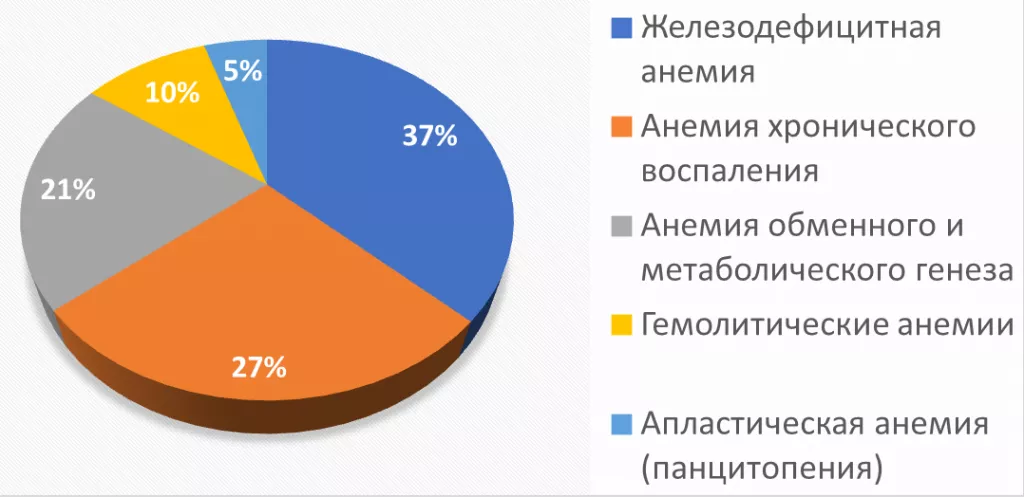
Рисунок 1. Наиболее частые причины анемий в клинической практике (ВОЗ, 2016).
Этиология и патогенез
Железо — наиболее распространенный микроэлемент в организме человека. Оно имеет принципиальное значение для транспорта кислорода, эритропоэза и играет важную роль во многих биологических процессах, в частности таких, как синтез ДНК, РНК, аминокислот, коллагена, стероидов, различных нейротрансмиттеров и белков, участвующих в транспорте электронов, митохондриальном дыхании, клеточной пролиферации, дифференцировке и регуляции экспрессии генов, а также в функционировании иммунной системы, процессах детоксикации и метаболизма лекарственных средств. Железо не синтезируется в организме человека, и его гомеостаз контролируется главным образом за счет поступления с пищей, всасывания в кишечнике и механизмов рециркуляции.
Метаболизм железа
Железо является важным микроэлементом, который используется главным образом в качестве компонента гема в эритроцитах для транспорта кислорода, в меньшем количестве присутствует в мышцах в виде миоглобина и в печени в виде ферритина. Достаточный его уровень необходим для поддержания физиологического гомеостаза. Вместе с тем избыточный уровень железа может привести к гибели клеток через образование свободных радикалов и перекисное окисление липидов биологических мембран, токсическое повреждение белков и нуклеиновых кислот. Таким образом, и дефицит, и перегрузка железом могут иметь катастрофические последствия для организма, поэтому содержание данного микроэлемента жестко регулируется.
В организме здорового человека содержится около 3–5 г железа. Примерно 2,5 г этого железа присутствует в гемоглобине для транспорта кислорода, а еще 2 г хранится в виде ферритина, в основном в костном мозге, печени и селезенке. В костном мозге железо используется для образования гемоглобина, железо печени — главный резерв микроэлемента. Наконец, относительно небольшое количество железа (примерно 400 мг) присутствует в клеточных белках, таких как миоглобин и цитохромы, и примерно 3–4 мг связано с транспортным белком трансферрином. Практически все метаболически активное железо находится в связанном с белками состоянии, свободные ионы железа могут присутствовать в крайне низких концентрациях.
Уровень железа плазмы строго регулируется. В естественных условиях ежедневно теряется не более 0,05% (<2,5 мг) от общего количества железа за счет слущивающегося эпителия кожи и желудочно-кишечного тракта (ЖКТ), а также в результате потоотделения.
Для эффективного эритропоэза ежедневно требуется 20–30 мг железа. 90% ежедневной потребности обеспечивается эндогенным железом, поступающим в ходе рециркуляции. Пополнение происходит из железа, поглощаемого макрофагами селезенки и печени из стареющих эритроцитов. Значительно меньшее количество железа (1–2 мг в день) всасывается из пищи в двенадцатиперстной кишке, где усвоение железа возможно только в двухвалентном состоянии (Fe2+), поскольку трехвалентное железо (Fe3+) практически не всасывается.
Суточная потребность в железе у взрослых мужчин и женщин составляет 13 мкг на 1 кг массы тела и 21 мкг на 1 кг массы тела соответственно. В соответствии с этим рекомендуемая доза железа в сутки составляет 8–10 мг и 18 мг для взрослых мужчин и женщин в пременопаузе соответственно.
Обычная диета обеспечивает поступление от 5 до 15 мг элементарного железа в день. В ЖКТ (двенадцатиперстной кишке и верхнем отделе тощей кишки) всасывается лишь 10–15% железа, содержащегося в пище. Усвоение железа из пищи зависит от его количества в рационе, функционирования желудочно-кишечного тракта, физиологических потребностей. Пищевое железо содержится в виде гемового (мясо) и негемового (растительные источники) железа. Гемовое железо эффективно усваивается и менее подвержено влиянию других компонентов рациона, в то время как усвоение негемового железа менее эффективно и подвержено указанному влиянию, в связи с чем вегетарианская диета представляет собой фактор высокого риска дефицита железа. Витамин С улучшает усвоение негемового железа, а фитаты, содержащиеся в семенах и злаках, кальций и дубильные вещества, содержащиеся в чае и кофе, препятствуют усвоению негемового железа. Железо также может не усваиваться у людей с кишечными расстройствами.
В условиях сидеропении железо, всосавшееся в кишечнике, сразу поступает в кровоток, соединяясь с трансферрином. В составе трансферрина железо поступает в основные клетки-потребители: в гепатоциты, образуя депо в виде молекул ферритина, в клетки костного мозга и другие клетки, обладающие высокой пролиферативной активностью и имеющие на своей мембране рецепторы к трансферрину. Железо циркулирует в кровотоке в составе эритроцитов в течение в среднем 120 дней (период жизни эритроцитов), которые затем постепенно разрушаются под воздействием макрофагов селезенки и печени. Высвобожденный пул железа вновь окисляется до трехвалентного состояния церулоплазмином и соединяется с трансферрином, повторно поступая в клетки-потребители.
Основным регулятором всасывания железа в кишечнике и высвобождения его из макрофагов и гепатоцитов является пептидный гормон гепсидин (см. ниже).
Основные показатели метаболизма железа
К запасным формам железа относят ферритин и гемосидерин, содержащиеся в клетках ретикулоэндотелиальной системы и печени.
Ферритин представляет собой главное депо железа в организме. Он является растворимым в воде комплексом апоферритина и гидроокиси железа (ферритин включает до 4500 ионов Fe2+). Он является внутриклеточным белком и содержится во многих органах и тканях, преобладая в клетках печени, селезенки, костного мозга, также циркулирует в сыворотке крови. Основная функция данного белка заключается в депонировании железа и высвобождении по мере потребности, в связи с этим его концентрация в плазме крови отражает запасы железа в организме в физиологических условиях. Его уровень в сыворотке крови составляет 30–300 мкг/л. Для ЖДА характерно снижение концентрации ферритина <30 мкг/л. Повышение ферритина >300 мкг/л свидетельствует о перегрузке железом, деструкции клеток и воспалении. Также следует отметить, что ферритин относится к острофазовым белкам и значительно повышается при наличии в организме человека воспалительного очага или очага опухолевого роста. Тем не менее, при наличии воспаления ВОЗ предлагает диагностировать дефицит железа при концентрации ферритина менее 30 мкг/л у детей в возрасте до 5 лет и менее 70 мкг/л у детей старшего возраста и взрослых.
Гемосидерин, являясь еще одним белком, обеспечивающим депонирование железа, представляет собой нерастворимое в воде производное ферритина, труднее высвобождающее железо.
Трансферрин является белком, играющим ключевую роль в транспорте железа. Он отвечает за внеклеточный транспорт железа от места всасывания, из энтероцитов тонкого кишечника, депо и мест его высвобождения в результате катаболизма эритроцитов (печень, селезенка) к месту его нового использования, т.е. к клеткам-предшественникам эритроидного ряда в костном мозге. Примерно 0,1–0,2% от общего количества железа в организме связывается с трансферрином, и в этой форме железо может поступать в ткани через рецептор трансферрина. Трансферрин синтезируется в гепатоцитах, в норме его уровень составляет 2–3 г/л. Увеличение количества трансферрина является следствием тканевого дефицита железа, и наоборот снижение трансферрина отражает перегрузку организма железом или нарушение белково-синтетической функции печени.
При лабораторном исследовании с уровнем трансферрина взаимосвязаны также такие показатели, как уровень сывороточного железа, общая железосвязывающая способность сыворотки (ОЖСС) и насыщение трансферрина железом (НТЖ).
Уровень сывороточного железа отражает транспортируемое в настоящее время количество железа к клеткам, связанного как с трансферрином (основная часть), так и другими белками плазмы. Концентрация железа в сыворотке крови снижается как при дефиците железа, так и при воспалении; сама по себе концентрация железа (вне связи с другими показателями) не может быть использована для диагностики железодефицита. Сывороточное Fe (нормальное содержание у женщин – 12–25 мкмоль/л, у мужчин – 13–30 мкмоль/л) снижено при выраженной ЖДА до 1,8–5,4 мкмоль/л, нетяжелой ЖДА – до 7,2–10,8 мкмоль/л. Проведение этого исследования обязательно до начала терапии препаратами Fe. Не следует определять этот показатель на фоне приема препаратов Fe или в первые 6–7 дней перерыва в приеме препарата.
Общая железосвязывающая способность сыворотки (ОЖСС) представляет собой резервный объем трансферрина, не участвующего в транспорте ионов железа. Отражает количество микромолей железа, которое может связать 1 л сыворотки крови. При ЖДА общая железосвязывающая способность сыворотки составляет > 60 мкмоль/л.
Латентная железосвязывающая способность сыворотки представляет собой разность между общей железосвязывающей способностью сыворотки и сывороточным Fe (в норме составляет 25–48 мкмоль/л).
Насыщение трансферрина железом (НТЖ) является расчетным показателем и определяется как соотношение показателей сывороточного железа и ОЖСС (в норме 20–40%). Показатель полезен для определения низкой доступности железа в плазме для тканей как в абсолютном, так и в функциональном выражении. Для ЖДА характерно снижение НТЖ <25%.
Растворимый рецептор трансферрина (sTfR). Рецептор трансферрина является трансмембранным белком преимущественно эритроидных клеток-предшественниц, инициирующим захват железа в комплексе с трансферрином внутрь клетки для синтеза гемоглобина и образования депо железа. Внеклеточная часть рецептора трансферрина подвергается воздействию протеаз и попадает в кровоток, представляя собой так называемый растворимый рецептор трансферрина (рТФР, sTfR). Уровень рТФР отражает плотность рецепторов трансферрина на клетках (насыщенность клеток железом) и количество клеток с этими рецепторами (эритропоэтическая активность). Количество рТФР в крови пропорционально количеству железа, необходимого для эффективного эритропоэза, то есть чем выше концентрация рТФР, тем более выражен железодефицит. рТФР — единственный маркер железодефицита, на содержание которого в крови не влияет воспалительный процесс.
Индекс растворимый рецептор трансферрина/ферритин (sTfR/log Fer) является интегральным показателем, объединяющим обмен железа и эритропоэтическую функцию костного мозга. Основным источником растворимого рецептора трансферрина являются эритробласты. Уровень растворимого рецептора трансферрина отражают плотность рецепторов трансферрина на клетках (насыщенность клеток железом) и количество клеток с этими рецепторами (эритропоэтическая активность). Ферритин является переносчиком железа, который синтезируется гепатолиенальной системой, определяющий перенос железа из селезенки в костный мозг. Его концентрация значительно снижается при железодефицитной анемии (ЖДА). Уровни ферритина в сыворотке отражают запасы железа, тогда как уровни sTfR отражают степень доступности железа для клеток. Расчет индекса sTfR/log ферритина по этим двум показателям позволяет оценить содержание железа в организме в широком диапазоне нормальных и истощенных запасов железа. Таким образом, индекс sTfR/log ферритина использует взаимную зависимость между двумя переменными, на которые влияет дефицит железа, увеличение sTfR и снижение концентрации ферритина. Комплексное исследование уровней sTfR и ферритина и вычисление индекса sTfR/log ферритина позволяет более тщательно диагностировать анемию хронического воспаления.
Гепсидин – пептидный гормон, который продуцируется клетками печени и регулирует процессы всасывания, рециркуляции и хранения запасов железа. Гепсидин взаимодействует с клеточным рецептором ферропортином (единственный известный клеточный экспортер элементарного железа). По принципу отрицательной обратной связи гепсидин способствует снижению абсорбции пищевого железа в тонком кишечнике, тормозя экспрессию транспортного белка DMT-1, а также способствует интернализации и деградации ферропортина, что приводит к блокировке высвобождения и поступления железа в кровь из энтероцитов, макрофагов и гепатоцитов. В физиологических условиях продукция гепсидина контролируется сложным взаимодействием сигналов, прежде всего уровнем железа в крови и степенью оксигенации ткани печени.
При абсолютном дефиците железа или в периоды повышенной потребности в железе подавление экспрессии гепсидина повышает абсорбцию и рециркуляцию железа для оптимизации его поступления.
При избыточном содержании железа в организме гепсидин блокирует функционирование ферропортина, соединяясь с ним и после поступления внутрь клетки разрушаясь в лизосомах, что приводит к задержке и накоплению железа внутри энтероцитов, которые удаляются путем слущивания.
Гепсидин относится к острофазовым белкам, в связи с чем отмечается повышение уровня гепсидина при воспалительных процессах, протекающих в организме. Продукция гепсидина стимулируется провоспалительными цитокинами, из которых главную роль играет ИЛ-6. При воспалении повышенные концентрации гепсидина и сниженная транскрипция ферропортина ограничивают поступление железа в плазму, вызывая функциональный дефицит железа. Снижение доступности железа для производства эритроцитов вызывает дефицит железа в эритропоэзе, проявляющийся в виде гипохромии, микроцитоза и в конечном счете развитию «анемии хронического воспаления».
Нарушения метаболизма железа
Нарушения метаболизма железа подразделяют на абсолютный и функциональный (относительный или перераспределительный) дефицит железа, и перегрузку железом (гемохроматоз).
Дефицит железа, или сидеропения, — это состояние, при котором общие запасы железа в организме недостаточны для поддержания нормальных метаболических функций.
Функциональный (относительный или перераспределительный) дефицит железа развивается у пациентов с нормальными запасами железа при повышенной продукции гепсидина на фоне воспаления, что приводит к развитию анемии хронических заболеваний (АХЗ).
Абсолютный дефицит железа развивается вследствие значительного снижения запасов железа в депо и проявляется снижением уровня сывороточного ферритина. Выделяют следующие стадии абсолютного дефицита железа:
1) прелатентный дефицит железа – вследствие повышенного расхода железа развивается дефицит железа в депо, снижается уровень ферритина на фоне нормальных показателей гемоглобина крови и уровня сывороточного железа; уровень трансферрина может быть повышен или находиться в пределах нормы; анемический синдром отсутствует;
2) латентный дефицит железа – данная стадия наблюдается в том случае, если повышенный расход железа продолжается и происходит дальнейшее истощение депо; на этом фоне снижается уровень сывороточного железа и насыщения трансферрина железом, повышается концентрация сывороточного трансферринового рецептора, но уровни гемоглобина крови и эритроцитов остаются в пределах нормы; могут отмечаться симптомы, схожие с клиническими проявлениями анемического синдрома;
3) железодефицитная анемия – истощение депо и транспортного железа приводит к снижению уровня гемоглобина, неэффективному эритропоэзу с повышением уровня эндогенного эритропоэтина и клиническим проявлениям анемии.
Классификация ЖДА
1. Классификация анемии в зависимости от причины развития железодефицита.
В соответствии с преобладающим механизмом развития железодефицита, выделяют анемии, связанные с недостаточным поступлением железа с пищей, с повышенной потребностью в железе, с кровопотерей, и с нарушением всасывания железа.
ЖДА вследствие недостаточного поступления железа с пищей (алиментарная недостаточность).
Недостаточное поступление Fe с пищей (например, при голодании, вегетарианстве) происходит в основном за счет нехватки мясных продуктов и отсутствия восполнения физиологических потерь железа. Нередко встречается при неполноценном питание, в т.ч. у пожилых людей.
ЖДА вследствие повышения потребности в железе
Повышенная потребность в Fe отмечается при беременности и лактации, у недоношенных детей, при интенсивном росте в пубертатном периоде, в преклимактерическом периоде; при лечении В12-дефицитной анемии витамином В12.
ЖДА вследствие кровопотери
Основной причиной развития ЖДА у женщин репродуктивного возраста служат тяжелые менструальные кровотечения и дисфункциональные маточные кровотечения. Также к развитию ЖДА могут приводить хронические кровопотери других локализаций: желудочно-кишечные (при рефлюкс-эзофагите, эрозивно-язвенных заболеваниях желудка, опухолях желудка и толстой кишки, болезни Крона, язвенном колите, гельминтозах, дивертикулитах, кровоточащем геморрое), носовые, почечные (при гломерулонефрите, мочекаменной болезни, опухолях), десневые, в замкнутые полости и ткани (изолированный легочный гемосидероз, внематочный эндометриоз). Развитие ЖДА возможно у доноров крови, постоянно сдающих кровь в течение многих лет, а также у пациентов с хронической почечной недостаточностью, находящихся на программном гемодиализе (еженедельные потери 30-40 мл крови в контуре диализатора).
ЖДА вследствие нарушения всасывания железа
Нарушение всасывания железа встречается при энтеритах разного генеза; синдроме мальабсорбции; послеоперационных состояниях (резекция желудка с выключением двенадцатиперстной кишки, резекция тонкой кишки), приеме лекарственных препаратов, угнетающих всасывание Fe.
2. Классификация анемии по уровню гемоглобина (степени тяжести)
Диагностическими критериями анемии, по данным ВОЗ, являются показатели гемоглобина ниже 130 г/л у мужчин всех возрастов, для небеременных женщин репродуктивного возраста менее 120 г/л, для беременных — менее 110 г/л. Эти стандарты ВОЗ используются врачами большинства стран в целях профессиональной согласованности.
Уровни гемоглобина для диагностики анемии и определения ее степени тяжести (ВОЗ)
|
Популяция |
Норма Hb, г/л |
Анемия, степень тяжести |
||
|
Легкая, Hb, г/л |
Средняя, Hb, г/л |
Тяжелая, Hb, г/л |
||
|
Женщины (≥15 лет) |
≥120 |
110-119 |
80-109 |
<80 |
|
Беременные |
≥110 |
90-109 |
70-90 |
<70 |
|
Мужчины(≥15 лет) |
≥130 |
110-129 |
80-109 |
<80 |
Клиническая картина железодефицитной анемии
Основными клиническими проявлениями ЖДА являются анемический (гипоксический) и сидеропенический синдромы.
Анемический синдром обусловлен тканевой гипоксией, его проявления универсальны для всех видов анемий. К основным его проявлениям относятся:
-
слабость и/или быстрая утомляемость;
-
бледность кожи и слизистых;
- головокружение, обмороки;
-
одышка и сердцебиение при привычной физической нагрузке;
-
усиление ангинозных болей при ишемической болезни сердца;
-
снижение толерантности к физической нагрузке;
Сидеропенический синдром обусловлен тканевым дефицитом железа и свойствен только ЖДА.
Основные проявления:
-
сухость кожи, трещины на поверхности кожи рук и ног, в углах рта (ангулярный стоматит);
-
глоссит, сопровождающийся атрофией сосочков, болезненностью и покраснением языка;
-
ломкость, истончение, расслоение ногтей, ногти ложкообразной формы (койлонихия);
-
выпадение волос и раннее их поседение;
-
извращение вкуса (pica chlorotica), пациенты едят мел, уголь, глину, песок и/или сырые продукты: крупы, фарш, тесто;
-
пристрастие к необычным запахам: керосина, мазута, бензина, ацетона, гуталина, нафталина, выхлопных газов машин, которые полностью проходят на фоне приема препаратов Fe;
-
дисфагия (затруднение глотания твердой и сухой пищи).
Другие проявления:
Синдром вторичного иммунодефицита – склонность к частым рецидивам и хронизации инфекционно-воспалительных заболеваний.
Нарушения противоинфекционного иммунитета у пациентов с ЖДА имеют сложный характер. С одной стороны, железодефицит препятствует развитию патогенных микроорганизмов, нуждающихся в железе для собственного роста и размножения. С другой стороны, железодефицит опосредованно приводит к нарушению клеточных механизмов резистентности к инфекциям (снижение микробицидной активности гранулоцитов, нарушение пролиферации лимфоцитов). В целом, предрасположенность пациентов с ЖДА к развитию инфекционных заболеваний не столь велика, как это предполагалось ранее. Напротив, лечение железодефицитных состояний парентеральными препаратами железа значительно увеличивает риск развития инфекций, вероятно, вследствие доступности вводимого железа для использования микроорганизмами и их быстрого роста.
Висцеральный синдром
Основные симптомы:
-
поражение ЖКТ: глоссит, дисфагия, снижение кислотообразующей функции желудка, суб- и атрофический гастрит, вздутие, запоры, поносы;
-
поражение гепатобилиарной системы: жировой гепатоз, дисфункциональные расстройства билиарного тракта;
-
изменения сердечно-сосудистой системы: одышка, тахикардия, кардиалгии, отеки на ногах, ангинозные боли, гипотония, расширение границ сердца влево, наличие приглушенности тонов сердца и систолического шума на верхушке, возможно снижение зубца Т и депрессия сегмента ST на электрокардиограмме;
-
поражение центральной нервной системы: снижение памяти и способности концентрировать внимание;
-
поражение мышц и сфинктеров: мышечная слабость при обычной нагрузке, смешанное недержание мочи.
Кожные покровы бледные, не желтушные, печень, селезенка и периферические лимфатические узлы не увеличены.
Лабораторное и инструментальное обследование при железодефицитной анемии
1) Клинический анализ крови с подсчётом ретикулоцитов.
При ЖДА анемия является гипохромной, микроцитарной, норморегенераторной. Отмечается снижение уровня гемоглобина, гематокрита, среднего содержания и средней концентрации гемоглобина в эритроцитах (МСН и МСНС, соответственно), среднего объема эритроцитов (МСV). Количество эритроцитов обычно находится в пределах нормы. Ретикулоцитоз не характерен, но может присутствовать у пациентов с кровотечениями или при ретикулоцитарном кризе на фоне ферротерапии. Морфологическим признаком ЖДА является гипохромия эритроцитов и анизоцитоз со склонностью к микроцитозу. Перечисленные морфологические характеристики не позволяют отличить железодефицитную анемию от анемии хронических заболеваний (АХЗ), в основе которой лежит перераспределительный дефицит железа, связанный с наличием в организме очага воспаления, инфекции или опухоли (дифференциальную диагностику ЖДА и АХЗ см. ниже).
Анизоцитоз – это изменение размеров эритроцитов. При ЖДА эритроциты имеют неодинаковые размеры со склонностью к микроцитозу.
Пойкилоцитоз – это изменение формы эритроцитов. При ЖДА эритроциты имеют самую разную форму.
Содержание ретикулоцитов в норме составляет до 2%.
Современные гематологические анализаторы способны определять дополнительные параметры, являющиеся индикаторами железодефицитного эритропоэза, к ним относятся Ret-He (содержание гемоглобина в ретикулоцитах) и HYPO-He (процент гипохромных эритроцитов). Снижение показателя Ret-He менее 30,6 пг и увеличение HYPO-He более 5 % свидетельствует о наличии дефицита железа. На значения этих показателей не влияют воспалительные процессы, уремия и беременность, что является важным преимуществом перед биохимическими маркерами метаболизма железа. Увеличение показателя Ret-He на фоне ферротерапии является ранним маркером эффективности лечения ЖДА и опережает развитие ретикулоцитарного криза и повышение концентрации гемоглобина.
2) Показатели обмена железа – исследование уровня железа сыворотки крови, ферритина, трансферрина, общей железосвязывающей способность сыворотки (ОЖСС), насыщения трансферрина железом (НТЖ).
Отличительными признаками ЖДА являются низкий уровень сывороточного ферритина, отражающий истощение тканевых запасов железа, и повышенные показатели ОЖСС и трансферрина, отражающие транспортный пул железа. Показатели сывороточного железа и коэффициент НТЖ в типичных случаях снижены, однако наличие нормальных и даже повышенных показателей не исключает диагноз ЖДА, поскольку прием пациентом накануне исследования железосодержащих препаратов, мясная диета или предшествующая (за 10-14 дней) трансфузия эритроцитсодержащих компонентов крови могут сильно исказить показатель сывороточного железа и, соответственно, коэффициент НТЖ, что необходимо учитывать при оценке результатов исследования. Развитию ЖДА предшествует период латентного железодефицита, лабораторными критериями которого служат низкие показатели сывороточного железа и ферритина на фоне нормального уровня гемоглобина.
Гепсидин (тест 01.02.15.1670) используется для дифференциальной диагностики абсолютного (ЖДА) и функционального (АХЗ) дефицита железа. При ЖДА уровень гепцидина снижен, при АХЗ – повышен.
Растворимый рецептор трансферрина (sTfR) (тест 01.02.15.940) и индекс растворимый рецептор трансферрина/ферритин (sTfR/log Fer) (тест 01.02.15.945) также используются для дифференциальной диагностики ЖДА и АХЗ. При ЖДА оба показателя повышены. При АХЗ sTfR в норме, sTfR/log Fer снижен
3) Всем пациентам с впервые установленным диагнозом ЖДА рекомендуется проведение инструментальных исследований для поиска возможного источника кровотечения и выявления сопутствующей патологии
4) Комплекс исследований для выяснения причины развития ЖДА и диагностики сопутствующей патологии:
-
Общий белок, альбумин c целью оценки белково-синтетической функции печени и корректной интерпретации показателей метаболизма железа
-
Общий, прямой и непрямой билирубин, ЛДГ c целью дифференциальной диагностики ЖДА с гемолитическими анемиями
-
АЛТ, АСТ для исключения цитолитического синдрома
-
Креатинин, мочевина с целью исключения патологии почек
Результаты перечисленных базовых исследований могут указывать направление дальнейшего диагностического поиска. Оценка биохимических показателей функции печени необходима для правильной интерпретации параметров обмена железа, так как нарушение белково-синтетической функции печени приводит к снижению продукции гепатоцитами трансферрина и, как следствие, к снижению показателей сывороточного трансферрина и ОЖСС, искажению расчетного коэффициента НТЖ. Нарушение функции почек может приводить к развитию как относительного, так и абсолютного железодефицита. Оценка других биохимических показателей используется при дифференциальной диагностике с анемиями иной этиологии.
5) Рекомендации по гастроэнтерологическому обследованию пациентов с ЖДА
В практических рекомендациях Американской гастроэнтерологической ассоциации (2020 г.) основное внимание уделяется первичной желудочно-кишечной оценке хронической ЖДА.
У пациентов с анемией при определении уровня ферритина для диагностики железодефицита рекомендуется использовать пороговое значение <45 вместо <15 мкг/л.
Мужчинам и бессимптомным женщинам в постменопаузе с ЖДА рекомендуется проводить верхнюю и нижнюю эндоскопию, данный метод предпочтительней стратегии наблюдения без проведения эндоскопии.
Бессимптомным женщинам с ЖДА в пременопаузе рекомендуется проводить верхнюю и нижнюю эндоскопию, этот метод предпочтительней, чем стратегия эмпирического проведения заместительной терапии препаратами железа. При отказе пациентов с ЖДА от проведения эндоскопии, особенно у лиц молодого возраста, с высокой вероятностью других причин развития ЖДА и низкой вероятности онкопатологии ЖКТ, возможно проведение начального курса заместительной терапии препаратами железа без предварительного эндоскопического исследования.
Пациентам с ЖДА без выявленной причины после проведения верхней и нижней эндоскопии рекомендуется неинвазивное тестирование на Helicobacter pylori (если оно не проводилось раньше) с последующим проведением эрадикации при позитивном тесте.
Пациентам с ЖДА не рекомендуется проведение рутинной биопсии желудка для диагностики атрофического гастрита.
Бессимптомным пациентам с ЖДА и подозрением на целиакию рекомендуется проводить предварительное серологическое тестирование с последующей биопсией тонкой кишки, только если результаты серологического теста положительные. В рекомендациях отмечается, что целиакия относится к общепризнанным причинам развития ЖДА и вероятность ее наличия, даже у бессимптомных пациентов, необходимо рассматривать при проведении дифференциальной диагностики.
В заключение эксперты Американской гастроэнтерологической ассоциации отмечают, что у всех пациентов с ДЖ без явного этиологического фактора в первую очередь необходимо рассматривать вероятные желудочно-кишечные причины.
6) Не рекомендуется проводить исследования костного мозга для подтверждения диагноза ЖДА за исключением отдельных случаев
Необходимость в проведении пункции (получение цитологического препарата костного мозга путем пункции) и трепанобиопсии (получение гистологического препарата костного мозга) может возникнуть в случаях упорной, резистентной к лечению анемии и/или при наличии других цитопений (лейко- или тромбоцитопении) и подозрении на гемобластоз. При ЖДА в костном мозге какие-либо патологические признаки не определяются, клеточность, как правило, нормальная, может отмечаться умеренная гиперплазия эритроидного ростка. Характерной особенностью костного мозга при ЖДА является уменьшение количества сидеробластов – эритрокариоцитов, содержащих гранулы железа (в норме 20-40%).
Дифференциальный диагноз при железодефицитной анемии
ЖДА необходимо дифференцировать с анемиями, осложняющими течение хронических воспалительных и опухолевых заболеваний («анемия хронических заболеваний»), а также с гипохромными анемиями, протекающими с перегрузкой железом: α- и β-талассемии, порфирии, свинцовая интоксикация.
В клинической практике наиболее часто возникает необходимость проведения дифференциальной диагностики между ЖДА и анемией хронических заболеваний (АХЗ). Различить эти состояния позволяет исследование полной панели параметров метаболизма железа в комплексе с оценкой клинического статуса больного и базовых лабораторных показателей, отражающих функциональную способность печени и почек.
Таблица 1. Дифференциальная диагностика АХЗ, ЖДА и анемии смешанного генеза
|
Показатель |
АХЗ |
ЖДА |
Сочетание АХЗ и ЖДА |
|---|---|---|---|
|
Гемоглобин |
Умеренно снижен |
Снижен |
Снижен |
|
Гипохромия эритроцитов |
Часто |
Всегда |
Возможна |
|
Объем эритроцитов (MCV) |
В норме |
Микроцитоз |
В норме или микроцитоз |
|
Сывороточное железо |
Умеренно снижено |
Снижено |
Снижено |
|
ОЖСС |
Снижена или в норме |
Повышена |
Снижена или нижняя граница нормы |
|
Насыщение трансферрина железом (НТЖ) |
Снижено |
Снижено |
Снижено |
|
Сывороточный ферритин |
В норме или повышен |
Снижен |
В норме |
|
В норме |
Повышен |
В норме или повышен |
|
|
Снижено (<1) |
Повышено (>2) |
Повышено (>2) |
|
|
Уровень провоспалительных цитокинов в сыворотке |
Повышен |
В норме |
Незначительно повышен |
|
Повышен |
Снижен |
Повышен |
|
|
Уровень эритропоэтина |
В норме или незначительно повышен |
Повышен |
Повышен или в норме |
ЖДА в типичном варианте имеет характеристику норморегенераторной (в случае продолжающейся кровопотери - гиперрегенераторной) микроцитарной, гипохромной анемии. При ЖДА наблюдается истощение запасов железа в организме (снижение показателей сывороточного железа, насыщения трансферрина и сывороточного ферритина, компенсаторное повышение эритропоэтина, увеличение ОЖСС).
АХЗ в большинстве случаев носит нормохромный и нормоцитарный характер с низким уровнем ретикулоцитов. При АХЗ показатели сывороточного железа и насыщения трансферрина, как правило, снижены или в норме, а уровень ферритина в сыворотке крови — повышен, ОЖСС в пределах нормы, низкая продукция ЭПО, неадекватная тяжести анемии. Кроме того, при АХЗ наблюдается более выраженная активация иммунной системы (повышение уровня гепсидина, ИЛ-6, ИФН-γ/-α, ФНО-α, sICAM-1 и лактоферрина).
Гепсидин (тест 01.02.15.1670) используется для дифференциальной диагностики абсолютного (ЖДА) и функционального (АХЗ) дефицита железа. При ЖДА уровень гепцидина снижен, при АХЗ – повышен.
Растворимый рецептор трансферрина (sTfR) (тест 01.02.15.940) и индекс растворимый рецептор трансферрина/ферритин (sTfR/log Fer) (тест 01.02.15.945) также используются для дифференциальной диагностики ЖДА и АХЗ. При ЖДА оба показателя повышены. При АХЗ sTfR в норме, sTfR/log Fer снижен
При ЖДА имеет место абсолютный дефицит железа, вследствие чего ферротерапия приводит к положительному клинико-гематологическому ответу (активируется эритропоэз, осстанавливаются показатели красной крови). При АХЗ развивается функциональный (относительный) дефицит железа, поэтому на фоне приема препаратов железа внутрь в течение 4 нед. и более должного повышения уровня гемоглобина не отмечается, что требует назначения иной патогенетической терапии.
Дополнительную информацию может предоставить определение лабораторных показателей – концентрации С-реактивного белка (СРБ) и расчетный параметр - Delta-Hе (разница между средним содержанием гемоглобина в ретикулоцитах и средним содержанием гемоглобина в эритроцитах, расчет проводится автоматически в современных гематологических анализаторах). Для АХЗ характерны отрицательные показатели Delta-He и повышенный уровень СРБ.
Определение у пациента этиологии анемии (АХЗ или ЖДА) имеет большое практическое значение, поскольку неправильная трактовка результатов может привести к назначению при АХЗ неэффективной терапии железом, что способно повлечь за собой развитие осложнений в виде перегрузки железом.
Дифференциальная диагностика ЖДА и β-талассемии
Микроцитарная гипохромная анемия является характерным морфологическим признаком β-талассемии, тяжелые формы которой ассоциируются с глубокой анемией и выраженными признаками перегрузки железом (повышенные показатели сывороточного ферритина и НТЖ, сниженные – трансферрина и ОЖСС). Однако легкие субклинические формы талассемии, протекающие с легкой микроцитарной гипохромной анемией, зачастую расцениваются как железодефицитные без исследования сывороточных показателей метаболизма железа, что влечет за собой назначение неадекватной ферротерапии, способной привести к ускоренному развитию тканевой перегрузки железом.
Таблица 2. Показатели метаболизма железа у больных с ЖДА, АХЗ и врожденными анемиями, протекающими с перегрузкой железом
|
Показатель |
ЖДА |
АХЗ |
Перегрузка железом (β-талассемия) |
|---|---|---|---|
|
Сывороточное железо |
↓ |
↓ N |
↑ |
|
ОЖСС |
↑ |
N |
↓ |
|
Трансферрин |
↑ |
↓ N |
↓ |
|
НТЖ |
↓ |
↓ N |
↑ |
|
Ферритин сыворотки |
↓ |
N ↑ |
↑ |
При подозрении на β-талассемию выполняется электрофорез гемоглобина (тест 01.02.15.1135), затем, при получении данных в пользу β-талассемии – полногенное молекулярно-генетическое исследование при бета-талассемии (ген HBB) (тест 01.02.15.1465).
Лабораторная диагностика на фоне терапии ЖДА
Целью лечения ЖДА является введение железа в количестве, необходимом для нормализации уровня гемоглобина (у женщин 120-140 г/л, у мужчин 130-160 г/л) и восполнения тканевых запасов железа (ферритин сыворотки> 40-60 нг/мл). Для лечения и профилактики используют пероральные препараты двухвалентного железа или пероральные препараты трехвалентного железа.
Эффективность лечения пациентов с ЖДА определяется по динамике клинических и лабораторных показателей. Самочувствие пациентов начинает улучшаться через 5-6 дней после начала ферротерапии, содержание ретикулоцитов повышается через 8-12 дней (ретикулоцитарный криз или ретикулоцитарная реакция – повышение количества ретикулоцитов более, чем на 20-25% от исходного), концентрация гемоглобина возрастает через 2,5-3 недели и нормализуется в большинстве случаев через месяц или позже. По окончании курса лечения препаратами железа необходимо контролировать показатели гемоглобина ежемесячно в течение года для определения необходимости поддерживающей ферротерапии.
Железодефицитная анемия при беременности
Важнейшей по значимости медицинской и социальной проблемой является анемия у беременных, которая, по данным ВОЗ, выявляется у 24–30% женщин в экономически развитых странах и более чем у 50% женщин в странах с низким уровнем экономики.
Во время беременности наблюдается значительное физиологическое увеличение потребности в железе для нормального функционирования плаценты и роста плода. Общее количество железа, необходимое для нормальной беременности, составляет 1000–1200 мг. Чтобы завершить нормальную беременность без развития железодефицита, женщина должна иметь запасы железа в организме при зачатии ≥500 мг, что соответствует концентрации сывороточного ферритина 70–80 мкг/л.
При беременности в организме женщины происходит ряд физиологических изменений, в том числе и со стороны крови. Общий объем плазмы увеличивается примерно на 30-50% от исходного, а глобулярный объем возрастает только на 25%. Повышается потребность в микроэлементах и витаминах, необходимых как для синтеза гемоглобина, так и для обеспечения нормального развития плода и плаценты. При отсутствии адекватного восполнения возрастающих потребностей развивается дефицит микроэлементов, и как следствие, беременность может сопровождаться анемией различной степени выраженности. Обусловлено это множеством факторов: нередко беременность наступает при исходно сниженном гемоглобине, и анемия диагностируется в связи с более тщательным лабораторным контролем беременных женщин. Но наиболее частой причиной является недостаточный запас железа в организме, нередко обусловленный особенностями диеты (вегетарианство), хроническими заболеваниями желудочно-кишечного тракта или длительными обильными менструациями, что в связи с возрастающими потребностями в железе на фоне беременности приводит к развитию анемии. Выявление и коррекция анемии на этапе планирования и ранних сроках беременности играет важную роль в дальнейшем вынашивании беременности.
Для скрининга анемии при первом обращении, на 28-й неделе и 34 неделе беременности, а также в любое время во время беременности, если есть симптомы анемии, выполняется общий анализ крови.
Диагноз анемии при беременности основывается на определении концентрации гемоглобина крови: Hb < 110 г/л в первом и третьем триместрах беременности и Hb < 105 г/л во втором триместре беременности; в послеродовом периоде – Hb < 100 г/л через 24–48 ч после родов.
Также определяют послеродовую анемию (ПРА) как концентрацию Hb < 110 г/л через 1 неделю после родов и концентрацию Hb < 120 г/л через 8 недель после родов. В зависимости от концентрации Hb выделяют следующие степени тяжести анемии:
90-110 г/л – легкая анемия;
70-90 г/л – анемия средней степени тяжести;
менее 70 г/л – тяжелая анемия
Коррекция анемии у беременных играет принципиальную роль для нормального развития плода.
1) Железодефицитная анемия. Клинические рекомендации. 2024 г.
2) Полякова О.А., Клепикова М.В., Литвинова С.Н., Исаакян Ю.А., Остроумова О.Д. Проблема дефицита железа и железодефицитной анемии в общемедицинской практике. Профилактическая медицина. 2022;25(12):127–134.
3) Лукина Е.А., Ледина А.В., Роговская С.И. Железодефицитная анемия: взгляд гематолога и гинеколога. Оптимизируем диагностику и лечебную тактику. РМЖ. Мать и дитя. 2020;3(4):248-253.
4) Мартынов А.И., Лукина Е.А., Малявин А.Г., Остроумова О.Д., Ших Е.В., Клепикова М.В., Телкова С.С., Дубинина А.В. Современный взгляд на лечение дефицита железа и фолиевой кислоты. Профилактическая медицина. 2023;26(7):80–87.
5) Трухан Д.И., Деговцов Е.Н., Никоненко В.А., Самойлов Д.В. Железодефицитная анемия в практике гастроэнтеролога и хирурга: актуальные аспекты диагностики и лечения. Consilium Medicum. 2020; 22 (8): 71–77.
6) Трухан Д.И., Тарасова Л.В. Железодефицитная анемия: актуальные вопросы диагностики, лечения и профилактики. Гинекология. - 2013. - Т. 15. - №5. - C. 95-99.
7) Pasricha SR, Tye-Din J, Muckenthaler MU, Swinkels DW. Iron deficiency. Lancet. 2021 Jan 16;397(10270):233-248. doi: 10.1016/S0140-6736(20)32594-0
8) Fletcher A, Forbes A, Svenson N, Wayne Thomas D; A British Society for Haematology Good Practice Paper. Guideline for the laboratory diagnosis of iron deficiency in adults (excluding pregnancy) and children. Br J Haematol. 2022 Feb;196(3):523-529. doi: 10.1111/bjh.17900