Аполипопротеины (апо) - это белковые составляющие липопротеинов (ЛП). Все липиды являются гидрофобными и нерастворимы в крови, поэтому они транспортируются в составе липопротеинов, в комплексе с белками (аполипопротеинами) и фосфолипидами. Аполипопротеины выполняют структурную функцию, действуют как лиганды для рецепторов ЛП, регулируют образование ЛП, служат активаторами или ингибиторами ферментов, участвующих в метаболизме ЛП. Аполипопротеины могут обладать про-атерогенными и анти-атерогенными свойствами.
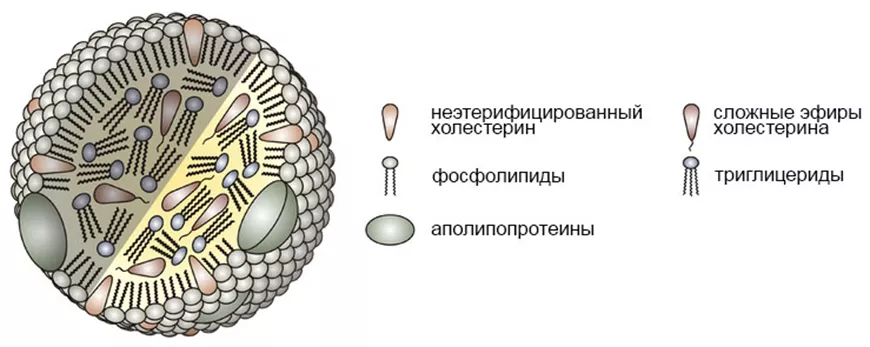
Рис 1. Структура липопротеина
Ниже будут рассмотрены основные классы аполипопротеинов и их функции.Аполипопротеин А-I (апо A-I)
Апо-А1 синтезируется в печени и кишечнике и является основным структурным белком ЛПВП (70% белка ЛПВП), главной антиатерогенной фракции липопротеинов.
Апо-А1 обеспечивает взаимодействие с рецепторами ABCA1, ABCG1 и SR-B1, участвуя в обратном транспорте холестерина из периферических тканей в печень в составе ЛПВП. “Незрелые” ЛПВП частицы поглощают холестерин и фосфолипиды, которые выводятся из клеток (процесс опосредован ABCA1), и формируются “зрелые” ЛПВП. Они могут захватывать дополнительный холестерин через ABCG, SR-B1 и пассивной диффузии.
Апо-А1 является активатором лецитин-холестеринацилтрансферазы (ЛХАТ), фермента, который превращает свободный холестерин в эфиры холестерина, таким образом холестерин выводится из внепеченочных тканей.
Суммируя вышесказанное, можно сказать, что Апо-А1 участвует в механизмах антиатерогенного действия ЛПВП, препятствующих отложению холестерина в атеросклеротических бляшках сосудов. Концентрация Апо-А1 хорошо коррелирует с уровнем ХС ЛПВП. Определение Апо-А1 важно для оценки антиатерогенной активности и определения риска развития сердечно-сосудистых заболеваний.
Высокий уровень Апо-А1 связан со сниженным риском атеросклероза. Снижение концентрации Апо-А1 свидетельствует о повышении вероятности атеросклеротических изменений. Пониженное содержание Апо-А1 ассоциировано с низким уровнем "хорошего" холестерина ЛПВП и замедленным выведением холестерина из сосудов, то есть с увеличением риска развития атеросклероза (особенно если повышен уровень Апо B). Понижение уровня Апо-А1 может быть результатом семейной гиперлипидемии.
Тест 01.02.15.1675. Исследование уровня аполипопротеина (апо-А1)
Повышение коэффициента апо В/апо А1 свидетельствует о повышенном риске развития сердечно-сосудистых заболеваний (риск повышен при соотношении >0,9 у мужчин и >0,8 у женщин).
Тест 01.02.15.1690. Индекс дислипидемии AпoВ/AпoА1
Аполипопротеин А-II (Апо А-II)
Апо А-II синтезируется в печени и является вторым наиболее распространенным белком ЛПВП (20% белка ЛПВП). Активирует печёночную липазу. Аро A-II является предиктором риска сердечно-сосудистых заболеваний.
Аполипопротеин А-IV (апо А-IV)
Основной белок хиломикронов. Минорный белок ЛПВП, обмениваемый между липопротеинами. Синтезируется в печени и кишечнике. Может активировать ЛХАТ. Предполагают, что Аро A-IV может играть в регулировании пищевого поведения.
Аполипопротеин А-V (апо А-V)
Входит в состав ЛП, богатых триглицеридами: хиломикроны, ЛПВП и ЛПОНП. Синтезируется, в основном, в печени. Стимулятор ЛПЛ-зависимого липолиза ТГЦ. Определяет уровень ТГЦ в плазме.
Аполипопротеин B-48 (апо В-48)
Аро В-48 синтезируется в кишечнике и является основным структурным белком хиломикронов и остаточных хиломикронов.
Аполипопротеин B-100 (апо В-100)
Апо В-100 синтезируется в печени и является основным структурным белком ЛПОНП, ЛППП и ЛПНП, т.е. про-атерогенных фракций ЛП. Холестерин, входящий в состав ЛПНП, доставляется к клеткам организма. Если в организме существует избыток холестерина, он откладывается в стенках сосудов в виде атеросклеротических бляшек.
Апо В-100 синтезируется в печени и является основным структурным белком ЛПОНП, ЛППП и ЛПНП, т.е. про-атерогенных фракций ЛП. Апо В-100 является лигандом LDLR. Холестерин, входящий в состав ЛПНП, доставляется к клеткам организма. Если в организме существует избыток холестерина, он откладывается в стенках сосудов в виде атеросклеротических бляшек
Согласно рекомендация ESC/EAS по лечению дислипидемий 2019 г., апо В-100 следует считать альтернативным маркером риска во всех случаях, когда он был определен, особенно у пациентов с высоким уровнем триглицеридов.
Тест 01.02.15.1675. Исследование уровня аполипопротеина В100 (апо-В)Повышение коэффициента апо В / апо А1 свидетельствует о повышенном риске развития сердечно-сосудистых заболеваний (риск повышен при соотношении >0,9 у мужчин и >0,8 у женщин).
Тест 01.02.15.1690. Индекс дислипидемии AпoВ/AпoА1
Мутации гена APOB обуславливают от 5 до 10% случаев семейной гиперхолестеринемии.
Тест 01.02.15.865. Исследование 26-го экзона гена APOB100
Аполипопротеины С (апо С)
Синтезируются в печени. Входят в состав ЛПОНП, ЛПВП, хиломикронов, свободно обменивается между липопротеинами. Апо С-I является активатором ЛХАТ. Является кофактором ЛПЛ и, таким образом, стимулирует гидролиз ТГЦ. Мутации с потерей функции в аpo C-II приводят к выраженной гипертриглицеридемии из-за неспособности метаболизировать ЛП, богатые ТГЦ.
Аполипопротеин (а) - апо (a)
Апо (а) синтезируется в печени. Этот белок является гомологом плазминогена. Он присоединен к апo B-100 через дисульфидную связь. Высокий уровень аро (а) связан с повышенным риском атеросклероза. Аро (а) является ингибитором фибринолиза и может также усиливать поглощение липопротеинов макрофагами, что может увеличить риск атеросклероза. Физиологическая функция аро (а) мало изучена.
Тест 01.02.15.1685. Исследование уровня аполипопротеина Lp(a)
Аполипопротеин Е (апо Е)
Апо Е синтезируется во многих тканях, но печень и кишечник являются основным источником циркулирующего Аро Е. Аро Е входит в состав хиломикронов, остаточных хиломикронов, ЛПОНП, ЛППП и некоторых ЛПВП.
Основная функция АпоЕ – участие в транспорте ХС к тканям в составе ЛП от мест его синтеза или всасывания. Таким образом, данный белок способствует удалению избыточного количества атерогенных ЛПНП и хиломикронов, а также обеспечивает клетки различных тканей холестерином.
Белок АпоЕ не способен проникать через гемато-энцефалический барьер, в связи с чем существуют две его независимые фракции в ЦНС и на периферии. На периферии большая часть циркулирующего АпоЕ продуцируется печенью, в то время как в ЦНС данный белок синтезируется преимущественно клетками микроглии и астроцитами. Роль данного белка в ЦНС заключается в доставке холестерина к нейронам через связывание с рецепторами ЛПНП для поддержания целости клеточной мембраны и синапсов, а также для их восстановления после повреждения.
Было обнаружено, что белок АпоЕ может существовать в трех изоформах – E2,E3,E4, которые обусловлены однонуклеотидным полиморфизмом гена АпоЕ в позициях 112 и 158. У наименее распространенной изоформы, AпoE2 (около 5-10% в популяции), в обеих позициях находится цистеин; АпoE3, в свою очередь, является самой распространенной изоформой (60-70%) и содержит цистеин в 112 позиции, аргинин – в 158. У AпoE4 (15-20%) в обеих упомянутых позициях располагается аргинин. Также описана изоформа АпоЕ1, в 112 позиции которой находится аргинин и в 158 – цистеин, однако данная изоформа (также обозначаемая APOE3r) встречается крайне редко: в литературе описано лишь 4 случая носительства данного аллеля.
Вследствие описанных минорных различий, изоформы белка АпоЕ имеют разную конформацию, а также отличаются уровнем аффинности к своим рецепторам, что определяет возможность их влияния на липидный обмен, а также на развитие атеросклероза и нейродегенеративных заболеваний. Так, например, изоформа АпоЕ2 характеризуется нарушением связывания AпoE с остатками хиломикронов, что приводит к их длительной циркуляции в крови и отложению липопротеинов в тканях и сосудах. Наличие гомозиготного аллеля е2/е2 ассоциировано с гиперлипопротеинемией III типа, которая характеризуется повышением концентрации ОХС, ТГЦ и ЛППП.
Изоформа АпоЕ3 не влияет на риск развития атеросклероза и нейродегенеративных заболеваний – в гомозиготной форме данный аллель встречается у 60% людей в популяции. Кроме того, считается, что наличие данного аллеля предотвращает аккумуляцию Тау-белка, который накапливается в нейронах при болезни Альцгеймера (БА).
Изоформа АпоE4, связываясь преимущественно с ЛПОНП, также приводит к нарушению регуляции рецепторного аппарата липопротеинов. Результатом этого является увеличение количества циркулирующих атерогенных ЛПНП, что повышает риск развития атеросклероза и ССЗ. Однако более значимой является ассоциация аллеля е4 со значительным риском развития БА. Изоформа АпоЕ4 встречается примерно в половине спорадических случаев данного заболевания. Существует так называемый «дозо-зависимый» эффект, который заключается в том, что наличие одной копии аллеля е4 (гетерозиготная форма) повышает риск развития БА примерно в 4 раза, в то время как наличие двух копий е4 (гомозиготная форма) ассоциировано с 8-12-кратным увеличением риска. Кроме того, наличие данной аллели характеризуется более ранним дебютом БА (в среднем, на 12 лет) и быстрой прогрессией заболевания.
На сегодняшний день известно, что изоформа АпоЕ4 ассоциирована с аккумуляцией бета-амилоида, однако точный механизм патогенеза до сих пор не ясен. Считается, что склонность бета-амилоида к агрегации ассоциирована с изоформами АпоЕ в следующей зависимости: АпoE4 > АпoE3 > АпoE2. При этом вклад изоформ в клиренс амилоида определяется в обратной последовательности. Поскольку изоформа АпоЕ2 ассоциирована с наименьшей агрегацией амилоида и лучшим его клиренсом, считается, что наличие аллели е2 обладает протективным эффектом в отношении болезни Альцгеймера.
Тест 01.02.05.250. Генотипирование аллелей E2, E3, E4 гена APOE
Таблица 1. Аполипопротеины и их функции.|
Апо-липопротеин |
Источник |
Входит в состав липопротеинов |
Функция |
|---|---|---|---|
|
Апo A-I |
Печень, кишечник |
ЛВП, хиломикроны |
Основной белок ЛВП. Активатор ЛХАТ |
|
Aпo A-II |
Печень |
ЛВП, хиломикроны |
Минорный белок ЛВП. Активирует печёночную липазу |
|
Aпo A-IV |
Кишечник, печень |
Хиломикроны, ЛВП |
Основной белок хиломикронов. Минорный белок ЛВП. Может активировать ЛХАТ |
|
Aпo A-V |
Печень |
ЛВП, ЛОНП, хиломикроны |
Стимулятор ЛПЛ-опосредованного липолиза ТГЦ |
|
Aпo B-48 |
Кишечник |
Хиломикроны, остаточные хиломикроны |
Основной белок хиломикронов. |
|
Aпo B-100 |
Печень |
ЛНП, ЛОНП, ЛПП, ЛП(а) |
Основной белок ЛНП. Лиганд для LDLR |
|
Aпo C-I |
Печень |
Хиломикроны, ЛОНП, ЛВП |
Активатор ЛХАТ |
|
Aпo C-II |
Печень |
Хиломикроны, ЛОНП, ЛВП |
Активатор внепечёночной ЛПЛ |
|
Aпo C-III |
Печень |
Хиломикроны, ЛОНП, ЛВП |
Ингибитор ЛПЛ и захвата ЛП |
|
Aпo E |
Печень, кишечник, другие ткани |
Хиломикроны, остаточные хиломикроны, ЛПП, ЛВП |
Лиганд для LDLR |
|
Aпo (a) |
Печень |
ЛП (а) |
Ингибирует активацию плазминогена |
1) Обзор метаболизма липидов. MSD Manual
2) Feingold KR. Introduction to Lipids and Lipoproteins. [Updated 2021 Jan 19]. In: Feingold KR, Anawalt B, Blackman MR, et al., editors. Endotext [Internet]. South Dartmouth (MA): MDText.com, Inc.; 2000-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK305896/
3) Sniderman AD, Thanassoulis G, Glavinovic T, Navar AM, Pencina M, Catapano A, Ference BA. Apolipoprotein B Particles and Cardiovascular Disease: A Narrative Review. JAMA Cardiol. 2019 Dec 1;4(12):1287-1295. doi: 10.1001/jamacardio.2019.3780
4) Husain MA, Laurent B, Plourde M. APOE and Alzheimer's Disease: From Lipid Transport to Physiopathology and Therapeutics. Front Neurosci. 2021 Feb 17;15:630502. doi: 10.3389/fnins.2021.630502