- Рекомендовано всем пациентам с меланомой кожи резектабельной и нерезектабельной III стадии и IV стадий для определения показаний к назначению комбинированной таргетной терапии тирозинкиназными ингибиторами BRAF/MEK;
- Рекомендовано всем пациентам с метастатическим колоректальным раком для определения возможности применения анти-EGFR антител;
- Рекомендовано всем пациентам с метастатическим колоректальным раком для определения показаний к добавлению к системной терапии тирозинкиназного ингибитора BRAF;
- Рекомендовано всем пациентам с метастатическим немелкоклеточным раком легкого для определения показаний к назначению комбинированной таргетной терапии тирозинкиназными ингибиторами BRAF/MEK;
- Рекомендовано всем пациентам с верифицированным раком щитовидной железы для послеоперационной стратификации риска рецидива для определения послеоперационной тактики ведения пациентов.
BRAF представляет собой протеинкиназу, которая играет важную роль в сигнальном пути RAS-RAF-MEK-ERK (MAPK). Большинство мутаций BRAF приводит к его конститутивной активации и вследствие этого - стимуляции клеточного деления и роста, ингибированию апоптоза и неопластической трансформации.
V600E - наиболее частая мутация BRAF (90%), она представляет собой замену валина на глутаминовую кислоту в позиции 600 в киназном домене. Эта замена имитирует фосфорилирование, тем самым индуцируя конститутивную активность протеинкиназы BRAF.
BRAF-мутации выявляются при меланоме, раке щитовидной железы, колоректальном раке, немелкоклеточном раке легкого и некоторых других новообразованиях. Идентификация мутации V600E в гене BRAF при данных видах метастатических злокачественных опухолей служит показанием к назначению конкурентных ингибиторов BRAF в виде монотерапии либо в комбинации с ингибиторами MEK.
Частота мутаций в гене BRAF при меланоме кожи (МК), по данным разных исследователей, варьирует от 50% до 80%. Наиболее частой (69-94% случаев) мутаций является V600E.
Мутация BRAF V600E представляет собой наиболее частую аберрацию, обнаруживаемую при папиллярном раке щитовидной железы (40-50 % случаев). Также данная мутация встречается в 20-40 % случаев низкодифференцированных карцином и 30-40 % случаев анапластических карцином. Определение мутации BRAF V600E рекомендовано всем пациентам с высокодифференцированным раком щитовидной железы для послеоперационной стратификации риска рецидива в целях определения тактики ведения пациентов.
У 8-12% пациентов с метастатическим колоректальным раком выявляется мутация BRAF V600E, она ассоциирована с плохим ответом на стандартную химиотерапию и низкой общей выживаемостью. Примерно у 30% пациентов с мутацией BRAF V600E также выявляется микросателлитная нестабильность (MSI).
Наличие мутации V600E в гене BRAF – предиктор ответа на комбинированную таргетную терапию тирозинкиназными ингибиторами BRAF/MEK у пациентов с меланомой кожи резектабельной и нерезектабельной III стадии и IV стадий, у пациентов с метастатическим немелкоклеточным раком легкого, у пациентов с метастатическим раком щитовидной железы и метсастатическим колоректальным раком. У пациентов с колоректальным раком монотерапия ингибиторами BRAF, как правило, неэффективна. Однако, исследование III фазы BEACON подтвердило эффективность комбинации ингибиторов BRAF с ингибиторами EGFR.
Также необходимо напомнить, что V600E является частой, но далеко не единственной мутацией в гене BRAF. 22–30% мутаций в гене BRAF при колоректальном раке не являются V600E мутациями. 50–80% мутаций в гене BRAF при немелкоклеточном раке легкого не являются V600E мутациями.
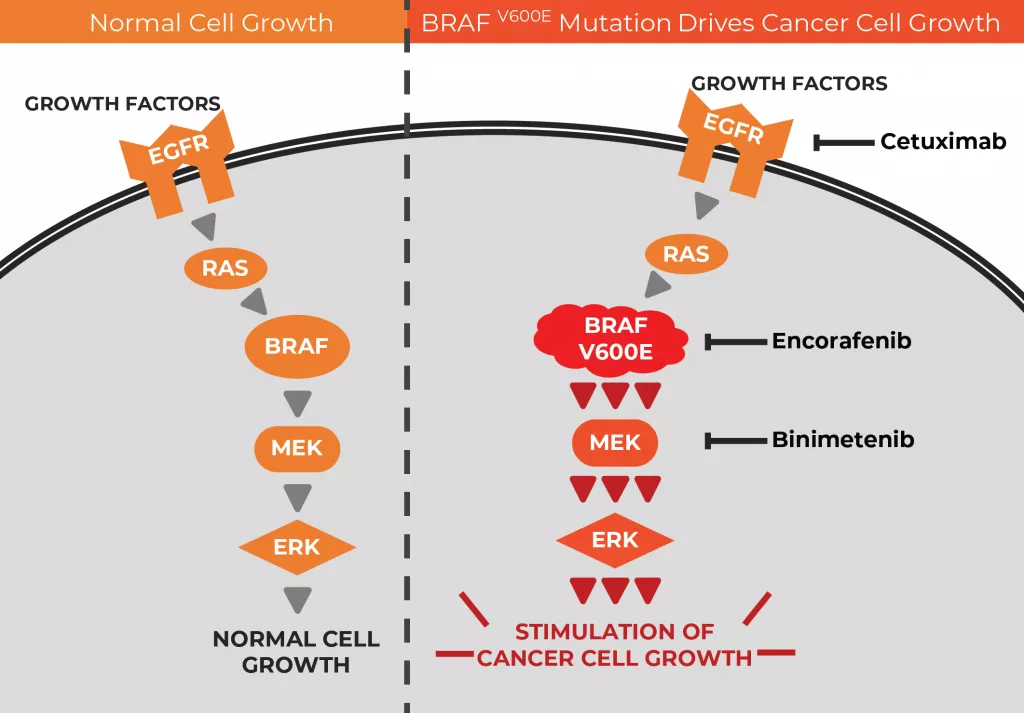
Рис 1. Сигнальный путь RAS-RAF-MEK-ERK в норме (слева) и при паталогической активации за счет мутации BRAF V600E (справа). Справа также изображены препараты для таргетной терапии и их мишени.
1) Меланома кожи и слизистых оболочек. Рекомендации МЗ РФ (взрослые). 2025 г.
2) Дифференцированный рак щитовидной железы. Рекомендации МЗ РФ (взрослые). 2024 г.
3) Злокачественное новообразование бронхов и легкого. Рекомендации МЗ РФ (взрослые). 2022 г.
4) Dankner M, Rose AAN, Rajkumar S, Siegel PM, Watson IR. Classifying BRAF alterations in cancer: new rational therapeutic strategies for actionable mutations. Oncogene. 2018 Jun;37(24):3183-3199. doi: 10.1038/s41388-018-0171-x
5) Zaman, Aubhishek et al. Targeting Oncogenic BRAF: Past, Present, and Future. Cancers vol. 11,8 1197. 16 Aug. 2019, doi: 10.3390/cancers11081197
6) Tabernero J, Ros J, Élez E. The Evolving Treatment Landscape in BRAF-V600E-Mutated Metastatic Colorectal Cancer. Am Soc Clin Oncol Educ Book. 2022 Apr;42:1-10. doi: 10.1200/EDBK_349561
7) Мусаелян А.А., Лапин С.В., Назаров В.Д., Козорезова Е.С., Воробьев С.Л., Орлов С.В. Диагностическая и прогностическая значимость выявления мутаций в генах BRAF, TERT, RAS и транслокаций RET/PTC и PAX8/PPARG в материале тонкоигольной аспирационной биопсии узлов щитовидной железы IV цитологической категории (Bethesda, 2017). Опухоли головы и шеи. 2022;12(2):71-78.
8) Оганян К.А., Мусаелян А.А., Котикова М.А., Лапин С.В., Назаров В.Д., Беляев М.А., Захаренко А.А., Орлов С.В. Молекулярно-генетическая характеристика колоректального рака в зависимости от статуса микросателлитной нестабильности. Медицинский Совет. 2022;(9):139-146.
