Исследование мутаций в генах EGFR, RAS, BRAF, ALK, ROS1 для назначения таргетной терапии онкологических заболеваний
Роль генетических мутаций в назначении таргетной терапии
Активное изучение молекулярно-генетических основ туморогенеза привело к обнаружению ряда клональных драйверных мутаций генов вторичных посредников, определяющих появление и развитие опухолевого процесса.
На данный момент разработаны ряд высоко-активных препаратов, которые таргетно ингибируют белок, мутации гена которого являются главной причиной развития злокачественного процесса в рассматриваемой опухоли.

Рисунок 1. Таргетные препараты
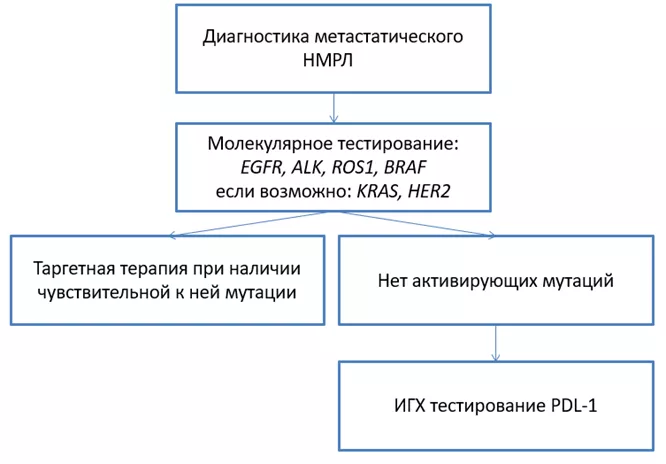
Мутации EGFR и HER2 при немелкоклеточном раке легкого (НМРЛ)
Идентификация активирующих мутаций в гене рецептора эпидермального фактора роста (EGFR) привела к разработке и клиническому использованию новых «таргетных» препаратов, специфически ингибирующих повышенную тирозинкиназную активность мутантных белковых молекул.
Активирующие мутации в гене EGFR встречаются приблизительно у 10-15% пациентов немелкоклеточным раком легкого (НМРЛ) в Европе и особенно распространены в азиатской популяции, где данные аберрации обнаруживаются до 62% случаев НМРЛ. EGFR-положительным пациентам могут быть назначены препараты, направленные тирозинкиназный домен данного рецептора, такие как эрлотиниб, гефитиниб, афатиниб и осимертиниб. Данные препараты значительно улучшают течение заболевания. Например, в клиническом исследовании OPTIMAL было показано, что у китайских пациентов метастатическим НМРЛ с наличием активирующих мутаций в гене EGFR, принимавших эрлотиниб, выживаемость без прогрессии составила 13.1 месяцев. Для сравнения: данный показатель у пациентов, принимавших комбинацию гемцитабина и карбоплатина, составил 4.6 месяцев. Эрлотиниб также одобрен для лечения пациентов раком поджелудочной железы, хотя в этой ситуации использование данного агента не зависит от наличия активирующей мутации в гене EGFR. Так, в исследовании III фазы, в котором проводилось сравнение применения комбинации эрлотиниба и гемцитабина и монотерапии гемцитабином, было показано, что добавление в терапию эрлотиниба привело к небольшому, но статистически значимому, увеличению медианы общей выживаемости примерно на 2 недели (HR 0.82; P = 0.038). Более недавнее рандомизированное исследование, проведенное в Тайване, показало, что медиана общей выживаемости составила 7.2 месяца у пациентов, принимавших данную комбинации против 4.4 месяцев у пациентов, принимавших монотерапию гемцитабином.
Ген рецептора человеческого эпидермального фактора роста 2 (HER2/ERBB2) кодирует мембранный рецептор с тирозинкиназной активностью, являющийся одним из членов семейства рецепторов ERBB. В отличие от других белков данного семейства, HER2/ERBB2 не связывает лиганд напрямую, но образует гетеродимеры с другими лигандассоциированными рецепторами данного семейства. Активация ведет к индуцированию ряда сигнальных путей, таких как PI3K, MAPK и JAK/STAT. Активация HER2 обнаруживают в небольшой доле всех случаев рака легкого в связи с гиперэкспрессией в 20%, амплификацией гена в 2% и активирующих мутации в 1,6-4% НМРЛ. К активирующим мутациям гена HER2 относят инсерции в 20 экзоне размером 3-12 нуклеотидов. С использованием in vivo моделей было показано, что активирующие мутации в трансгенных мышиных моделях вызывают развитие множественных аденокарцином. Генетические аберрации в HER2 в основном встречаются при аденокарциноме легкого, которые не имеют аберраций в генах EGFR и KRAS.
Колоректальный рак: влияние мутаций KRAS на анти-EGFR терапию
EGFR также является терапевтической мишенью для антител, которые используются у пациентов с колоректальным раком (КРР) (панитумумаб и цетуксимаб) и опухолями головы и шеи (цетуксимаб). У этих пациентов наличие активирующей мутации в гене EGFR не является показанием для назначения анти-EGFR терапии, и устойчивость обычно не опосредуется мутациями в гене EGFR. Однако, предсуществующие активирующие мутации в гене KRAS, которые кодируют ГТФ-азу, опосредующую активацию нижележащих компонентов сигнального пути от EGFR, являются распространенным событием у пациентов КРР. Данные мутации способствуют функциональному ускользанию от блокирующего действия анти-EGFR антител, что приводит к резистентности к данным препаратам. Поэтому анти-EGFR терапия панитумумабом и цетуксимабом показана пациентам КРР только с отсутствием мутаций в гене KRAS. Наличие мутаций в гене KRAS также ассоциирована с отсутствием ответа на ТКИ EGFR у пациентов НМРЛ, хотя рутинное тестирование на данные мутации не применяется для решения вопроса о назначении таргетной терапии. Как и при тестировании мутаций в гене EGFR у пациентов НМРЛ, клиническая польза от обнаружения мутаций в гене KRAS в значительной степени зависит от чувствительности используемого метода. У пациентов КРР, которые имели дикий тип гена KRAS до проведения терапии, применение анти-EGFR антител, как считается, приводит к появлению мутаций в данном гене.
В последующем, список активирующих мутаций при раке легкого был значительно расширен: мутации были обнаружены в генах HER2 (также известный как ERBB2), рецептор фактора роста фибробластов 1 (FGFR1) и FGFR2, а также онкогенах анапластической лимфомакиназы (ALK), тирозинкиназы рецептора ROS1, нейрегулина 1 (NRG1), рецептора нейротрофической тирозинкиназы типа 1 (NTRK1) и RET.

Биологическая роль генов семейства RAS (в том числе KRAS)
KRAS представляет собой протоонкоген из семейства белков RAS и кодирует G-белок, активно участвующей в регуляции и контроле клеточной пролиферации, дифференцировки и выживании. Белок Ras неактивен в нормальных не пролиферирующих клетках, но вступает в работу при связывании с гуанозинтрифосфатом, что приводит к реактивации рецепторов факторов роста. Активированные комплекс Ras-ГТФ связывается и активирует ряд вторичных посредников передачи клеточного сигнала, такие как митоген активирующую протеин киназу (MAPK), белки путей RAS/RAF/MEK/MAPK и PI3K/AKT/mTOR. KRAS играет основную роль в контроле передачи сигнала от ряда основных рецепторов факторов роста, в том числе EGFR. Активирующие мутации в гене KRAS изменяют ГТФ-азную активность белка и блокируют возможность его деактивации, что ведет к гиперактивации ряда внутриклеточных путей передачи сигнала, контролирующих рост и пролиферацию клеток. Мутации в RAS/RAF/MEK/MAPK-сигнальном пути играют важную роль в развитии рака легкого, колоректального рака, рака щитовидной железы, меланомы.
Особенности мутаций KRAS при аденокарциноме легкого
Мутации в RAS/RAF/MEK/MAPK-сигнальном пути играют основную роль в развитии рака легкого. Как минимум, одна активирующая мутация была обнаружена в генах данного сигнального пути в 132 из 188 образцов опухолевого материала рака легкого. Чаще всего аберрации наблюдались в гене KRAS. Активирующие мутации в онкогене KRAS представляют собой наиболее частую генетическую аберрацию при аденокарциноме легкого, встречающуюся в 25-40% случаев, в то время как мутации в генах HRAS и NRAS встречаются намного реже. Высокая вариация распространённости мутаций в гене KRAS связана с этническими, половыми различиями, а также факторами влияния внешней среды исследуемых выборок пациентов. Так, мутации в данном гене более распространены в европейской популяции, чем у пациентов из Азии. У пациентов с аденокарциномой легкого, которые никогда не курили, распространённость аберраций в гене KRAS составила 0-15% [46]. Кроме этого, мутации в данном гене редко встречают при мелкоклеточном раке легкого (в одном случае из 188). Самой частой мутацией в гене KRAS при аденокарциноме лёгкого является аминокислотная замена в 12 кодоне, реже встречаются мутации в кодоне 13 и 61. Учитывая, что аберрации в гене KRAS представляют собой драйверные мутации, они редко встречаются совместно с изменениями в гене EGFR. Было показано, что пациенты с KRAS-ассоциированным раком легкого резистентны к терапии ингибиторами EGFR тирозинкиназы, так как мутации в гене KRAS ведет к активации вторичных посредников, находящихся выше в цепочке сигнального пути, чем белки гена EGFR. Существуют данные о том, что различные генетические аберрации в гене KRAS имеют разное клиническое значение. В соответствии с исследованием BATTLE (Biomarker-integrated Approaches of Targeted Therapy for Lung cancer Elimination), генетические изменения G12C и G12V в гене KRAS предсказывают более быстрое прогрессирование заболевания у пациентов по сравнению с другими типами KRAS-мутаций или отсутствием генетических изменений в этом гене. Более того, различные мутации ведут к активации различных путей передачи сигнала (PI3-K и MEK при Gly12Asp и Ral при Gly12Cys или Gly12Val), что объясняется разницей в конформации мутантного белка и, как следствие, разницей специфичности к нижестоящим медиаторам передачи сигнала. Это еще раз подчеркивает важность учета генетической составляющей рака легкого при разработке новых таргетных лекарственных средств.
Меланома: мутация V600E в гене BRAF и таргетная терапия
Активирующая мутация V600Е в гене BRAF обнаруживается приблизительно у 50% пациентов метастатической меланомой и определяет чувствительность к терапии BRAF ингибиторами, такими как вемурафениб и дабрафениб. Известно, что большинство V600E-позитивных опухолей отвечают на BRAF-ингибитор вемурафениб, однако на животной модели было продемонстрировано парадоксальное увеличение активности сигнального пути MAPK и, как следствие, клеточного роста при наличии мутаций в гене HRAS. Кроме того, у пациентов, получающих монотерапию вемурафениба, часто развивается плоскоклеточный рак кожи и кератоакантома. Данный феномен может быть результатом стимуляции роста клеток кожи, имеющих мутации в генах семейства RAS. Комбинированная терапия с MEK ингибитором, таким как траметиниб, который одобрен для лечения V600E-позитивной меланомы также и в качестве монотерапии, позволяет устранить стимулирующий эффект роста RAS-позитивных клеток, что препятствует появлению вторичных новообразований кожи у пациентов с имеющейся меланомой. Более того, результаты исследования III фазы продемонстрировали высокую выживаемость при двойном BRAF–MEK ингибировании: медиана общей выживаемости при использовании комбинированной терапии составил 25.1 месяцев, а при монотерапии BRAF ингибиторами 18.7 месяцев. Также в данном исследовании показан более низкий риск появления плоскоклеточной карциномы кожи и кератоакантомы при применении комбинированной терапии: 1% в группе пациентов с использованием комбинации против 18% в группе пациентов с монотерапией BRAF-ингибитором. К сожалению, примерно у 30% пациентов при применении комбинированной терапии BRAF/MEK ингибиторами наблюдается прогрессирование заболевания в первые 6 месяцев. В работе Girotti M B et al. было показано, что у 9 из 10 пациентов, у которых развилась быстрая прогрессия заболевания при использовании комбинированной терапии, обнаружены дополнительные мутации в компонентах сигнального пути MAPK. Наиболее частыми были амплификация BRAF и активирующие мутации в генах NRAS либо MEK2. Эти аберрации не были обнаружены в опухолевом материале, взятом до проведения терапии, но в данном исследовании не использовались высокочувствительные методы. В настоящее время в разработке находятся альтернативные ингибиторы семейства RAF, которые позволят преодолеть данные механизмы резистентности. Таким образом, раннее выявление субклональных активирующих мутаций в генах NRA NRAS и MEK2 позволит стратифицировать пациентов по наибольшей пользе от применения этих ингибиторов.
Перестройки генов ALK и ROS1 при раке легкого
Реорганизация гена ALK, чаще всего характеризующееся слиянием внутриклеточного киназного домена белка ALK с терминальным концом эхинодермального микротубулярного белка 4 (EML4), наблюдается при некоторых случаях рака легких. Данная аберрация возникают в результате короткой инверсии на хромосоме 2р, когда 13 интрон гена EML4 сливается с 19 интроном гена ALK. Описано большое количество различных вариантов EML4-ALK слияния. Одним из самых распространенных вариантов является слияние экзонов 1-13 гена EML4 с экзонами 20-29 гена ALK. Кроме этого, было обнаружено, что ген ALK дополнительно может сливаться с такими генами, как KIF5B, TFG и KLC-1.
Онкогенный белок слияния EML4-ALK имеет конституционально активированный киназный домен. С использованием экспериментальных моделей было доказано, что слияния генов EML4-ALK вызывает развитие множественных аденокарцином легкого у мышей. Активация ALK ведет к повышенной пролиферации клеток и ингибированию апоптоза, которые регулируются сигнальными путями RAS/RAF/MAPK1, PI3K/AKT и JAK3-STAT3. Мутации в гене ALK обнаруживаются в 4% случаев НМРЛ, чаще всего у молодых пациентов без курения в анамнезе и с аденокарциномой. В то время как мутации ALK исключают возможные аберрации в EGFR и KRAS генах, были описаны случаи компаудных мутаций, что приводило к резистентности проводимой терапии ингибиторами тирозинкиназ. Пациенты с EML4-ALK мутацией имеют хороший ответ на проводимую терапию кризотинибом, но при наличии точечных мутаций в ALK гене или сопутствующей активирующей аберрации EGFR гена, ответ на терапии резко снижается.
Роль протоонкогена ROS1
ROS1 представляет собой протоонкоген, располагающийся на 6q22 хромосоме и кодирующий трансмембранный белок рецептор тирозинкиназы, который имеют высокую гомологию с ALK1. Мутации гена ROS1 ведут к гиперактивации сигнальных путей PI3K/AKT/mTOR, STAT3 и RAS/MAPK/ERK. В 2007 году было обнаружено, что при НМРЛ происходит слияние гена ROS1 с генами SLC34A2 и CD74. Позднее было описано KDELR2-ROS1 слияние при аденокарциноме легкого. В 2-х объемных исследованиях с использованием FISH, ROS1- мутации были обнаружены в 18 случаях из 694 аденокарциномы легкого (2.6%) и в 13 из 1116 случаев аденокарциномы легкого (1.2%). На данный момент обнаружены следующие гены, с которым происходит слияние гена ROS1: FIG, KDELR2, TPM3, SDC4, LRIG3, EZR, SLC34A2 и CD74. Не совсем ясно, какую роль играют данные гены в патогенезе рака легкого. Мутации в гене ROS1 наблюдаются чаще у молодых некурильщиков азиатской расы. Более того, у пациентов с ROS1-ассоциированным раком легкого показана чувствительность к ингибиторам тирозинкиназ, в том числе кризотинибу.
Рак щитовидной железы: молекулярно-генетический профиль
Большинство мутаций при раке щитовидной железы (РЩЖ) возникает в генах, кодирующих белки MAPK-киназного и PI3K–AKT путей. MAPK-протеинкиназы — сборная группа белков, включающая три семейства протеинкиназ — p38, JNK/SAPK (c-Jun N-terminalkinase/ Stress-activatedproteinkinase) и ERK (extracellularsignal-regulatedkinase). Практически во всех случаях активация протеинкиназ (ПК) семейства ERK связана с клеточным выживанием и стимуляцией пролиферации, а активация ПК семейства p38 и JNK с индукцией апоптоза. Поскольку в ответ на различные клеточные стимулы в клетках должна меняться экспрессия тех или иных генов, основными мишенями MAPK-протеинкиназ являются траскрипционные факторы [Rousset B. etal., 2011]. Несмотря на то, что транскрипционные факторы, локализованные в ядре, являются важными субстратами MAPK, только часть активированных в цитоплазме MAPK транслоцируется в ядро. Немалая часть MAPK остается в цитоплазме и других субклеточных компартментах, где роль этих ПК изучена гораздо меньше. Известно, что MAPK могут регулировать экспрессию генов и на посттранскрипционном уровне, используя в качестве субстратов цитоплазматические белки. Активация MAPK является одним из самых важных этапов канцерогенеза РЩЖ. Гены, аберрации в которых обнаруживаются при РЩЖ, кодируют тирозинкиназные трансмембранные белки RET, NTRK1, а также внутриклеточные вторичные посредники сигнала BRAF и KRAS. Аберрации в данных генах являются взаимоисключающими и обнаруживаются в 70% случаев папиллярной карциномы и ассоциированы с характерными гистопатологическими и биологическими характеристиками. Гистологически BRAF-ассоциированный РЩЖ представлен высококлеточным (ВПРЩЖ) и классическим (КПРЩЖ) вариантами папиллярного рака, экстратиреоидным распространением, склонностью к дедифференцировке. В то же время RAS-ассоциированный рак характеризуется фолликулярным вариантом ПРЩЖ (ФВПРЩЖ) и частой инкапсуляцией.
Транслокации генов RET/PTC и NTRK1
Транслокация RET/PTC встречается в основном при папиллярном РЩЖ. В результате транслокации ген RET сливается с рядом других генов. Получающиеся химерные конструкции включают в себя часть гена RET, кодирующего тирозинкиназный домен рецептора RET, и активный промотор другого гена, который осуществляет экспрессию и лиганд-независимую димеризацию протеинового комплекса RET/PTC. Данная химерная конструкция ведет к постоянной стимуляции MAPK сигнального пути и злокачественного перерождения клеток. Наиболее частыми перестройками являются RET/PTC1 и RET/PTC3, в которых RET соединён с CCDC6 (H4) и NCOA4 (ELE1 или RFG) соответственно. Обе перестройки представляют собой парацентрические, интрахромосомные инверсии, так как все гены, образующие структуру, находятся на одной и той же 10 хромосоме. С другой стороны, RET/PTC2 и 9 других ранее описанных RET/PTC перестроек представляют собой интерхромосомные конструкции, формирующиеся при слиянии части гена RET с генами, расположенными на других хромосомах. Распространенность и специфичность RET/PTC перестройки при папиллярном РЩЖ варьирует в различных исследованиях. Частично, данные вариации объясняются реальной разницей распространённости описанной аберрации в различных возрастных группах и наличием пациентов, перенесших ионизирующее облучение. Кроме этого, гетерогенность объясняется неравномерным распределением мутации в опухоли и различающейся чувствительностью используемых методик. В некоторых случаях перестройка RET/PTC является клональной и обнаруживается в большинстве клеток опухоли. Также, аберрация RET/PTC может быть неклональной и обнаруживаться только в небольшом количестве клеток высокочувствительными методами ДНК-диагностики. Клональная RET/PTC-перестройка обнаруживается в 10-20% случаев папиллярного рака и является специфическим маркером данного типа РЩЖ. В то же время, неклональная перестройка RET/PTC обнаруживается намного чаще как при папиллярном раке, так и в других типах РЩЖ и доброкачественных образованиях (до 10-45% доброкачественных узлов и образований имели неклональную мутацию RET/PTC). Другая хромосомная перестройка, встречающаяся при папиллярном РЩЖ, затрагивает ген NTRK1, но встречается намного реже, чем перестройка RET/PTC. Ген NTRK1 располагается на хромосоме 1q22 и может сливаться, как минимум, с тремя различными генами, располагающимися на той же или других хромосомах. Перестройка NTRK1, также известная как TRK-перестройка, наблюдалась в 10-15% случаев папиллярного РЩЖ в одном из исследований, хотя, вероятнее всего, распространенность данной аберрации не превышает 5%.
Значение мутаций RAS и BRAF при раке щитовидной железы
Гены HRAS, KRAS, NRAS кодируют G-белки, располагающиеся на внутренней части клеточной мембраны и переносящие сигналы, возникающие с мембранных тирозинкиназных рецепторов и G-связанных рецепторов по сигнальным путям MAPK и PI3K–AKT. Активирующие мутации в генах RAS чаще всего находятся в 12, 13 и 61 кодонах. При РЩЖ мутации в кодонах 61 генов NRAS и HRAS встречаются чаще всего. Мутации в RAS-генах обнаруживаются в 10-20% случаев ПРЩЖ, 40-50% случаев ФРЩЖ и 20-40% случаев НДРЩЖ и АРЩЖ. Среди ПРЩЖ, практически все RAS-ассоциированные опухоли формируют неопластические фолликулы без папиллярных структур и, таким образом, диагностируются как ФВПРЩЖ. Мутации в RAS-генах встречаются в 20-40% доброкачественных фолликулярных аденомах. Обнаружение мутаций в RAS-генах в доброкачественных аденомах говорит о том, что RAS-положительные фолликулярные аденомы могут служить прекурсорами для RAS-положительных фолликулярных карцином и ФВПРЩЖ. Более того, RAS-мутации предрасполагают высокодифференцированный рак трансформироваться в анапластические образования. При РЩЖ BRAF активируется точечными мутациями, малыми делециями или инсерциями и хромосомными перестройками. Наиболее частым механизмом активации является замена тимина на аденин в нуклеотидной позиции 1799, что приводит к замене валина на глутамин в позиции 600 транслируемого белка (Val600Glu). Данная аберрация встречается в 98-99% процентов всех мутаций, выявляемых в гене BRAF при РЩЖ. Другими менее распространенными генетическими изменениями являются Lys601Glu-замена, инсерции и делеции около кодона 600, а также AKAP9/BRAFперестройка. AKAP9/BRAF-перестройка представляет собой парацентрическую инверсию хромосомы 7q, что ведет к слиянию части BRAF-гена, кодирующей протеинкиназный домен и AKAP9-ген. Все точечные мутации и перестройки ведут к активации BRAF-киназы и хронической стимуляции MAPK-пути. Мутация BRAF Val600Glu представляет собой наиболее частую аберрацию, обнаруживаемую при папиллярном РЩЖ (40-50% случаев). Также данная мутация встречается в 20-40% случаев НДРЩЖ и 30-40% случаев АРЩЖ. Гистологически во многих случаях BRAF-ассоциированных карцином обнаруживаются области высокодифференцированного папиллярного рака, и BRAF-положительные клеточные линии присутствуют во всех областях опухоли, что говорит о том, что появление Val600Glu является ранним событием и предрасполагает к дедифференцировке опухоли. При папиллярном РЩЖ BRAF Val600Glu-мутация обнаруживается чаще всего в двух вариантах ПРЩЖ: классическом и высококлеточном. В то же время, BRAF Val601Glu гистологически может быть представлена фолликулярным вариантом.
Перестройка PAX8/PPARγ при фолликулярном раке
PPARγ представляет собой ядерный рецептор, участвующий в регуляции клеточного цикла и апоптоза. PAX8, в свою очередь, является фактором транскрипции, регулирующим активность тиреоидо-специфических генов. PAX8/PPARγ перестройка наблюдается при слиянии части гена PAX8, который кодирует фактор транскрипции и гена PPARγ. Образование данной конструкции ведет к сильной гиперэкспрессии химерного PAX8/PPARγ белка. Аберрация PAX8/PPARγ представляет собой прототипную мутацию, обнаруживаемую при фолликулярном РЩЖ, где она возникает в 30-35% случаев. Данная перестройка редко встречается при фолликулярных аденомах (2-13%) и ФВПРЩЖ (1-5%). Мутация PAX8/PPARγ ассоциируется с развитием фолликулярной карциномы в раннем возрасте и высоким уровнем сосудистой инвазии. С точки зрения клинической значимости, обнаружение мутации PAX8/PPARγ говорит о фолликулярной структуре опухоли с предрасположенностью к ранней сосудистой инвазии, но в то же время данная аберрация может встречаться и в доброкачественных образованиях. Несмотря на это, обнаружение перестройки PAX8/PPARγ при фолликулярной неоплазии предсказывает конверсию доброкачественного образования в рак.
Влияние радиации и факторов внешней среды на мутагенез
Существует строгая корреляция между хромосомными соматическими аномалиями, характерными для ПРЩЖ, и случаями облучения ионизирующим излучением. Перестройка RET/PTC обнаруживается у 80% пациентов с ПРЩЖ, которые ранее подверглись воздействию радиации в терапевтических целях или случайно. Чернобыльская катастрофа значительно увеличила частоту возникновения RET/PTC3 и нового RET/PTC-ассоциированного РЩЖ. Перестройка BRAF/AKAP9 также чаще всего встречается у пациентов с ПРЩЖ, подвергнувшихся радиационному облучению. Нужно отметить, что точечные мутации в генах BRAF и KRAS редко встречаются в случаях РЩЖ, индуцированных излучением. Хотя точные механизмы формирования хромосомных перестроек при радиационном излучении не до конца понятны, считается, что ядерная и хромосомная архитектура вносят существенный вклад в перестройки RET/PTC и TRK, располагая склонные к рекомбинации участки генома в непосредственной близости друг к другу. Пространственная близость предрасполагает соседние гены к неверному ресоединению двуцепочечных разрывов, вызванных радиацией. Дополнительно, индуцирование RET/PTC-перестройки может быть ассоциировано с хромосомной ломкостью. Регионы 10q11.2 и 10q21 расположения генов RET и CCDC6 соответственно, а также их партнеров при перестройках RET/PTC1, содержат два сайта ломкости: FRA10G и FRA10C. На культуре клеток было показано, что индукция ломкости в этих сайтах вызывало появление перестроек RET/PTC1. Хромосомная ломкость может вызываться или усиливаться гипоксией, этанолом, кофеином и другими эндогенными и экзогенными факторами. Таким образом, перестройка RET/PTC1 может вызываться и другими, помимо радиации, факторами. Данный мультифакториальный механизм, вероятнее всего, характерен для молодых пациентов с ПРЩЖ. В отличие от хромосомных перестроек, появление точечных соматических мутаций при РЩЖ чаще всего не связано с воздействием радиации. В китайском исследовании с выборкой более 1000 случаев ПРЩЖ было показано, что появление BRAFVal600Glu-мутаций ассоциировано с высоким уровнем потребления йода (OR=1,97). Результаты данного исследования не позволяют подтвердить причинно-следственную связь между высоким потреблением йода и мутагенезом. Но в случае подтверждения, эти данные дадут биологический базис для понимания причин повышенной распространённости ПРЩЖ по сравнению с фолликулярным в районах с повышенных потреблением йода. Другое исследование показало значительно большую встречаемость BRAF-позитивного папиллярного РЩЖ в вулканическом районе Сицилии, в воде которого наблюдаются повышенные концентрации бора, железа, ванадия, магния и других химических элементов. Эти данные позволили предположить, что индуцирование точечных BRAF-мутаций может быть ассоциировано с чрезмерным воздействием различных химических элементов и соединений.
