- Рекомендовано всем пациентам с метастатическим колоректальным раком для определения возможности применения анти-EGFR антител;
- Рекомендовано пациентам с метастатическим немелкоклеточным раком легкого для определения возможных вариантов таргетной терапии.
KRAS представляет собой протоонкоген из семейства белков RAS и кодирует G-белок, активно участвующей в регуляции и контроле клеточной пролиферации, дифференцировки и выживании. Белок KRAS неактивен в нормальных не пролиферирующих клетках, но вступает в работу при связывании с ГТФ, что приводит к реактивации рецепторов факторов роста. Комплекс KRAS-ГТФ связывается и активирует ряд вторичных посредников передачи клеточного сигнала, такие как RAS/RAF/MEK/MAPK и PI3K/AKT/mTOR.
KRAS играет основную роль в контроле передачи сигнала от ряда рецепторов факторов роста, в том числе EGFR. Активирующие мутации в гене KRAS изменяют ГТФ-азную активность белка и блокируют возможность его деактивации, что ведет к гиперактивации ряда внутриклеточных путей передачи сигнала, контролирующих рост и пролиферацию клеток.
Мутации KRAS наиболее часто встречаются при раке поджелудочной железы (88%), колоректальном раке (45%-50%), и немелкоклеточном раке легкого (31%-35%).
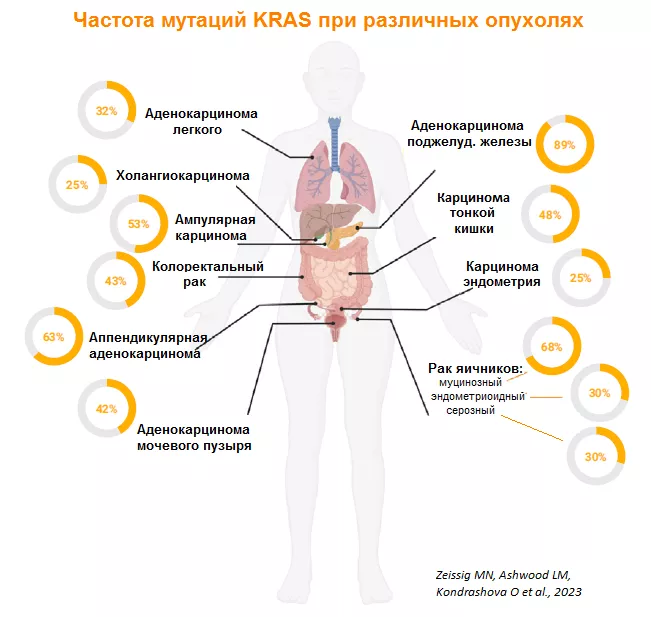
Таблица 1. Частота встречаемости мутаций KRAS при злокачественных опухолях человека [6]
|
Тип опухоли |
Частота встречаемости мутаций KRAS |
|---|---|
|
аденокарцинома поджелудочной железы |
≥ 80% |
|
колоректальный рак (КРР) |
30–50% |
|
немелкоклеточный рак легкого (НМРЛ): |
|
|
- аденокарцинома |
30% |
|
- плоскоклеточная карцинома |
5% |
|
холангиокарцинома: |
|
|
- внепеченочная |
45–54% |
|
- внутрипеченочная |
10–15% |
|
множественная миелома |
21–33% |
|
рак тела матки: |
|
|
- эндометриоидный |
21–26% |
|
- серозный |
2% |
|
рак желудка |
3–13% |
|
рак яичка |
9–16% |
|
аденокарцинома шейки матки |
7–18% |
|
диффузная B-клеточная крупноклеточная лимфома |
1.6% |
|
рак пищевода: |
|
|
- аденокарцинома |
3.8–17% |
|
- плоскоклеточная карцинома |
0–12% |
|
рак молочной железы |
8–13% |
|
острый миелоидный лейкоз |
5–23% |
|
хронический лимфолейкоз |
0.7–7% |
|
рак желчного пузыря |
4% |
|
злокачественная кожная меланома |
<1% |
Высокая вариабельность распространённости мутаций в гене KRAS связана с этническими, половыми различиями выборок пациентов, а также факторами риска. Так, мутации в данном гене шире распространены в европейской популяции, чем у пациентов из Азии. У пациентов с аденокарциномой легкого, которые никогда не курили, распространённость аберраций в гене KRAS составила 0-15%. Кроме этого, мутации в данном гене редко встречают при мелкоклеточном раке легкого.
Наиболее часто встречаются активирующие мутации в кодонах 12 и 13 (экзон 2), 59 и 61 (экзон 3), 117 и 146 (экзон 4) гена KRAS. Чаще всего мутации выявляются в кодоне 12: G12D, G12V, G12C и другие.
Паталогическая аберрация G12D встречается в 20–50% злокачественных опухолей с мутациями KRAS; в том числе в 50% случаев ампуллярной карциномы, 48% случаев аппендикулярной карциномы, 44% случаев холангиокарциномы.
Частота встречаемости мутаций KRAS при немелкоклеточном раке легкого составляет 30% при аденокарциномах и 5% при плоскоклеточном раке. 97% мутаций KRAS локализованы в экзонах 2 и 3 (G12, G13, и Q61); частота встречаемости мутаций в экзоне 12 следующая: G12C – 39-40%, G12V - 18–21%, G12D - 17–18%. Мутации KRAS редко сочетаются с мутациями в EGFR, BRAF и перестройками ALK. Мутации G12C и G12V в гене KRAS являются предикторами более быстрого прогрессирования заболевания.
Частота выявления мутации KRAS при метастатическом колоректальном раке составляет от 30-50%. Наиболее часто встречаются мутации G12D и G12V.
При раке поджелудочной железы мутации KRAS выявляются в 80% случаев, наиболее частой является G12D.
Было показано, что у пациентов с мутациями в кодонах 12,13 (экзон 2), 59, 61 (экзон 3), 117, 146 (экзон 4) гена KRAS терапия ингибиторами EGFR неэффективна, поскольку происходит паталогическая активация сигнальных путей ниже уровня рецептора к EGFR.
В настоящее время разработана таргетная терапия при мутации KRAS G12C у пациентов с распространенным немелкоклеточным раком легкого (препарат соторасиб одобрен к применению, препарат адаграсиб проходит финальную стадию клинических испытаний).
1) Judd J, Abdel Karim N, Khan H et al. Characterization of KRAS Mutation Subtypes in Non-small Cell Lung Cancer. Mol Cancer Ther. 2021 Dec;20(12):2577-2584. doi: 10.1158/1535-7163.MCT-21-0201
2) Margonis GA, Kreis ME, Wolfgang CL, Weiss MJ. Mutation status and surgical selection. J Surg Oncol. 2019 Apr;119(5):616-622. doi: 10.1002/jso.25413
3) Zeissig MN, Ashwood LM, Kondrashova O, Sutherland KD. Next batter up! Targeting cancers with KRAS-G12D mutations. Trends Cancer. 2023 Nov;9(11):955-967. doi: 10.1016/j.trecan.2023.07.010
4) Hyun S, Shin D. Small-Molecule Inhibitors and Degraders Targeting KRAS-Driven Cancers. Int J Mol Sci. 2021 Nov 9;22(22):12142. doi: 10.3390/ijms222212142
5) Zhu G, Pei L, Xia H, Tang Q, Bi F. Role of oncogenic KRAS in the prognosis, diagnosis and treatment of colorectal cancer. Mol Cancer. 2021 Nov 6;20(1):143. doi: 10.1186/s12943-021-01441-4
6) Uprety D, Adjei AA. KRAS: From undruggable to a druggable Cancer Target. Cancer Treat Rev. 2020 Sep;89:102070. doi: 10.1016/j.ctrv.2020.102070
