- Диагностика иммунодефицитов, связанных с нарушением работы путей системы комплемента;
- Диагностика нарушения работы классического пути системы комплемента;
- Диагностика нарушения работы альтернативного пути системы комплемента;
- Диагностика нарушения работы классического пути системы комплемента;
- Диагностика нарушения работы лектинового пути системы комплемента;
- Диагностика системных заболеваний соединительной ткани.
Система комплемента - это каскадная система протеолитических ферментов, являющаяся частью врождённого гуморального иммунного ответа. Она представляет собой набор из более чем 40 различных белков, как растворенных в плазме крови, так и экспрессируемых на мембранах клеток организма. Эти белки взаимодействуют между собой и формируют сложный каскад биохимических реакций, обеспечивающих иммунную реакцию в ответ на взаимодействие антигена с антителом, фагоцитоз, разрушение чужеродных бактерий и поддерживает различные воспалительные реакции. Существует система ингибиторов и регуляторов.
Существует три пути активации системы комплемента: классический, лектиновый и альтернативный.
Классический путь начинается со связывания антител IgM и/или IgG с антигеном, а также может активироваться связыванием CRP с поверхностью клетки; далее происходит связывание белка C1q и последовательная активация C1r и C1s. Активированные C1s расщепляют белки C4 и C2 на фрагменты C4b и C4a, C2a и C2b соответственно. Из фрагментов C4b и C2a формируется C3-конвертаза классического пути C4bC2a, которая может расщеплять белок C3 на два фрагмента – C3b и C3a.
Лектиновый путь, в целом, очень похож на классический путь активации комплемента, лишь с тем отличием, что в качестве «паттернов» распознавания патогена выступают полимеры моносахаров, соединенных о-гликозидными связями, – гликаны, часто встречающиеся на мембранах бактерий и редко появляющиеся на мембранах клеток организма. Так, например, гликаны дрожжей часто оканчиваются маннозой, а гликаны клеток человека – сиаловыми кислотами. Один из белков, запускающих активацию по лектиновому пути, – маннозосвязывающий лектин (mannose-binding lectin – MBL, МСЛ). В дальнейшем происходит активация MASP1 и MASP2, которые расщепляют C2 и C4 на те же C4b, C4a, C2a и C2b, и происходит сборка C3-конвертазы классического пути C4bC2a. Ингибиторы C4BP и FH ускоряют распад C4bC2a и предотвращают ее сборку.
Альтернативный путь. Активация начинается со спонтанного гидролиза C3, не зависящего от присутствия в организме патогенных клеток. С помощью факторов B и D происходит образование изначальной «initial» С3-конвертазы альтернативного пути C3(H2O)FBb, которая может расщеплять белок C3 на те же два фрагмента – C3b и C3a. На следующей стадии происходит усиление ответа системы комплемента от всех путей активации. Расщепление белка C3 и образование фрагмента C3b приводит к запуску петли положительной связи системы комплемента и лавинообразному нарастанию концентрации C3b. При участии белков фактора B и фактора D образуется C3-конвертаза альтернативного пути C3bFBb, которая может расщеплять новые C3. Этот процесс регулируется ингибиторами DAF, FH, MCP, CR1 и FI. При лавинообразном нарастании количества C3b этот фрагмент на поверхности клеток начинает связываться с C3-конвертазами C4bC2a и C3bFBb с образованием С5-конвертаз C4bC2aC3b и C3bFBbC3b.
Здесь начинается терминальная стадия активации комплемента, одинаковая для всех путей: расщепление C5 на фрагменты C5a и C5b приводит к последовательному связыванию с C5b белков C6, C7, C8 и нескольких C9, в результате чего в мембране патогенной клетки собирается мембраноатакующий комплекс (МАК), приводящий к лизису патогена.
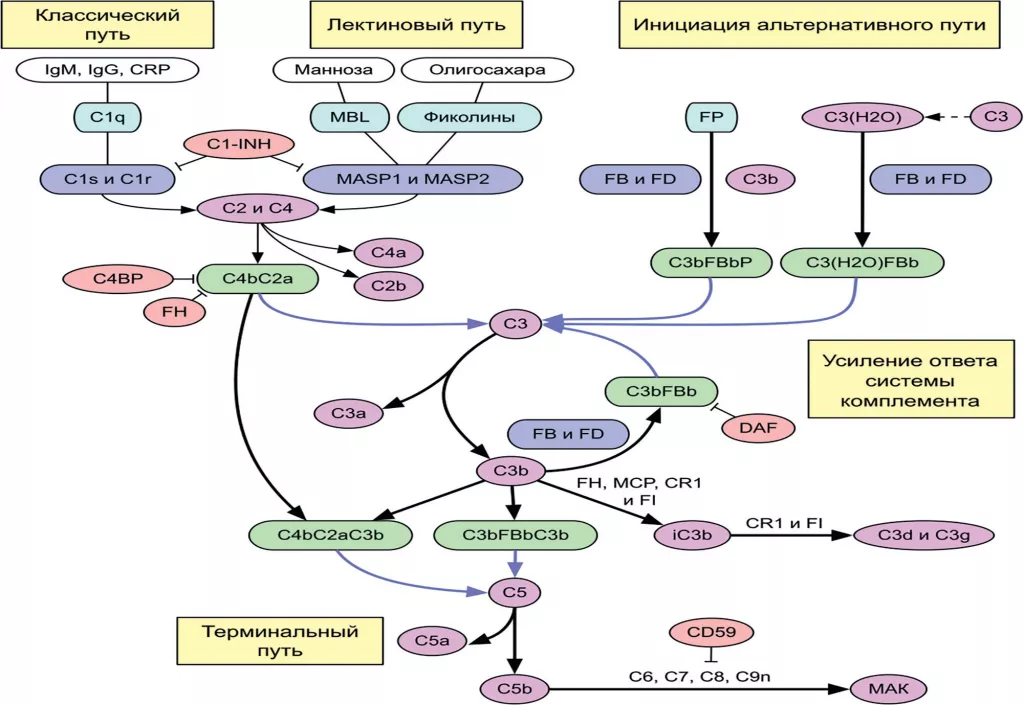
Рис 1. Система комплемента [3]
Дефекты системы комплемента – самый редкий вид иммунодефицитов, составляющий около 1% от всех первичных иммунодефицитов. Обычно дефекты компонентов классического или альтернативного пути комплемента приводят к развитию или системного аутоиммунного заболевания, в основном системной красной волчанки (СКВ), которая часто ассоциирована с врожденными дефектами системы комплемента, или рецидивирующих бактериальных инфекций, преимущественно респираторного тракта.
Нарушение функции комплемента следует подозревать во всех случаях рецидивирующего отека Квинке, аутоиммунных заболеваний, хронического нефрита или сегментарной липодистрофии, а также при частых гнойных инфекциях, диссеминации менингококковой или гонококковой инфекции и повторной бактериемии у больных любого возраста.
Проба на общую гемолитическую активность комплемента (СН50) позволяет выявить большинство нарушений этой системы. Нормальные результаты пробы свидетельствуют о способности всех 11 компонентов классического пути активации комплемента и мембрано-атакующего комплекса лизировать покрытые антителами эритроциты. При наследственной недостаточности компонентов от С1 до С8 показатель СН50 близок к нулю.
Первичная недостаточность компонентов комплемента.
Описаны случаи врожденной недостаточности всех 11 компонентов комплемента классического пути, а также фактора D-альтернативного пути.
Первичная недостаточность C1q чаще всего обнаруживается при СКВ или волчаночном синдроме (в отсутствие характерных для СКВ серологических данных), хронической сыпи (при которой в биоптатах кожи находят васкулит) или мезангиопролиферативном гломерулонефрите. У некоторых детей с недостаточностью С1q развиваются тяжелые инфекции, включая септицемию и менингит.
Для недостаточности C1rs характерно полное отсутствие C1r в сочетании с той или иной степенью недостаточности C1s. Это обусловлено, вероятно, близким соседством генов обоих белков на хромосоме 12. Как и при недостаточности C1q, больные с недостаточностью C1r/C1s, C4, C2 или С3 очень часто подвержены аутоиммунным заболеваниям, особенно СКВ или волчаночному синдрому (при котором уровень антиядерных антител не повышен).
Компонент С4 кодируется двумя генами, и их продукты называются С4А и С4В. Полное отсутствие С4А встречается примерно у 1% населения и также предрасполагает к СКВ, хотя общий уровень С4 при этом снижен лишь в умеренной степени.
Пациенты с недостаточностью С5, С6, С7 или С8 могут страдать СКВ, но для них более характерны частые инфекции, вызываемые микроорганизмами рода Neisseria.
У ряда больных с недостаточностью С2 повторно развивается угрожающая жизни септицемия, чаще всего пневмококковая. Это наиболее распространенная форма недостаточности комплемента у представителей европеоидной расы. Однако у большинства подверженность инфекциям не повышена, что связано, вероятно, с защитной функцией компонентов альтернативного пути.
Гены С2, фактора В и С4 расположены на хромосоме 6 близко друг к другу, и недостаточность С2 может сочетаться со снижением фактора В. При недостаточности обоих белков риск инфекций особенно высок.
Одновременное снижение концентраций С4 и С3 указывает на активацию классического пути. Напротив, низкий уровень С3 при нормальном уровне С4 свидетельствует об активации альтернативного пути. Поскольку С3 активируется по ходу как классического, так и альтернативного пути, нарушение одного из них может, по крайней мере, частично компенсироваться другим.
Без С3 не образуется хемотаксический фрагмент С5 (С5а) и не происходит опсонизации бактерий. Уничтожение некоторых микробов возможно лишь после их надежной опсонизации. Поэтому генетическая недостаточность С3 сопровождается частыми и тяжелыми гнойными инфекциями, вызываемыми пневмококка ми, менингококками и гонококками.
Более чем у 50% больных врожденной недостаточностью С5, С6, С7 или С8 развивается менингококковый менингит или экстрагенитальная гонококковая инфекция. При недостаточности С9 показатель СН50 снижен примерно вдвое, у 30% таких больных обнаруживается инфекция, вызываемая микроорганизмами рода Neisseria. Особенно часто дефицит С9 регистрируют в японской популяции (более 1:500).
У 3–15% больных (в возрасте 10 лет и старше) с системной менингококковой инфекцией обнаруживается генетическая недостаточность С5, С6, С7, С8, С9 или пропердина.
У немногих больных выявляется недостаточность фактора D-альтернативного пути. Все они страдают рецидивирующими инфекциями, обычно вызванными Neisseria. Гемолитическая активность комплемента остается нормальной, но активность альтернативного пути практически отсутствует.
Маннозосвязывающий лектин (МСЛ) – важный компонент врожденного иммунитета, который защищает организм от инфекций одновременно с возникновением специфического иммунного ответа. Полиморфизм промоторной области гена МСЛ и мутации его структурного гена обсулавливают резкие различия уровня МСЛ в крови разных людей. При очень низкой его концентрации (недостаточность МСЛ) возрастает предрасположенность к рецидивирующим гнойным и грибковым инфекциям, особенно в раннем детском возрасте. Эта тенденция исчезает с возрастом по мере становления функциональной активности иммунной системы. У взрослых лиц дефицит МСЛ не ассоциирован с тяжелыми нарушениями, если он не сопровождается иммуносупрессией.
Существует также недостаточность плазменных, мембранных и сывороточных регуляторных белков комплемента, а также вторичные нарушения системы комплемента.
1) Сердобинцев К.В. (2016). Система комплемента (часть 1). Аллергология и иммунология в педиатрии, (2 (45)), 41-48. doi: 10.24411/2500-1175-2016-00013
2) Сердобинцев К.В. (2016). Система комплемента. Патология, диагностика, лечение (часть 2). Аллергология и иммунология в педиатрии, (3 (46)), 33-40. doi: 10.24411/2500-1175-2016-00018
3) Шахиджанов С.С., Филиппова А.Е., Бутылин А.А., Атауллаханов Ф.И. Cовременное представление о системе комплемента. Вопросы гематологии/онкологии и иммунопатологии в педиатрии. 2019;18(3):130-144. https://doi.org/10.24287/1726-1708-2019-18-3-130-144
4) Бутылин А.А., Филиппова А.Е., Шахиджанов С.С., Атауллаханов Ф.И. Патологии системы комплемента. Вопросы гематологии/онкологии и иммунопатологии в педиатрии. 2020;19(1):131-138. https://doi.org/10.24287/1726-1708-2020-19-1-131-138
5) Defendi F, Thielens NM, Clavarino G, Cesbron JY, Dumestre-Pérard C. The Immunopathology of Complement Proteins and Innate Immunity in Autoimmune Disease. Clin Rev Allergy Immunol. 2020 Apr;58(2):229-251. doi: 10.1007/s12016-019-08774-5
6) Frazer-Abel A, Sepiashvili L, Mbughuni MM, Willrich MA. Overview of Laboratory Testing and Clinical Presentations of Complement Deficiencies and Dysregulation. Adv Clin Chem. 2016;77:1-75. doi: 10.1016/bs.acc.2016.06.001
7) Willrich MAV, Braun KMP, Moyer AM, Jeffrey DH, Frazer-Abel A. Complement testing in the clinical laboratory. Crit Rev Clin Lab Sci. 2021 Nov;58(7):447-478. doi: 10.1080/10408363.2021.1907297
