Международные рекомендации 2020 г. по выявлению АНЦА при прочих заболеваниях, помимо системного васкулита
Тестирование на антинейтрофильные цитоплазматические антитела (АНЦА), направленные против протеиназы 3 (ПР3) и миелопероксидазы (МПО) широко используется для диагностики АНЦА-ассоциированных васкулитов (ААВ), к которым относятся гранулематоз с полиангиитом (ГПА, гранулематоз Вегенера), микроскопический полиангиит (МПА) и эозинофильный гранулематоз с полиангиитом (ЭГПА). В 2017 г. был опубликован пересмотренный международный консенсус по выявлению АНЦА при АНЦА-ассоциированных васкулитах. Настоящие рекомендации касаются диагностической значимости АНЦА при различных аутоиммунных, инфекционных и неопластических заболеваниях.
Сначала мы приводим сводную таблицу с рекомендациями по тестированию. Ниже приведены подробные комментарии по различным заболеваниям.
Таблица 1. Рекомендации по тестированию на АНЦА при прочих заболеваниях, помимо АНЦА-ассоциированного васкулита
|
Заболевание |
Рекомендации |
Уровень согласия экспертов |
|---|---|---|
|
Любое заболевание |
Тестирование на АНЦА* обязательно только у пациентов с клиническими признаками ААВ |
100% |
|
Синдром Гудпасчера |
Тестирование на АНЦА* показано всем пациентам с синдромом Гудпасчера |
100% |
|
Идиопатическая интерстициальная пневмония |
Тестирование на АНЦА* показано всем пациентам с идиопатической интерстициальной пневмонией |
96.6% |
|
Ревматоидный артрит |
Рутинное тестирование не рекомендовано. Рекомендовано тестирование на АНЦА* только у пациентов с поражением почек и «нефритическим» мочевым осадком |
96.6% |
|
Системная красная волчанка |
Рутинное тестирование не рекомендовано. Рекомендовано тестирование на АНЦА* только у пациентов с выраженными некротизирующими и серповидными поражениями или пролиферативным волчаночным нефритом по данным биопсии почки |
100% |
|
Болезнь Шегрена |
Рутинное тестирование не рекомендовано. Рекомендовано тестирование на АНЦА* только у пациентов с поражением почек и «нефритическим» мочевым осадком |
96.6% |
|
Системная склеродермия |
Рутинное тестирование не рекомендовано. Рекомендовано тестирование на АНЦА* только у пациентов с поражением почек и «нефритическим» мочевым осадком |
96.6% |
|
Аутоиммунные заболевания печени (АИГ-1, ПСХ и ПБХ) |
Рутинное тестирование не рекомендовано. Тестирование на АНЦА с помощью нРИФ может быть полезно у пациентов с подозрением на АИГ-1 при отсутствии типичных аутоантител. Примечание: наша лаборатория, основываясь на собственных данных, рекомендует проводить тестирование на АНЦА при аутоиммунных заболеваниях печени |
89.7% |
|
Воспалительные заболевания кишечника (ЯК и БК) |
Рутинное тестирование не рекомендовано. АНЦА и ASCA могут использоваться для дифференциальной диагностики ЯК и БК в сложных диагностических случаях. |
96.6% |
|
Инфекции |
Рутинное тестирование не рекомендовано. Рекомендовано тестирование на АНЦА* при поражении почек, особенно у больных с инфекционным эндокардитом |
89.7% |
|
Злокачественные новообразования |
Рутинное тестирование не рекомендовано. |
96.6% |
*Тестирование на АНЦА предполагает определение МПО-АНЦА и ПР3-АНЦА методом твердофазного ИФА в соответствии с рекомендациями 2017 г.
Методики выявления АНЦА и номенклатура
Скрининговым тестом является непрямая иммунофлюоресценция (нРИФ), использующая фиксированные этанолом нейтрофилы. Определяется титр антител и тип свечения. Существует два основных типа свечения: цитоплазматический (цАНЦА) и перинуклеарный (пАНЦА). АТ к протеиназе-3 (ПР3) дают цитоплазматический тип свечения (цАНЦА) с центральной или междольковой акцентуацией в цитоплазме. АТ к миелопероксидазе (МПО) дают перинуклеарный тип свечения (пАНЦА) с окрашиванием гранул вокруг ядра нейтрофила. Строго говоря, тип свечения цитоплазмы нейтрофила представляет собой артефакт фиксации нейтрофильных гранул эталонолом. Будучи слабым фиксатором, этанол позволяет пререраспределиться белковым антигенам азурофильных гранул. Миелопероксидаза, которая обладает выраженным положительным зарядом выходит из гранул и фиксируется на ядре клетки, содержащем отрицательно заряженные нуклеиновые кислоты. Именно это обуславливает т.н. перинуклеарный тип флюоресценции. Протеиназа-3, напротив, является нейтральным белком и из гранул не мигрирует, поэтому отмечается цитоплазматический (цАНЦА) тип свечения, максимальная интенсивность которого выявляется между дольками ядра.
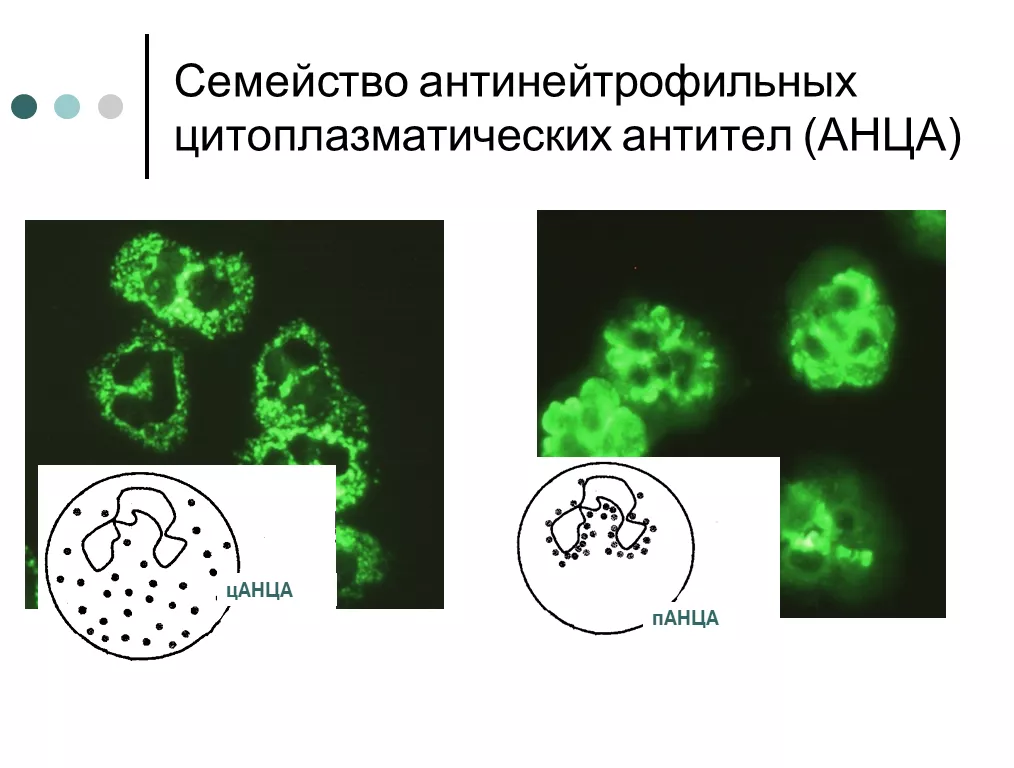
Атипичный тип свечения пАНЦА (далее будет обозначаться как аАНЦА или xANCA) может быть обнаружен у пациентов с АТ к другим АГ: эластазе, катепсину G, лактоферрину, лизоциму. пАНЦА могут не выявляться (могут быть «скрыты») при наличии АНА. АТ к BPI («бактерицидный, увеличивающий проницаемость белок»), дают атипичный характер цАНЦА без междольковой акцентуации. Твердофазные тесты, такие как ИФА и хемилюминесцентный иммуноанализ, используются для обнаружения специфических антител к протеиназе-3 и МПО.
АНЦА при ревматоидном артрите
Тип свечения пАНЦА, который изначально назывался "гранулоцитарно-специфическим", впервые был описан у пациентов с синдромом Фелти (разновидность серопозитивного ревматоидного артрита, при котором развивается нейтропения и спленомегалия) и позднее был обнаружен у 50-70% пациентов с РА, осложненного васкулитом и у 20-40% пациентов с РА, не осложненным васкулитом или синдромом Фелти. Следует подчеркнуть, что при РА антигенную специфичность пАНЦА удается установить менее чем в 5% случае, чаще всего причиной пАНЦА являются аутоантитела к МРО или к лактоферрину.
В последующих исследованиях частота пАНЦА при РА варьировала от 16% до 50%. В самом большом исследовании пАНЦА-позитивность была выявлена только у 15% больных с РА. Данные о прогнозировании активности РА и прогрессии костных деструкции на основании пАНЦА крайне противоречивы. В некоторых исследованиях была показана корреляция между пАНЦА-позитивностью и активностью и степенью тяжести заболевания. В других исследованиях эта корреляция не была подтверждена. В очень редких случаях РА может сочетаться с АНЦА-ассоциированным васкулитом.
АНЦА при системной красной волчанке
В одном из исследований АНЦА были выявлены методом нРИФ у 16,4% из 566 пациентов-европейцев, в то время как методом ИФА антитела к МПО и ПР3 были выявлены только у 9.3% и 1.7% пациентов соответственно. Следует отметить, что АНА, присутствующие в высоких титрах в этих случаях, могут быть неотличимы от пАНЦА.
В другом исследовании была показана частота встречаемости пАНЦА 14,0 – 31,4%, встречаемость антител к МПО составила 23,8%, а антител к ПР3 - 12,7%. Ряд исследователей отмечает, что при наличии высокого титра АТ к дсДНК высока вероятность ложно-положительных тестов на МПО-АНЦА.
СКВ и АНЦА-ассоциированный васкулит могут существовать одновременно у одного пациента. Было показано, что МПО-АНЦА значительно чаще встречаются при волчаночном нефрите с полулуниями, чем в случаях гломерулонефрита при котором полулуния отсутствуют (21.2% vs. 0.8%). По-видимому, АНЦА опосредует специфические механизмы воспаления в почечных клубочках, которые накладываются на иммунокомплексные механизмы.
Как и в случае с РА, при СКВ выявляются другие мишени для АНЦА, в частности АНЦА к лактоферрину были выявлены у 14,3% пациентов с СКВ.
В целом, АНЦА-позитивность (особенно МПО-АНЦА) нечасто встречается у больных с СКВ. Клиническая значимость АНЦА при СКВ неясна, но может указывать на быструю прогрессию гломерулонефрита.
АНЦА при системной склеродермии
Системная склеродермия редко сочетается с АНЦА-ассоциированным васкулитом (0,2-0,4%). В австралийском исследовании по склеродермии, в котором были проанализированы данные 1303 пациентов, АНЦА были обнаружены у 8,9% пациентов, при это антитела к МПО и ПР3 были выявлены только у 2,4% пациентов. Позитивность по ПР3-АНЦА была ассоциирована с высоким риском развития интерстициальной болезни легких. В целом, АНЦА редко встречаются при склеродермии, АНЦА-ассоциированный васкулит – ещё реже.
АНЦА при синдроме Шегрена
В трех исследованиях было показано, что частота встречаемости АНЦА при СШ составила 9%, чаще всего это были пАНЦА. Частота антител к МПО составила 3%, а антитела к ПР3 не встречались вообще. Была показана значимая ассоциированность между выявлением АНЦА и экстрагландулярными проявлениями (феноменом Рейно, кожным васкулитом, периферической нейропатией) среди пациентов с первичным синдромом Шегрена. В целом, МПО-АНЦА редко выявляются при синдроме Шегрена.
АНЦА при аутоиммунных болезнях печени
Аутоиммунные болезни печени (АБП) включают в себя аутоиммунный гепатит, первичный склерозирующий холангит (ПСХ) и первичный билиарный холангит (ПБХ). В мире описано всего семь случаев сочетания АНЦА-ассоциированного васкулита с АБП, вместе с тем АНЦА часто обнаруживаются при АБП. Обычно выявляются аАНЦА (xANCA), которые в отличие от МПО-АНЦА и ПР3-АНЦА направлены против антигенов, находящихся на периферии ядра. аАНЦА реагируют с бета-тубулином (изотип 5), для которого характерна высокая степень структурной гомологии с бактериальным белком FtsZ. Последний есть почти у всех представителей кишечной микрофлоры. Везикулярный интегральный мембранный протеин-36, который выполняет роль внутриклеточного лектина – ещё одна потенциальная антигенная мишень аАНЦА при АБП. Также некоторые нейтрофильные гранулярные белки могут выступать в качестве мишеней для аАНЦА: лактоферрин, катепсин G, каталаза, альфа-энолаза, BIP. Однако реакции с этими АГ были обнаружены лишь у незначительной части больных с АБП. аАНЦА, по-видимому не являются специфичными для АБП и могут быть также обнаружены у значительного процента пациентов с вирусным и алкогольным поражением печени.
Пациенты с аутоиммунным гепатитом (АИГ) по спектру выявляемых у них АТ подразделяются на АИГ тип 1 (95%) и АИГ тип 2 (5%). аАНЦА чаще всего выявляются при АИГ-1 (65-81%), при АИГ-2 пациенты обычно негативны по этим АТ. Прогностическая значимость аАНЦА при АИГ спорная, хотя в двух исследованиях было показано, что они могут быть ассоциированы с рецидивом гепатита и с более тяжелой некротизирующей воспалительной активностью. Выявление аАНЦА может иметь диагностическую значимость в некоторых случаях, особенно при отсутствии типичных АТ.
Частота встречаемости аАНЦА при первичном билиарном холангите составляет 26-67%. В настоящее время нет убедительных данных в пользу того, что они имеют диагностическую значимость при данном заболевании.
Первичный склерозирующий холангит (ПСХ) может «пересекаться» с аутоиммунным гепатитом в 5-10% случаев и устойчиво ассоциирован с воспалительными заболеваниями кишечника, чаще всего с ЯК; частота встречаемости аАНЦА при ПСХ составила 26%-94% (в среднем, 63%). В одном из исследований аАНЦА были охарактеризованы как диагностически значимый биомаркер ПСХ. В других исследованиях было показано, что позитивность по аАНЦА при ПСХ ассоциирована с желчными камнями и холангиокарциномой, более обширным поражением желчных путей и трансплантацией печени. В недавнем норвежском исследовании АНЦА были обнаружены у 80% пациентов с ПСХ, пАНЦА – у 70%. Эти АНЦА-позитивные пациенты были моложе на момент постановки диагноза, и у них был более низкий риск развития билиарного рака, но ассоциации с ВЗК не было. Частота развития билиарного рака в значительно большей степени была ассоциирована с возрастом на момент постановки диагноза, нежели с АНЦА-статусом. Таким образом, данных в пользу прогностической значимости аАНЦА-позитивности при ПСХ недостаточно.
АНЦА выявлялись в желчи больных с ПСХ достоверно чаще (38%), чем у больных без ПСХ (6%; p = 0.001) и были ассоциированы с десятикратным повышением риска ПСХ. Обнаружение АНЦА в желчи коррелировало с более тяжелым поражением желчных путей и последующим количеством вмешательств.
В нескольких исследованиях частота выявления антител к МПО и к ПР3 у пациентов с ПСХ составила лишь 2% и 4% соответственно.
Таким образом, аАНЦА (xANCA) часто обнаруживаются в сыворотке пациентов с аутоиммунными заболеваниями печени и могут помочь в постановке диагноза АИГ-1, особенно при отсутствии типичных АТ. аАНЦА не специфичны для АЗП и могут быть обнаружены при вирусном и алкогольном поражении печени. Только в одном исследовании была показана диагностическая значимость антител к ПР3 как биомаркеров первичного склерозирующего холангита, при помощи которого можно дифференцировать данное состояние от АИГ и ПБХ.
АНЦА при воспалительных заболеваниях кишечника
Две основные формы воспалительных заболеваний кишечника (ВЗК) – болезнь Крона (БК) и язвенный колит (ЯК). У этих форм есть как общие, так и специфичные признаки.
У пациентов с ВЗК часто выявляются аАНЦА (xANCA), антигликановые АТ, в частности, АТ к Saccharomyces cerevisiae (ASCA) и другие АТ, направленные против микробных и дрожжевых пептидов. ASCA направлены к маннану клеточной стенки дрожжей Saccharomyces, обладающему высокой степенью гомологии с кишечными бактериями.
Согласно обзорам литературы, ASCA и аАНЦА были обнаружены у 29-69% и 6-38% соответственно пациентов с БК, 0-29% и 41-73% пациентов с ЯК, 0-23% и 8% пациентов с другими заболеваниями ЖКТ, 0-16% и 0-8% здоровых людей.
ASCA чувствительны и специфичны для болезни Крона, аАНЦА (xANCA) – для ЯК. Позитивность по ASCA ассоциирована с поражением тонкой кишки, позитивность по аАНЦА – с поражением толстой кишки.
У некоторых пациентов с поражением толстой кишки может быть установлен диагноз ВЗК, но дальнейшая дифференцировка на БК и ЯК представляется затруднительной. По данным мета-анализа, доля недифиренцированных ВЗК составляет от 1 до 20% у взрослых и от 4 до 22% у детей (в среднем, 6% и 13% в этих группах соответственно).
В проспективном исследовании, в которое вошли 97 пациентов с недифиренцированным ВЗК, статус ASCA (+) / аАНЦА (-) помог установить диагноз БК у 80% пациентов, а статус ASCA (-) / аАНЦА (+) помог установить диагноз ЯК у 63,6% пациентов.
Наиболее интригующим стало исследование, в котором половина пациентов с недифиренцированным ВЗК были негативны по ASCA и по аАНЦА. Аналогичные тенденции наметились и в других исследованиях. В другом проспективном исследовании была показана ограниченная значимость ASCA и аАНЦА в плане уточнения диагноза при недифиренцированном ВЗК.
Высокие титры аАНЦА были обнаружены при активном ЯК. Однако в некоторых исследованиях не было обнаружено ассоциации между аАНЦА-позитивностью и активностью ЯК, в то время как в других исследованиях было показано более агрессивное течение ЯК у серопозитивных пациентов. В проспективном исследовании, которое включало в себя 406 детей, у пациентов с аАНЦА (+) /ASCA (-) чаще было более тяжелое течение заболевания на момент постановки диагноза. В другом европейском исследовании, в которое вошли 432 пациента с ЯК, позитивность по аАНЦА была ассоциирована с повышенным риском рецидива заболевания и общим количеством рецидивов. В недавнем исследовании, в которое вошел 601 пациент с ЯК, не было обнаружено ассоциации между аАНЦА, ASCA и тяжестью течения заболевания, проксимальным распространением ЯК или необходимостью выполнения колэктомии. У пациентов с ЯК серонегативность по аАНЦА была предвестником более выраженного раннего ответа на инфликсимаб. Напротив, у 279 пациентов с БК не было выявлено взаимосвязи между наличием аАНЦА или ASCA и ответом на инфликсимаб.
Было показано, что основной мишенью для аАНЦА при НЯК является комплекс ДНК-лактоферрин.
Недавно ПР3-АНЦА стал рассматриваться как биомаркер ВЗК. Сывороточный титры антител к ПР3, выявленный хемилюминесцентным тестом, чаще встречается при ЯК, чем при БК (29,2% vs. 2.7%; P<0.0001). Наличие антител к ПР3 при ЯК было ассоциировано с более распространенным колитом и более короткой продолжительностью заболевания.
В одном из исследований в группе, включавшей 61 детей, был показан наилучший баланс чувствительности и специфичности антител к ПР3 при ЯК (58% и 93%, соответственно).
В другом исследовании, антитела к ПР3 и МПО были обнаружены у 39,2% и 12,8% из 102 пациентов с ЯК соответственно, тогда как распространенность антител к ПР3 у пациентов с БК и здоровых людей контрольной группы была очень низкой (1,5 -6,0%), и ни у одного пациента или контрольной группы не было положительного результата выявления антител к МПО. В этом исследовании выявление антител к ПР3 имело чувствительность 39,2% и специфичность 96,1% для ЯК.
Целиакия, как и ВЗК, характеризуется хронической диареей и наличием определенного спектра аутоантител, направленных к тканевой трансглутаминазе, деимидированному глиадину и другим антигенам. В одном из исследований была показана высокая распространенность аАНЦА и ASCA у пациентов с целиакией (22% и 43% соответственно). Следовательно, наличие аАНЦА или ASCA в сыворотке больных хронической диареей не исключает диагноз целиакии.
Таким образом, аАНЦА могут быть обнаружены с помощью нРИФ у 40-70% пациентов с ЯК, тогда как ASCA обнаруживается у пациентов с БК. Определение этих антител может помочь диференцировать ЯК от БК в сложных диагностических случаях. Накопленные данные свидетельствуют о том, что антитела к ПР3 могут быть дополнительным чувствительным и специфичным биомаркером для выявления ЯК и дифференциальной диагностики с БК.
АНЦА при синдроме Гудпасчера
Синдром Гудпасчера (в современной англоязычной литературе используется термин «anti-glomerular basement membrane disease» или «anti-GBM»)– редкий системный васкулит, характеризующийся выработкой АТ к коллагену IV типа, который экспрессируется в базальной мембране почечных клубочков и альвеолярной базальной мембране.
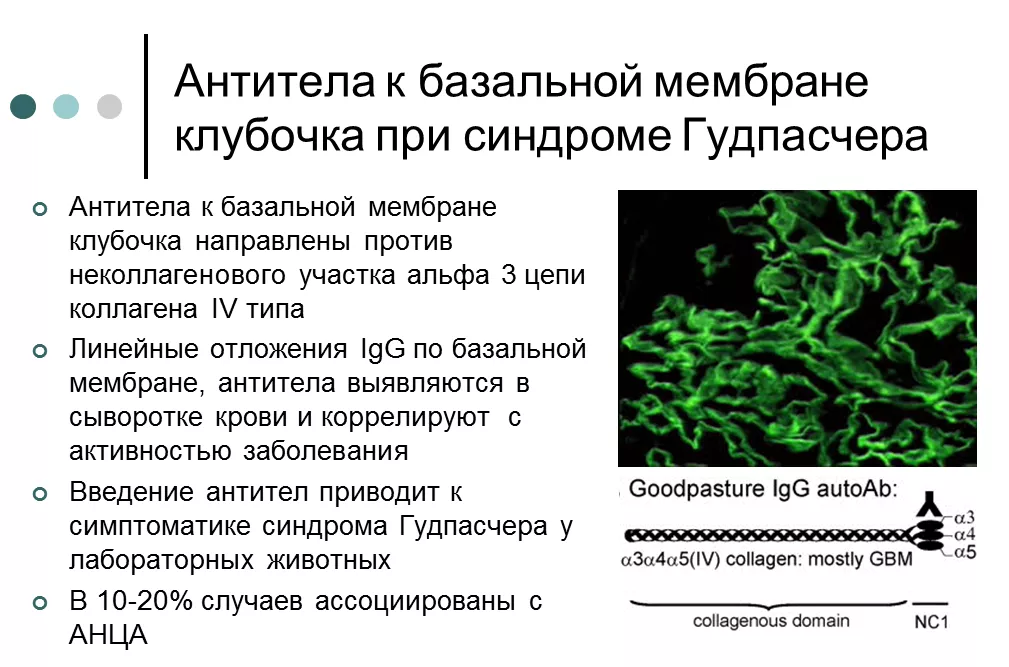
Примерно у 50% пациентов развивается быстро прогрессирующий гломерулонефрит с сопутствующим альвеолярным кровотечением. В нескольких исследованиях было показано, что у 5-9% АНЦА-позитивных пациентов с ААВ выявляются АТ к базальной мембране клубочков (БМК). С другой стороны, у 13-47% пациентов с АТ к БМК выявляются АНЦА, в основном, антитела к МПО (61-90% двойных позитивных случаев).
АНЦА в низком титре появляются у пациентов с синдромом Гудпасчера за годы или даже десятилетия до постановки диагноза, далее появляются АТ к БМК в низком титре, сохраняющиеся в течение многих лет, а затем их уровень резко повышается за несколько недель или месяцев до первых клинических проявлений заболевания. Эти данные указывают на то, что АНЦА и АГ, против которых они направлены, могут играть причинную роль в патофизиологии синдрома Гудпасчера, возможно, за счет нарушения четвертичной структуры гексамера α345NC1 базальной мембраны клубочков, провоцирующего аутоиммунный ответ. В недавнем исследовании было показано, что сыворотка более половины пациентов с АТ к базальной мембране клубочков может распознавать дегликозилированную МПО, что указывает на потенциальный общий патогенетический путь между синдромом Гудпасчера и МПО-АНЦА-васкулитом.
Данные по поводу прогностической значимости «двойной позитивности» (АТ к БМК (+)/МПО-АНЦА(+)) в плане прогноза течения заболевания и возможности восстановления функции почек крайне противоречивы.
McAdoo и коллеги сравнили клинические признаки заболевания и долгосрочный прогноз у 568 пациентов с ААВ, 41 пациента с синдромом Гудпасчера и 37 пациентов с «двойной позитивностью». У пациентов с «двойной позитивностью» были общие характеристики, типичные для ААВ, такие как пожилой возраст, дополнительные экстраренальные проявления и более длительная продолжительность симптомов до постановки диагноза, а также особенности синдрома Гудпасчера, такие как тяжелое заболевание почек и высокая частота легочных кровотечений в дебюте заболевания. У пациентов с «двойной позитивностью» был промежуточный риск прогрессии до терминальной почечной недостаточности по сравнению с пациентами с ААВ и синдромом Гудпасчера без АНЦА. Около одной трети выживших пациентов с «двойной позитивностью» и потребностью в диализе восстановили почечную функцию через три месяца, для сравнения: почечную функцию восстановили только 10% «моно-позитивных» пациентов с АТ к БМК. У АНЦА-негативных пациентов с АТ к БМК не отмечалось рецидивов заболевания. Напротив, у половины выживших пациентов с «двойной позитивностью» развился рецидив, эта частота была сопоставима с аналогичной у пациентов с ААВ. Авторы предполагают, что синдром Гудпасчера является преобладающим фенотипом у пациентов с двойной позитивностью (АТ к БМК (+)/АНЦА(+)).Однако эти пациенты лучше отвечали на иммуносупрессивную терапию и, в отличие от синдрома Гудпасчера, имели значительный риск рецидива заболевания. Последнее было связано с АНЦА, а не с АТ к БМК.
В другом недавнем исследовании процент пациентов с «двойной позитивностью» среди пациентов с АТ к БМК был меньше (33% против 47%), и ни у кого из этих пациентов не было рецидива заболевания в течении периода наблюдения, который длился 2,9 лет.
В целом, можно сказать, что АНЦА, особенно антитела к МПО могут быть обнаружены примерно у 1/3 пациентов с синдромом Гудпасчера. У пациентов с «двойной позитивностью» фенотип сходен с синдромом Гудпасчера без АНЦА (тяжелое заболевание почек, часто требующее диализа, и сопутствующее альвеолярное кровотечение, возникающее примерно у 40% пациентов). У пациентов, у которых есть и АНЦА и АТ к БМК есть сходные черты с пациентами, страдающими АНЦА-ассоциированным васкулитом (таких как пожилой возраст, наличие внепочечных проявлений, склонность к восстановлению функции почек, а также риск рецидивов, требующих тщательного длительного наблюдения).
АНЦА при интерстициальных заболеваниях легких
Идиопатические интерстициальные пневмонии (ИИП) – термин, пересекающийся по своему значению с термином «интерстициальные заболевания легких». Они классифицируются по гистопаталогическим, рентгенологическим и клиническим параметрам (Таблица 2).
Таблица 2. Классификация идиопатических интерстициальных пневмоний Американского торакального сообщества / Европейского респираторного сообщества
|
«Большие» идиопатические интерстициальные пневмонии:
Редкие идиопатические интерстициальные пневмонии:
Неклассифицируемые идиопатические интерстициальные пневмонии |
У многих пациентов с ИИП есть серологические или клинические признаки аутоиммунного заболевания, но нет полного соответствия критериям того или иного диффузного заболевания соединительной ткани. Европейское респираторное сообщество совместно с Американским торакальным сообществом недавно предложили термин «интерстициальная пневмония с аутоиммунными признаками» (ИПАП), и предложили для этого состояния классификационные критерии.
Интерстициальные болезни легких нечасто встречаются у пациентов с АНЦА-ассоциированными васкулитами. Они чаще встречаются при микроскопическом полиангиите, на фоне антител к МПО, чем при грануломатозе с полиангиитом (т.е. ПР3-АНЦА-васкулите). Развитие интерстициального заболевания легких часто предшествует клиническим признакам анти-МПО-васкулита. В недавнем исследовании было показано, что частота возникновения интерстициальной болезни легких составляет 7,2-15,9% при МПА и 0-3,0% при ГПА. В другом исследовании интерстициальная болезнь легких была обнаружена только у пациентов с МПО-АНЦА (12-21%). В большинстве случаев присутствовали рентгенологические и гистопатологические признаки обычной интерстициальной пневмонии или неспецифической интерстициальной пневмонии.
Частота встречаемости АНЦА у пациентов с ранее существовавшим интерстициальным заболеванием легких составила 4–36% для МПО-АНЦА и 2–4% для ПР3-АНЦА. В течении периода наблюдения у 5-10% АНЦА-негативных пациентов появились АТ к МПО и ПР3, в то время как у 25% пациентов с МПО-АНЦА развился микроскопический полиангиит.
Таким образом, АНЦА могут быть обнаружены у небольшого процента пациентов с интерстициальными заболеваниями легких. У четверти МПО-АНЦА-положительных пациентов с ИЗЛ в течение следующих месяцев или лет развиваются клинические проявления МПО-АНЦА-ассоциированного васкулита. Мы предлагаем тестировать всех пациентов с ИЗЛ на МПО-АНЦА и ПР3-АНЦА, эти тесты могли бы быть включены в серологические критерии «интерстициальной пневмонии с аутоиммунными признаками» (ИПАП). АНЦА-позитивность при ИЗЛ / ИИП может быть критерием для выбора терапии, в частности, для назначения иммуносупрессивных и антифибротических препаратов. Однако эти вопросы нуждаются в дальнейшем обсуждении, необходимо проведение соответствующих исследований.
АНЦА при инфекциях
Различные вирусные, бактериальные, грибковые и протозойные инфекции могут имитировать АНЦА-ассоциированный васкулит и осложнять иммуносупрессивное лечение. Напротив, инфекции могут быть триггером выработки АНЦА, также как развития и рецидивирования ААВ. АНЦА-позитивность была выявлена у пациентов с многочисленными хроническими инфекциями различной этиологии (Таблица 3). Кроме того, эксперименты на крысах показали, что иммунизация при помощи Staphylococcus aureus и Escherichia coli может вызвать развитие ААВ у некоторых животных.
Таблица 3. Инфекции, ассоцированные с АНЦА-позитивностью
|
Вирусы |
ВИЧ, вирусы гепатита В и С, парвовирус B-19, вирус Эпштейн-Барра, Арбовирус, вирус реки Росс |
|---|---|
|
Бактерии |
Streptococcus, Staphylococcus, Enterococcus, Bartonella, Gemella, Propionibacterium, Neisseria, Actinobacillus, Pseudomonas, Escherichia, Bacteroides, Campylobacter, Helicobacter, Yersinia, Salmonella, Proteus, Corynebacterium, Stenotrophomonas, Klebsiella, Mycoplasma, Chlamydia, Ricketsia, Treponema, Leptospira, Mycobacterium |
|
Грибы |
Aspergillus, Histoplasma, Sporothrix, Pneumocystis, Paracoccidioides, Saccharomyces |
|
Простейшие |
Entamoeba histolytica, Plasmodium, Leishmania |
|
Многоклеточные организмы |
Echinococcus, Strongyloides, Toxocara |
Staphylococcus aureus ассоциирован с ПР3-АНЦА-васкулитом, и существует множество доказательств того, что данный микроорганизм участвует в патогенезе данного заболевания. Носительство Staphylococcus aureus в носовой полости ассоциировано с высоким риском рецидива грануломатоза с полиангиитом, в то время как триметоприм-сульфометоксазон предотвращают рецидив.
В больших выборках пациентов было показано, что встречаемость АНЦА у пациентов с гепатитом В и С сравнительно низкая (МПО-АНЦА 2% и 7%, ПР3-АНЦА 8% и 0%). Данные по поводу пациентов с туберкулезом противоречивые (от 40% в одном исследовании до 0-1.5% в другом).
АНЦА, особенно ПР3-АНЦА могут быть обнаружены у значительной пропорции пациентов с инфекционным эндокардитом (8-33% по данным ИФА). Связь между ПР3-АНЦА и инфекцией особенно выражена при эндокардите, вызванном Bartonella. В одном из обзоров у 54 пациентов с инфекционным эндокардитом, вызванным Bartonella, ассоциированный гломерулонефрит был у 14 пациентов, 78% были АНЦА-позитивны, 67% ПР3-АНЦА-позитивны. Langlois и коллеги предположили, что АНЦА могут быть ассоциированы с подострой формой инфекционного эндокардита, поражающего несколько клапанов и частым вовлечением почек.
Важно, что инфекционный эндокардит всегда должен быть исключен у пациентов с АНЦА-ассоциированным васкулитом. В целом, АНЦА-позитивность имеет спорное значение при инфекционном эндокардите. Тестирование на АНЦА может быть полезно у пациентов с инфекционным эндокардитом, ассоциированным с почечной недостаточностью.
АНЦА также часто выявляется у ВИЧ-пациентов с симптомами и без симптомов, получающих высокоактивную антиретровирусную терапию. Однако остается непонятным, против каких антигенов в данном случае направлены АНЦА.
В отдельных случаях сообщалось о связи во времени между вакцинацией против гриппа и возникновением или рецидивом ААВ. Природа этой связи остается невыясненной. Было показано, что только те вакцины против гриппа, которые содержат вирусную РНК, являющуюся естественным лигандом для TLR7 способны стимулировать выработку ПР3-АНЦА, это была показано у больных с ААВ, развившимся после вакцинации от гриппа. Также есть предположения, что адъюванты, содержащиеся в вакцине, способны индуцировать развитие аутоиммунных синдромов.
В целом можно сделать следующий вывод: инфекции могут быть ассоциированы с АНЦА-позитивностью и могут имитировать АНЦА-ассоциированный васкулит. Инфекция может индуцировать аутоиммунный ответ с выработкой АНЦА и развитие АНЦА-ассоциированного васкулита. При подозрении на АНЦА-ассоциированный васкулит всегда нужно исключить возможную провоцирующую инфекцию, поскольку проведение иммуносупрессивной терапии может существенно ухудшить течение инфекции.
АНЦА при злокачественных новообразованиях
У пациентов с ААВ значительно выше риск злокачественных новообразований, чем в общей популяции, особенно часто встречается немеланомный рак кожи, лейкозы и рак желчного пузыря. По мере того, как для лечения ААВ все реже и реже используется циклофосфан, у данной группы пациентов, получающих иммуносупрессивную терапию, все чаще развивается немеланомный рак кожи. В других исследованиях было показано отсутствие четкой взаимосвязи между ААВ и онкопатологией.
Протеиназа 3, которая представляет основной аутоантиген ГПА, является регулятором обратной связи в миелоидной дифференцировке и может иметь значение при взаимодействии между аутоиммунным ответом и пролиферацией гемопоэтических клеток. Повышенная экспрессия PR3 была показана на клеточных линиях острого и хронического миелолейкоза.
Различные злокачественные новообразования могут быть ассоциированы с выработкой АНЦА при отсутствии данных в пользу системного васкулита. Так, в турецком исследовании АНЦА были выявлены у 13,3% с лимфомой Ходжкина и не были выявлены у пациентов с неходжкинскими лимфомами. Эта ассоциация клинически значима в контексте дифференциальной диагностики, поскольку злокачественные новообразования, особенно лимфома, с высоким уровнем АНЦА в сыворотке крови могут напоминать АНЦА-ассоциированный васкулит.
Лекарственно-индуцированный АНЦА-ассоциированный васкулит
Спровоцировать развитие ААВ могут различные препараты, в том числе антитиреоидные лекарства (профитиоурацил, метимазол), антибиотики (цефотаксим, миноциклин, рифампицин), ингибиторы фактора некроза опухоли-α (адалимумаб, этанерцепт, инфликсимаб), психоактивные вещества (клозапин, тиоридазин), гидралазин, аллопуринол, D-пеницилламин, сульфасалазин и левамизол.
Связь между терапией биопрепаратами и развитием ААВ особенно важна с учетом возрастающего применения ингибиторов ФНО.
Также было показано, что использование ингибиторов контрольных точек иммунного ответа (immune checkpoint inhibitors) для лечения некоторых видов рака тоже может приводить к развитию ААВ.
У большинства пациентов с лекарственно-индуцированным ААВ выявляются антитела к МПО, часто в комбинации с АТ к другим нейтрофильным цитоплазматическим белкам (таким как ПР3, человеческая нейтрофильная эластаза и антинуклеарные АТ). Двойная позитивность по антителам к МПО и ПР3 наводит на мысль о лекарственно-индуцированном заболевании. Скорее всего, лекарственно-индуцированный ААВ имеет более благоприятный прогноз, чем первичный.
В нескольких исследованиях было показано, что средняя распространенность АНЦА составляла 30% при приеме пропилтиоурацила и 6% при приеме производных метилмеркаптоимидазола. Молодой возраст и длительность терапии антитиреоидными препаратами явились основными факторами, способствующими появлению АНЦА. Суммарно АНЦА были обнаружены у 223 из 1056 пациентов (21%) независимо от типа назначаемого антитиреоидного препарата. Только у 33 пациентов (3% от общей популяции или 15% АНЦА-положительных случаев) были клинические проявления АНЦА-ассоциированного васкулита. Однако вопрос о том, следует ли проводить рутинный скрининг на АНЦА во время терапии антитиреоидными препаратами, остается спорным.
Вдыхание кокаина может вызвать деструктивный хронический воспалительный синдром верхних дыхательных путей, сходный с ГПА. У таких пациентов возможна выработка АНЦА, направленных к эластазе или катепсину G, но также может выявляться ПР3-АНЦА, что еще больше усложняет дифференциальную диагностику. Также есть данные о развитии системного и/или кожного васкулита с выработкой ПР3- и МПО-АНЦА, после употребления фальсифицированного левамизолом кокаина, который либо вдыхается в виде кокаинового порошка, либо курится как крэк-кокаин.
АНЦА при муковисцидозе
АНЦА, направленные против BPI (бактерицидный белок, увеличивающий проницаемость клеточной мембраны) обнаруживаются у 17.9% - 83.0% пациентов с муковисцидозом (средняя распространенность 49,5%). BPI - эндогенный белок с мощной деструктивной активностью в отношении грамотрицательных бактерий, таких как Pseudomonas aeruginosa, АНЦА вырабатываются к BPI в ответ на бактериальную инфекцию и колонизацию и могут снижать защитные реакции паренхимы легких и замедлять выведение бактерий. В нескольких исследованиях было показано, что BPI-АНЦА может быть биомаркером ухудшения функции легких и плохого прогноза у пациентов с муковисцидозом. Необходимы дальнейшие проспективные исследования.
Выводы
Определение АНЦА является строго обязательным только у пациентов с подозрением на АНЦА-ассоциированный васкулит. Кроме того, определение АНЦА рекомендовано пациентам с синдромом Гудпасчера, идиопатическими интерстициальными пневмониями и инфекционным эндокардитом, ассоциированным с нефритом. В этих случаях тестирование на АНЦА предполагает определение МПО-АНЦА и ПР3-АНЦА методом твердофазного ИФА в соответствии с рекомендациями 2017 г.
Для пациентов с другой патологией (воспалительные заболевания кишечника, аутоиммунные заболевания печени) тестирование на АНЦА целесообразно только в определенных слуачаях (см. Таблицу 1 и 4). В этих случаях тестирование рекомендовано проводить методом нРИФ, поскольку антигены-мишени недостаточно хорошо определены.
Таблица 4. Обзор заболеваний, при которых могут быть обнаружены АНЦА (помимо АНЦА-ассоциированного васкулита).
|
Заболевание |
АНЦА-позитивность (%) |
Сочетание с АНЦА-ассоциированным васкулитом (%) |
Комментарии |
|---|---|---|---|
|
Ревматоидный артрит |
пАНЦА (нРИФ): 16–50%; МПО-АНЦА (ИФА): 0–4% (до 18%) |
Очень редко |
пАНЦА могут быть обнаружены у значительной части больных с РА методом нРИФ, однако клиническая значимость этого явления неясна. Позитивность по МПО-АНЦА при использовании антиген-специфичных тестов довольно низка. Тестирование на МПО-АНЦА оправдано у пациентов с РА с «нефритическим» мочевым осадком. |
|
Системная красная волчанка |
пАНЦА (нРИФ): 14–31.4%; МПО-АНЦА (ИФА): 0–23.8%; ПР3-АНЦА (ИФА): 0–12.7% |
Очень редко |
АНЦА-позитивность может определяться у 15–20% пациентов с СКВ (особенно МПО-АНЦА). В одном из исследований было показано, что выявление АНЦА может быть связано с тяжестью волчаночного нефрита и активностью заболевания. Однако клиническое значение АНЦА-позитивности при СКВ четко не определено. |
|
Системная склеродермия |
0–9.1% |
0.2–0.4% |
МПО-АНЦА преобладали во всех исследованиях, кроме одного. В одном крупном исследовании (n = 1303) выявление АНЦА было ассоциировано с более высокой распространенностью ИЗЛ, ТЭЛА и более высокой смертностью. Быстро прогрессирующий гломерулонефрит у АНЦА(+) пациентов с ССД следует дифференцировать от склеродермического почечного криза. |
|
Первичный синдром Шегрена (болезнь Шегрена) |
пАНЦА (нРИФ): 5.4–17.0%; МПО-АНЦА (ИФА) 2.0–6.7% |
Очень редко |
Распространенность МПО-АНЦА у пациентов с болезнью Шегрена составила 3%. АНЦА-позитивность ассоциирована с более высокой распространенностью экстрагландулярных проявлений. Тестирование на АНЦА может быть оправдано при наличии заболевания почек или других признаков, указывающих на ААВ. |
|
Аутоиммунные заболевания печени |
аАНЦА (нРИФ): 65–81% при АИГ тип 1; 26–67% при ПБХ, 26–94% при ПСХ |
Очень редко |
аАНЦА (xANCA), направленные против ядерных антигенов или белков нейтрофильных гранул, часто обнаруживается у пациентов с АИГ методом нРИФ и могут помочь в диагностике АИГ 1-го типа при отсутствии типичных ауто-АТ. Однако их клиническое или прогностическое значение точно не определено. В одном исследовании ПР3-АНЦА были специфическим биомаркером ПСХ, хотя и с низкой чувствительностью. |
|
Воспалительные заболевания кишечника |
аАНЦА (нРИФ): 41–73% при ЯК и 6–38% при БК; ПР3-АНЦА (CLIA): 29.2–57.6% при ЯК и 1.9–2.7% при БК; МПО-АНЦА (CLIA): 9.1–12.8 при ЯК и 0–3.6% при БК. |
Очень редко |
аАНЦА (xANCA) и ASCA могут быть полезны в дифференциальной диагностике ЯК и БК в сложных диагностических случаях. ПР3-АНЦА могут быть чувствительным и специфичным биомаркером ЯК. |
|
Синдром Гудпасчера |
МПО-АНЦА (чаще) и ПР3-АНЦА: 13–47% |
- |
АНЦА (+) выявляется у пациентов, которые лучше реагируют на начальную иммуносупрессивную терапию и имеют большую склонность к восстановлению функции почек, но могут иметь рецидив во время наблюдения и требуют тщательного длительного наблюдения. |
|
Идиопатическая интерстициальная пневмония |
МПО-АНЦА 4–36%, ПР3-АНЦА 2–4% |
- |
Развитие ИЗЛ может предшествовать постановке диагноза ААВ, например. МПА развивается у 25% пациентов с МПО-АНЦА(+) ИИП. АНЦА(+) выявленные при помощи нРИФ не может влиять на решение о лечении |
|
Инфекции |
нРИФ: 18–24% ИФА: 8–14% (33% в одном исследовании) |
- |
При инфекционном эндокардите АНЦА-позитивность может быть ассоциирована с множественным поражением клапанов и более частым поражением почек. Однако выявление АНЦА представляется более важным в контексте дифференциальной диагностики с ААВ. |
|
Злокачественные новообразования |
- |
Очень редко |
Доказательства, указывающие на причинную связь между злокачественными новообразованиями и ААВ, неубедительны. Однако в некоторых случаях такую связь нельзя исключить. |
|
Лекарства |
- |
Редко |
|
|
Другие заболевания |
- |
- |
Антиген-специфические АНЦА были выявлены у пациентов с деструктивным заболеванием легких, вызванным ингаляцией кокаина, при холестериновой эмболии, муковисцидозе, рецидивирующим полихондрите и IgG4-ассоциированном заболеванием. У пациентов с муковисцидозом BPI-АНЦА может иметь прогностическое значение. |
Moiseev S, Cohen Tervaert JW, Arimura Y et al. 2020 international consensus on ANCA testing beyond systemic vasculitis. Autoimmun Rev. 2020 Sep;19(9):102618. doi: 10.1016/j.autrev.2020.102618
