Определение
Антинуклеарные антитела (АНА) - это семейство аутоантител, связывающихся с рибонуклеиновыми кислотами и ассоциированными с ними белками. Они встречаются более чем у 90% больных с диффузными болезнями соединительной ткани, такими как системная красная волчанка (СКВ), системная склеродермия (СС), смешанное заболевание соединительной ткани (СмЗСТ) и синдром Шегрена (СШ). Выявление АНА лежит в основе аутоиммунной лабораторной диагностики и представляет незаменимый инструмент ранней диагностики и идентификации основных системных аутоиммунных заболеваний, аутоиммунных заболеваний печени, ревматических заболеваний в педиатрии и ряде других состояний. Выявление АНА являются в большинстве случаев единственным методом объективизации клинического диагноза. Этот тест имеет большое значение в диагностике ювенильного ревматоидного артрита и аутоиммунных заболеваний печени. Кроме того, представители этого семейства аутоантител могут быть обнаружены при многих других аутоиммунных, инфекционных, воспалительных и онкологических заболеваниях. Разнообразие патологических форм, сопровождающихся появлением АНА, заставляет заподозрить единство иммунологических реакций в их патогенезе. В то же время, встречаемость АНА достигает 1-5% у клинически здоровых людей и несколько возрастает у лиц старше 65 лет.
Таблица 1. Заболевания, ассоциированные с выявлением антинуклеарных антител
| Состояние |
Частота обнаружения антител (%) |
|---|---|
| Заболевания, при которых АНФ высоко информативен для диагностики |
|
Системная склеродермия Болезнь Шегрена Полимиозит/дерматомиозит |
97% 48-96% 40-80% |
| Заболевания, при которых выявление АНФ необходимо для постановки диагноза |
|
Системная красная волчанка Лекарственная волчанка Смешанное заболевание соединительной ткани Аутоиммунный гепатит | 100% 100% 100% 100% |
| Заболевания, при которых выявление АНА используется для оценки прогноза |
|
Ювенильный идиопатический артрит Антифосфолипидный синдром Синдром Рейно | 20-50% 40-50% 20-60% |
| Заболевания, при которых АНФ имеет самостоятельное клиническое значение | |
Дискоидная волчанка Фибромиалгия Ревматоидный артрит Рассеянный склероз Идиопатическая тромбоцитопеническая пурпура Заболевания щитовидной железы Пациенты с силиконовыми имплантами груди Инфекционные заболевания Онкологические заболевания | 5-25% 15-25% 30-50% 25% 30-50 15-25 Данные варьируют (~20%) Данные варьируют Данные варьируют (~30%) |
| Выявление АНФ в различных титров у клинически здоровых людей до 60 лет | |
1:40 1:80 1:160 1:320 | 20-30% 10-12% 5% <3% |
Механизмы образования антинуклеарных антител
Несмотря на значительные успехи в изучении системной красной волчанки и родственных состояний в течение последних 5 лет, причины и механизмы формирования иммунного ответа в отношении рибопротеиновых антигенов остаются неизвестными. Системные заболевания, при которых выявляются АНА, характеризуются выраженным иммуновоспалительным компонентом, схожим с системным ответом при хронических инфекциях. Кроме того, при большинстве этих заболеваний в разной мере отмечается поражение сосудов с развитием васкулита или васкулопатии.
Основным механизмом индукции образования АНА, по всей видимости, является иммунный ответ против постклеточных структур, образующихся в результате апоптоза кератиноцитов, лимфоцитов и других клеток, который возникает при диффузных заболеваниях соединительной ткани. Так, в 1994 году было показано, что при индукции апоптоза культуры кератиноцитов основные антигены антинуклеарных антител накапливаются в составе нескольких популяций апоптотических телец на поверхности клетки. Эти апоптотитические тельца, содержащие в своем составе антигены АНА, напоминают по структуре вирусные частицы, и способны индуцировать специфические иммунные ответы. ( L. A. Casciola-Rosen et al. Autoantigens targeted in systemic lupus erythematosus are Clastered in two population of surface structures on apoptotic keratinocytes. J. Exp. Med. 1994 Apr 1; 179(4): 1317-1330)
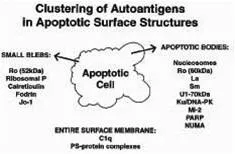

Рисунок 1. Образование основных антигенов антинуклеарных антител в ходе апоптоза эпителиальных клеток (по Casciola-Rosen et al.1994)
Значительные отложения апоптотического материала, связанного с антинуклеарными антителами, можно обнаружить при прямом иммунофлюоресцентном исследовании биопсии кожи. Этот феномен называют «волчаночная полоска». Он представляет собой крупногранулярные отложения иммуноглобулинов всех классов и факторов комплемента под базальной мембраной кожи. Выявление волчаночной полоски может использоваться в диагностике системных форм системной красной волчанки.
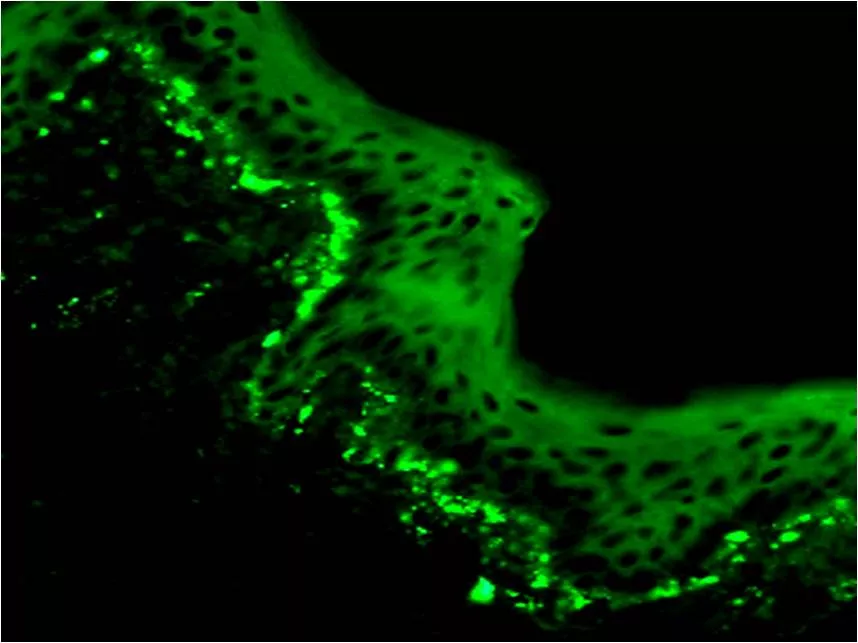

Рисунок 2. Волчаночная полоска под базальной мембраной кожи пациена с СКВ (прямая РИФ, х400)
Вопрос о патологии апоптоза при СКВ и других системных заболеваниях окончательно не решен. Исследование апоптоза кератиноцитов в эпидермисе кожи было проведено у здоровых лиц и больных СКВ по действием ультрафиолетового облучения. (E. Reefman et al.,Is disturbed clearance of apoptotic keratinocytes responsible for UVB-induced inflammatory skin lesions in systemic lupus erythematosus? ArthritisResTher. 2006; 8(6): R156.)
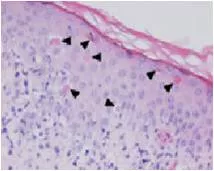
Рисунок 3. Иммунная реакция на апоптотические кератиноциты в UV-облученной коже пациента с СКВ (г/э, х1000)
При этом клиническом эксперименте было показано, что при облучении ультрафиолетом кожи больных СКВ и здоровых лиц значительное количество кератиноцитов вступает в апоптоз. Однако, в отличии от здоровой кожи, при СКВ в эпидермисе наблюдается выраженная лейкоцитарная и нейтрофильная инфильтрация, которая является причиной персистенции воспаления в коже больных системными заболеваниями. У здоровых лиц даже выраженный апоптоз клеток кожи под действием ультрафиолета не приводил к клеточной инфильтрации и ожог проходил самостоятельно.
Учитывая значительное разнообразие антинуклеарных антител, надо отметить, что большинство их разновидностей являются скорее вторичным феноменом по отношению к деструкции ткани при аутоиммунных заболеваниях. Тем не менее, ряд разновидностей антинуклеарных антител может иметь патогенетическое значение, что показано по отношению к антителам к двуспиральной ДНК при СКВ с поражением почек. Разнообразие типов АНА и уточнение клинико-лабораторных корреляций позволило использовать АНА как показатель, позволяющий клиницисту уточнить прогноз, течение и, зачастую, предупредить обострение заболевания. Антинуклеарные антитела могут обладать самостоятельной патогенностью благодаря нескольким механизмам:
- Формирование иммунного комплекса с отложением в стенке сосуда (например, сосудов почки) с развитием местного воспаления;
- Иммунные комплексы, содержащие АНА, могут захватываться Toll-likeрецепторами и обладать иммуномодулирующим действием;
- Цитотоксичность (например, при цитопении);
- Связывание антител с белками сыворотки (например, при антифосфолипидном синдроме);
- Проникновение антител в живую клетку и ядро, частое обнаружение АНА in vivo при выполнении биопсий ткани у больных СКВ.
Классификация и номенклатура антинуклеарных антител
Антинуклеарные (антиядерные или антиклеточные) антитела (АНА) представляют собой семейство аутоантител, реагирующих с нуклеиновыми кислотами и ассоциированными с ними белками. С связи с многообразием этого семейства возникает очевидная проблема с номенклатурой тестов, определяющих различные представители АНА. К настоящему времени описано более 200 клеточных мишеней АНА, направленных против нуклеиновых кислот, гистонов, белков ядерного матрикса, белков ядерной мембраны, компонентов сплайсосомы, рибонуклеоротеинов, рибосом, белков ядрышек и центромер. Многие из рибонуклеопротеиновых мишеней могут находиться как в ядре клетки так и в цитоплазме, а некоторые рибонуклеопротеины находят исключительно в цитоплазме, т.е. они являются не ядерными, а цитоплазматическими антигенами. Существует полемика, о том, можно ли называть антитела, направленные к цитоплазматическим антигенам термином "антинуклеарные антитела". В то же время, антитела к цитоплазматическим антигенам, выявляющиеся при полимиозите и дерматомиозите взрослых, также причисляются к АНА, так как они направлены против рибопротеиновых структур участвующих в синтезе белка, а в их возникновении предположительно участвуют сходные патогенетические механизмы. В то же время, определенная неопределенность присутствует, например антитела к митохондриям (АМА), которые формально не относятся к АНА, также выявляются при обнаружении антинуклеарного фактора. Понимание того, что рибонуклеопротеиновые антигены могут быть локализованы не только в ядре но и цитоплазме клетки, заставляет некоторых экспертов рекомендовать название "антиклеточные антитела", однако учитывая огромное количество литературных источников и роль традиции, термин "антинуклеарный фактор" подходит для описания результатов метода нРИФ.
Антинуклеарный фактор с определением типа свечения ядра
Основным методом обнаружения АНА является иммунофлюоресцентный тест на перевиваемых клеточных линиях человека (HEp-2) , в отечественной литературе получивший название «антинуклеарный фактор», тест 01.02.15.005. Несмотря на то, что в современной зарубежной литературе термином антинуклеарный фактор (АНФ) пользуются редко, мы считаем целесообразным сохранить данное наименование для иммунофлюоресцентных тестов, чтобы отличить их от других методов выявления АНА. АНФ определяется методом непрямой иммунофлюоресценции (НРИФ). Благодаря способности к выявлению широкого спектра аутоантител метод НРИФ с использованием перевиваемой клеточной линии Нер2 является наиболее чувствительным методом скрининга АНА.
Антинуклеарный фактор на НЕр-2 клетках является «золотым стандартом» диагностики, поскольку определяет максимальное количество и спектр антинуклеарных антител. Кроме того, антинуклеарный фактор указывает на распределение мишеней антинуклеарных антител в клетке, так называемый тип свечения ядра, и указывает на аффинность антител, что определяется титром серологческой реакции. Учитывая высокую чувствительность обнаружения АНФ, нередко проводят равенство между присутствием АНА в крови больных определенными заболеваниями и положительным результатом лабораторного обследования для обнаружения АНФ. Также немаловажным является указание субстрата выявления АНФ, например, «криосрезы почки крысы» или «клеточная линия Нер-2». Это позволяет ориентироваться в диагностическом значении результата теста, так как оно в значительной мере зависит от субстрата обнаружения АНФ и исходного титра сыворотки.
Присутствие в сыворотке крови антинуклеарного фактора обуславливает обнаружение в крови клеток красной волчанки (LE-клеток). Таким образом, LE-клетки также можно рассматривать в качестве вторичного показателя, указывающего на наличие антинуклеарных антител. Низкая чувствительность и плохая воспроизводимость тестов, используемых для обнаружения LE-клеток, не позволяет им на равных конкурировать с АНФ, и в настоящее время анализ на LE-клетки постепенно вытесняется серологическими методами обнаружения АНА.
Отдельно выделяют скриниговые тесты, основанные на смеси белков, часто именуемые скрининг антител к экстрагируемым ядерным антигенам (ENA скрин), тест 01.02.15.160. Большинство ИФА для скрининга АНА используют смеси очищенных аутоантигенов из нативных источников и/или рекомбинантных технологий. Состав этих антигенных смесей довольно разнообразен и зависит от нескольких факторов, включая доступность очищенных антигенов и техническую возможность объединения всех различных антигенов в одном анализе. Большинство доступных иммунометрических тестов содержат SS-A / Ro60, SS-B / La, Scl-70 / топоизомеразу I, CENP-B, Jo-1, U1-RNP, Sm и дсДНК. АНА-скрининг методом ИФА может содержать и другие аутоантигены, такие как PM/Scl или рибосомальный Р-протеин. реактивность к антигенам Ro52 или Ro60 (SS-A) не обнаруживается приблизительно в 20% случаев при использовании ИФА тест-систем на основе смеси очищенных антигенов.
В случае положительного результата АНФ необходимо уточнять антигенную специфичность выявленных антител. C этой целью применяются такие диагностические платформы, как ИФА, хемилюминесцентный анализ, иммуноблоттинг, проточная цитометрия с иммунореактивными микрочастицами (ПЦИМ) и другие. Они основаны на использовании очищенных и/или синтетических аутоантигенов, и их аналитические характеристики сильно отличаются от АНФ (Таблица 1). Преимуществом этих альтернативных подходов к тестированию АНА является простота эксплуатации, возможность проведения количественного анализа, объективность. Методы иммуноблота и проточной цитометрии с иммунореактивными частицами характеризуются мультиплексным подходом к детекции АНА, а именно обеспечивают одновременное обнаружение спектра аутоантител. Антитела к различным антигенам могут быть определены как качественно, так и количественно, с помощью денситометрического анализа в случае иммуноблоттинга или изменения интенсивности флюоресцентного сигнала при ПЦИМ. Основные недостатки использования альтернативных методов для обнаружения АНА связаны с ограниченным количеством выявляемых антигенов и низкой диагностической значимостью отрицательного результата.
Таблица 2. Методы выявления антинуклеарных антител
| Метод |
Лабораторное оборудование, фирмы-производители |
|---|---|
| Автоматизированный метод нРИФ на эпителиоидных клеточных линиях человека НEр-2 и Нер 2000 (нРИФ) | TITERPLANE (Euroimmun AG), AKLIDES (Medipan) |
| Иммуноферментный метод (ИФА) |
ANALYZER (Euroimmun AG), ALEGRIA (Orgentec) |
| Иммуноблот: лайнблот (LIA), вестерн-блот, дот-блот |
EUROBlotOne (Euroimmun AG), BlueDiver (D-TEK) |
| Хемилюминесценция (CLIA) | LIAISON (DiaSorin) |
Проточная цитометрия с иммунореактивными микрочастицами (ALBIA/XMAP) | BIOPLEX 2200 (BioRAD) |
| Иммуноферментный флюоресцентный метод (FEIA) |
PHADIA 250 (Thermo Scientific) |
Всеми действующими группами экспертов, в том числе группой по исследованию антинуклеарных антител Американского колледжа ревматологов (ACR ANA Task Force) и экспертами Европейской инициативы по стандартизации тестов в аутоиммунных заболеваниях - European Autoimmunity standartization Initiative (EASI), настойчиво рекомендуется использовать антинуклеарный фактор с помощью нРИФ на НЕр2 клетках (тест 01.02.15.005) в качестве основного метода скрининга антинуклеарных антител/
Рекомендации по тестированию антинуклеарных "антиклеточных" антител
Международные рекомендации по тестированию антинуклеарных антител были опубликованы в 2014 году группой экспертов из разных стран. Были сформулированы 25 рекомендаций для определения антинуклеарного фактора (АНФ) на НЕр2 клетках (1–13), антител к двухцепочечной ДНК (14–18), специфических антител (19–23) и валидации методик (24-25). В ходе разработки рекомендаций была определена роль НРИФ как эталонного метода для детекции антинуклеарного фактора, была подчеркнута важность определения как ядерного, так и цитоплазматического типов свечения, а также признана необходимость включить альтернативные автоматизированные методы в алгоритм лабораторной диагностики аутоиммунных заболеваний. Различные подходы к преодолению несходимости между методами были обсуждены. Эти рекомендации разработаны с целью стандартизации алгоритмов для тестирования и оценки АНА и ассоциированных с ними аутоантител.
Таблица 3. Международные рекомендации Agmon-Levin et al. 2014 по тестированию антинуклеарных антител (АНА)
1) Диагноз СЗСТ требует нескольких специализированых лабораторных тестов
2) Выявление АНФ, анти-дсДНК и антитела к ЭНА (специфичностей АНА) следует использовать для диагностики СЗСТ и ряда других аутоиммунных заболеваний
3) Выявление АНФ является первым лабораторным тестом в диагностике СЗСТ
4) Выявление АНФ следует использовать для диагностики, а не мониторинга СЗСТ
5) Непрямая иммунофлюоресценция (АНФ) является референтным методом скринигового выявления АНА. Другие методы выявления АНА могут отличаться по уровню ложных результатов. Если существует клиническое подозрение при отрицательном результате другого метода выявления АНА, следует провести выявление АНФ
6) Диагностические лаборатории должны указывать метод выявления АНА
7) Тесты, основанные на смеси нескольких конкретных ядерных антигенов не должны называться АНА- тестом или АНА –скринингом
8) Лаборатории, которые используют внутрилабораторные методы для выявления АНФ, равно как и антитела к дс ДНК и специфическим ЭНА должны стандартизовать эти методы с помощью международных стандартов (ВОЗ или CDC/IUIS)
9) Для выявления АНФ следует использовать меченную флюорохромом античеловеческую антисыворотку против IgG
10) Титр АНФ зависит от реактивов, оборудования и других факторов, поэтому разведение для скрининга сыворотки следует определять в лаборатории. Повышенный АНФ следует считать титр выше 95го перцентиля контролей из здоровой популяции. В большинстве случаев разведение сыворотки 1:160 достаточно для выявления АНФ во взрослой популяции
11) В случае положительного результата выявления АНФ в результате лабораторного теста должен быть указан тип свечения клетки и наивысший титр разведения сыворотки
12) Тип АНФ следует указывать в соответствии со стандартной терминологией
13) Кроме типов свечения ядра АНФ должны указываться свечения цитоплазмы и делящихся клеток
14) При обнаружении АНФ и клиническом подозрении на СКВ следует рекомендовать выявление антител к дсДНК
15) При выявлении антител к дсДНК наилучшую специфичность имеют радиоиммунный тест (тест Фарр/Farr) и непрямая иммунофлюоресценция на Crithidia luciliae (CLIFT). Положительные результаты других тестов следует подтверждать этими методами.
16) Метод, используемый для выявления антител к дсДНК, следует указывать в форме результата лабораторного теста
17) Результат выявления антител к дсДНК должен предоставляться в количественном виде
18) При мониторинге СКВ с помощью количественного измерения антител к дсДНК должен использоваться один и тот-же лабораторный метод
19) В случае положительного результата АНФ следует использовать лабораторные тесты для определения специфичности АНА
20) Для выявления антител к ЭНА следует указывать метод выявления. В случае расхождения с результатами АНФ или клинической картиной рекомендуется использование альтернативного метода выявления антител
21) Результаты определения специфичности антител к ЭНА следует указывать отдельно (включая отрицательный результат выявления антител). При интерпретации результатов скрининговых тестов выявления антител достаточно указать какие разновидности ЭНА присутствуют в составе тест-системы.
22) При подозрении на смешанное заболевание соединительной ткани рекомендуется количественное определение антител к RNP
23) В случае подозрения на конкретное СЗСТ следует проводить углубленное исследование конкретной специфичности АНА. Например, антител к Jo-1 при воспалительных миопатиях, антител к рибосомам и SSA антигену при различных формах волчанки и синдроме Шегрена
24) Каждая лаборатория должна верифицировать референтные пределы скрининговых методов выявления АНА с помощью сывороток здоровых лиц известного пола и возраста. Референтные пределы должны быть сопоставлены с 95 перцентилем результатов измерений в сыворотках здоровых лиц.
25) Каждая лаборатория должна верифицировать референтные значения методов выявления антител к дсДНК и антител к ЭНА. Следует использовать достаточное количество образцов больных с разными аутоиммунными заболеваниями, от заболевших и здоровых доноров. Референтные значения должны устанавливаться с помощью ROC-анализа
Примечание: АНА –антинуклеарные антитела; АНФ — антинуклеарный фактор; дсДНК — двуспиральная ДНК; СЗСТ — системные заболевания соединительной ткани; ЭНА- экстрагируемые нуклеарные антигены; CLIFT — Crithidia luciliae immunofluorescence test
Антиядерные (антинуклеарные) антитела и антитела к экстрагируемому ядерному антигену
Эта группа тестов представляет собой антитела к водорастворимым компонентам ядра клетки. Под названием extractible nuclear antigen (ENA) – "экстрагируемый нуклеарный (ядерный) антиген» (ЭНА/ENA) понимают фракцию растворимых ядерных белков, которые могут быть получены из ядра клетки. В ее состав входит 6 основных рибонуклеопротеиновых антигенов АНА, таких как SSA, SSB, Sm, U1-RNP, Scl-70 и Jo-1, а также ряд других минорных антигенов. Первоначально для этого теста использовался ацетонный экстракт тканей лабораторных животных, например, тимуса кролика, который содержал максимальное количество нуклеиновых и рибонуклеиновых антигенов. В настоящее время при выявлении антиядерных антител обычно используется смесь антигенов, некоторые из них синтезируют с помощью рекомбинантной технологии, некоторые выделяют из ткани.
Выявлением антител к ЭНА/ENA называют определение специфичностей антинуклеарных антител (см. ниже), направленных на конкретные антигены. В данном случае, спектр антигенов ENA пространственно разделен, и тестирование происходит с конкретными антигенами. Такое разделение достигается при нанесении очищенных антигенов в разные лунки иммуноферментного планшета (ИФА) или нанесение на разные части нитроцеллюлозной мембраны (иммуноблот).
При использовании в лабораторных тестах смеси антигенов, эти методы обычно называют ЭНА-скрин (ENA-screen) или АНА-скрин (ANA-screen) при выявлении антител к экстрагируемым ядерным антигенам или антинуклеарных антител, соответственно.
Существует две основные разновидности ИФА для скринингового обнаружения антител к ЭНА. В одном случае в лунку наносится тотальный ядерный экстракт, а в другом - смесь рекомбинантных очищенных белков, представляющих основные разновидности рибонуклеопротеиновых антигенов. Использование смеси рекомбинантных белков делает обследование более специфичным и улучшает стандартизацию выявления аутоантител. В то же время, далеко не все антигены АНА могут быть нанесены на ИФА планшет, в результате чего комбинированные тесты пропускают до 40-60% антинуклеарных антител, выявляемых с помощью антинуклеарного фактора.
В скрининговых методах смесь антигенов вносится в лунку планшета для иммуноферментного анализа (ИФА) или используется в автоматизированных тестах для обнаружения антинуклеарных (антиядерных) антител. Несмотря на сравнительную быстроту и удобство, эти методы значительно уступают антинуклеарному фактору, так как упускают до 20% положительных результатов, кроме того, возрастает частота ложноположительных реакций. Это происходит в силу ряда причин:
- Спектр исследуемых антигенов не превышает 6-10;
- Отсутствуют конформационные и лабильные антигены;
- В смеси антигенов образуется множество неоэпитопов;
- Одни антигены блокируют другие антигены;
- Сорбция антигенов на подложку неравномерна, заряженные антигены сорбируются;
- При рекомбинантном синтезе и очистке меняется структура большинства антигенов;
- Возможны реакции с блокирующим веществом.
В то же время, потребность в большей автоматизации лабораторного процесса привела к тому, что появляется все больше новых методов для выявления антинуклеарных антител, альтернативных процессу выявления антинуклеарного фактора. Более 10 лет назад появились первые наборы для определения АНА с помощью ручного метода ИФА, основанные на смеси очищенных и рекомбинантных антигенов ЭНА. В настоящее время ведущими мировыми производителями лабораторного оборудования создаются автоматизированные полузакрытые и закрытые системы, принцип работы которых основывается на различных методах: методе твердофазного иммуноферментного анализа (ИФА), хемилюминесцентного метода, технологии мультиплексного анализа.
Внедрение представленных современных автоматизированных систем ставит вопрос о целесообразности сохранения АНФ в качестве основного метода диагностики АНА. Для выработки рекомендаций по этой проблеме действует несколько европейских и американских групп экспертов, таких, как ANA Task Forcе Американского колледжа ревматологов и European Autoimmunity Standartization Initiative (EASI). Большинство экспертов сходятся во мнении, что определение антинуклеарных антител методом АНФ на клетках Нер-2 с помощью непрямой иммунофлюоресценции является первостепенным в диагностике системной аутоиммунной патологии. Если же для диагностики АНА используется другой лабораторный метод, то диагностические лаборатории должны указывать, каким методом исследуются антинуклеарные антитела. Кроме того, диагностические лаборатории должны указывать специфичность и чувствительность используемого метода выявления антинуклеарных/антиядерных/анти-ЭНА антител по сравнению с АНФ.
Со своей стороны, рекомендуем использовать обнаружение антител к ЭНА-скрин (АНА-скрин) в качестве дополнительного метода при выявлении антинуклеарного фактора. Скрининг болезней соединительной ткани (тест 01.02.15.245) позволяет не пропустить редкие случаи «АНФ-негативной СКВ» и другие заболевания, сопровождающиеся формированием высокорастворимых антигенов, таких как SSA-антиген. Отрицательный результат такого теста позволяет исключить диагноз системного ревматического заболевания с вероятностью 95-98%, что позволяет широко использовать его в целях скрининга и дифференциальной диагностики.
Таким образом, иммунохимические тесты по выявлению антиядерных (антинуклеарных) антител должны использоваться только совместно с антинуклеарным фактором. При использовании иммунохимических методов в качестве единственного метода выявления АНА наблюдается высокая частота ложноотрицательных результатов обследования (Bossuyt et al. Ann Rheum Dis 2008) и ошибочное исключение диагноза аутоиммунного заболевания. В частности, методы скринингового определения антинуклеарных антител оказываются бессильны при аутоиммунных заболеваниях печени, ювенильном ревматоидном артрите и ряде других аутоиммунных заболеваний, поскольку не содержат соответствующих антигенов антинуклеарных антител.
Нуклеиновые кислоты (ДНК, РНК) водонерастворимы и отрицательно заряжены, поэтому в состав экстрагируемых ядерных антител не входят. Для их выявления необходимо использовать антинуклеарный фактор и другие подтверждающие тесты (антитела к дсДНК методом ИФА, тест 01.02.15.125).
В то же время, выявление антител к экстрагируемому ядерному антигену (тест 01.02.15.160) представляет собой отдельный показатель , обычно определяемый с помощью метода ИФА. Его использование наряду с определение АНФ позволяет уточнить присутствие в исследуемой сыворотке антител к хорошо растворимым конформационным антигенам, прежде всего SS-A, которые могут утрачиваться в ходе фиксации клеток перевиваемых клеточных линий.
Определение специфичности антинуклеарных антител
Под определением «специфичность антинуклеарных антител» понимают выявление конкретного антигена, к которому направлены АНА. Номенклатура конкретных разновидностей АНА зависит как от ядерных мишеней аутоантител, так и от методов, с помощью которых они обнаруживаются. Отдельно выделяют: АНА, реагирующие с нуклеиновыми кислотами, прежде всего ДНК; антитела к водорастворимым антигенам, которые могут быть экстрагированы водно-солевыми растворами; антитела к экстрагируемому ядерному антигену (ЭНА); антитела к нерастворимым в воде антигенам; а также к конформационным антигенам, которые разрушаются при препаративном выделении из ядра клетки. Два последних вида аутоантигенов не могут быть получены в очищенном виде, поэтому единственным объективным методом их обнаружения является АНФ с описанием типа свечения ядра клетки. Хотя большинство белков, которые используются в коммерческих наборах для выявления АНА, являются рекомбинантными и уже не экстрагируются из ядер клеток, конкретные разновидности белковых антигенов АНА продолжают называть общим термином «экстрагируемый нуклеарный антиген» (ЭНА) - extractible nuclear antigen (ENA). Иногда исследование специфичностей антинуклеарных антител называют «определение антител к ЭНА». Для определения специфичностей антинуклеарных антител в нашей лаборатории используется иммуноблот антинуклеарных антител (тест 01.02.15.165)
Уточнение антигенных мишеней АНА зависит от антигенного субстрата, который применяется в иммунологических тестах. Антиген-содержащий субстрат может быть нативным, то есть полученным при минимальной очистке, либо высокоочищенным из ткани с помощью биохимических методов. Кроме того, белки-антигены могут быть получены методами генной инженерии или синтезированы химически методами пептидного синтеза. Использование того или другого метода очистки и синтеза аутоантигена зависит, прежде всего, от его биохимической природы и особенностей связывания с ним аутоантител. Рекомбинантные белки и синтетические пептиды более удобны в работе, так как методы их получения легко стандартизируются. Однако, чем менее очищен антиген, тем более он сохраняет свою третичную структуру, таким образом взаимодействие с аутоантителом более приближено к условиям взаимодействия in vivo.
Аутоантитела против внутриклеточных антигенов, открытые на стыке клинической иммунологии и молекулярной биологии, способствовали процессу постижения функционирования клеточных структур. Описание антинуклеарных антител активно продолжается в настоящее время одновременно с совершенствованием лабораторных техник и углублением фундаментальных познаний о строении клетки. Большинство видов АНА направлены к сложным комплексам рибонуклеиновых кислот и белков. Изучение антинуклеарных антител зачастую опережало открытие функциональных белков и рибопротеиновых комплексов, что привело к возникновению двойной номенклатуры при описании некоторых видов АНА, включающей как общепринятое название аутоантитела, так и указание конкретного ядерного белка. Обычно тип антинуклеарных антител получал название, в основе которого лежит имя пациента, у которого эта разновидность АНА была впервые обнаружена. В основе более современной номенклатуры лежат клеточные мишени аутоантител, с которыми они взаимодействуют.
Таким образом, номенклатура аутоантигенов может строиться на основе следующей информации:
- Структура молекулы (двуспиральная ДНК);
- Название антигена или молекулярная масса (snRNP70);
- Фамилия больного, у которого антитела были обнаружены впервые (например, Sm - Smith);
- Сокращение антигена/заболевания (PM-Scl – полимиозит-склеродермия).
Например, антитела к антигену Ro/SS-A (Ro по фамилии больного Robair /SS-A - Sjogren’s syndrome A antigen), направлены против белков массой 52 кДа и 60 кДа, связанных с Y1-Y5 РНК в составе сплайсосомы, а антитела к антигену La/SS-B (по больному Lapiere/Sjogren’s syndrome B antigen) направлены против белка, связанного с РНК полимеразой 3. Номенклатура аутоантител, основанная на фамилиях пациентов, постепенно уходит в прошлое, а в современной литературе превалирует название антигенов с указанием молекулярной массы, например, SS-A антиген молекулярной массой 52 и 60 кДа.
Возможна ситуация, при которой указывается конкретная клеточная мишень аутоантител. Так, антитела, направленные против ядерного антигена пролиферирующих клеток, получили название по имени белка, с которым они реагируют, - PCNA 1 (proliferating cell nuclear antigen 1). Разновидность АНА может получить название в соответствии с молекулярной массой белка, с которым оно взаимодействует, например, аутоантитела анти-р80 направлены к белку массой 80 кДа. Последующие исследования установили точную клеточную мишень, как, например, для анти-р80 антител это белок койлин. У больных со склеродермией были обнаружены антитела, направленные на антиген массой 70 кДа и получившие название Scl-70. Позднее было установлено, что мишенью Scl-70 - антител является топоизомераза 1, точнее, ее иммунодоминантный эпитоп, получивший название TOPO-1.
Может сложиться ситуация, когда в одной сыворотке могут быть одновременно обнаружены антитела разных специфичностей, направленные к нескольким антинуклеарным антигенам. Некоторые антитела часто отмечаются совместно – например, антитела к SS-Aи SS-B, либо U1-RNP и Sm антигенам. Эти ассоциации обусловлены тем, что антигены входят в состав одного белкового комплекса, с которым реагируют аутоантитела. Некоторые разновидности АНА могут часто отмечаться совместно за счет того, что они встречаются при одном заболевании или при перекрестных синдромах. Клиническое значение определения специфичности основных разновидностей антинуклеарных антител приведено в описании соответствующих тестов.
Антитела к двуспиральной (нативной) ДНК
Антитела к двуспиральной ДНК (дсДНК) (тест 01.02.15.124) играют большую роль в диагностике и мониторинге больных с системной красной волчанкой, однако их выявление имеет ряд особенностей. Для детекции антител к дсДНК методом иммуноферментного анализа сложно сохранить нативную структуру молекулы. Так, молекула дсДНК несет значительный отрицательный заряд и не может быть непосредственно нанесена на отрицательно заряженный пластик иммуноферментного планшета. Для того, чтобы сорбировать дсДНК на дне лунок планшета, необходимо использовать положительно заряженные вещества-линкеры. Часто использование УФ-облучения планшетов или использование чужеродных белков (например, протамина) приводит к деспирализации дсДНК с образованием значительного числа односпиральных молекул и снижению специфичности обследования. В результате, большинство твердофазных иммуноферментных систем первого поколения для обнаружения антител к дсДНК оказываются относительно неспецифичными. Практическим ревматологам необходимо знать об этой особенности выявления антител к дсДНК и с осторожностью интерпретировать низкие титры этого показателя. Для выявления антител к дсДНК рекомендуется использовать тест-системы второго поколения, обладающие улучшенными клинико-лабораторными параметрами. Используемая в нашей лаборатории тест система для выявления антител к дсДНК ассоциированной с нуклеосомами (anti-dsDNA-NcX) исключает неспецифическое связывание антител к односпиральной ДНК и имеет низкую частоту ложно-положительных результатов обследования пациентов с аутоиммунной патологией.
Лабораторные алгоритмы диагностики СмЗСТ
Учитывая разнообразие методов выявление АНА, одновременное назначение всех скрининговых и подтверждающих методов является трудоемким, дорогостоящим и часто неоправданным. Очевидно, что возникает необходимость последовательного тестирования данных АНА, основанном на определенном диагностическом алгоритме (Рисунок 1). Так как общепринятого алгоритма серологической диагностики АНА у лиц с подозрением на СмЗСТ не существует, ряд авторов рекомендуют использовать внутренние алгоритмы, оптимизирующие выявление АНА в рутинной работе.
В большинстве клинических лабораторий АНФ является скрининговым тестом. Положительный результат АНФ является показанием к подтверждающим исследованиям, а именно проведения ИФА или тестирования методом иммуноблота с целью установить специфичность выявленных аутоантител, таких как анти-дсДНК, анти-Ro / SS-A, анти-La / SS-B, анти-RNP и анти-Sm и т.д. Отрицательны или низкие титры АНФ при низкой вероятности наличия ревматическое заболевания обычно указывает на отсутствие аутоиммунных заболеваний. Однако, в отношении некоторых клинически значимых антител АНФ характеризуется низкой чувствительностью, как при Ro52, Jo-1. Для снижения вероятность ложноотрицательного результата на скрининговом этапе рекомендуется выполнять АНФ в комплексе с исследованием на антитела к экстрагируемому нуклеарному фактору, который обладает более высокой чувствительностью к данным антигенам.
Так как некоторые конкретные АНА обладают высокой диагностической значимостью, положительные результаты АНФ обычно требуют последующего дообследования с помощью подтверждающих специализированных тестов при наличии высокого клинического подозрения на наличие системного аутоиммунного заболевания, так как прогностическая ценность АНФ в отсутствие клинических проявлений ДБСТ являются низкой, так как АНА могут выявляться задолго до появления первых симптомов, и вследствие относительно высокой частоты АНА у здоровых людей. Таким образом, если присутствуют клинические проявления, характерные для СКВ, дальнейшее лабораторное исследование должно включать анти-дсДНК, анти-Sm, анти-U1 snRNP и анти-Ro антитела. Точно так же, если есть подозрение на смешанное заболевание соединительной ткани (СЗСТ), синдром Шегрена, системную склеродермию (ССД) или полимиозит, сыворотка может быть исследована на анти-U1 snRNP, анти-Ro52, анти-SSA, SSB, анти-топоизомераза I антитела, антицентромерные или антинуклеолярные антитела. Если эти тесты являются отрицательными в условиях высокого клинического подозрения, повторное тестирование на более позднем этапе может быть оправдано, поскольку титры таких аутоантител могут изменяться со временем, независимо от течения заболевания.
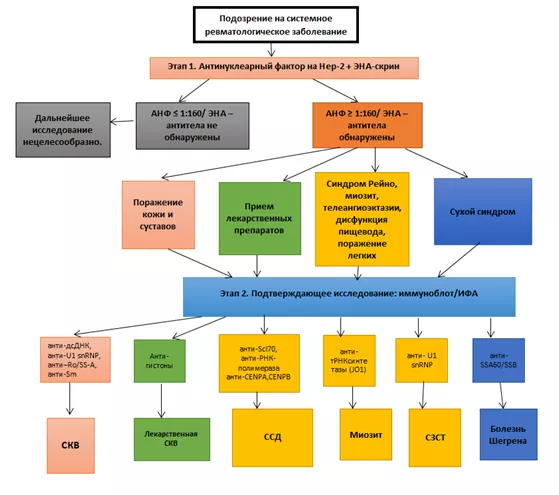
Рисунок 5. Алгоритм диагностики СЗСТ
В нашей лаборатории в 2011 году было проведено исследование по разработке и практической оценке алгоритма для диагностики СЗСТ, основанного на результатах обследования 981 пациентов (Лазарева Н.М., Лапин С.В. и др. КлинЛабДиаг, 2011). Для выявления АНФ с определением типа свечения (тест 01.02.15.005) нами был использован метод непрямой иммунофлюоресценции на клеточной линии НЕр-2 и Нер2000 (Euroimmun AG, Германия). Клеточная линия Нер-2000 обладает повышенной частотой клеточных делений, и клетки делятся в 4–10 раз чаще по сравнению с классической линией Нер-2. Среди исследованных 981 образцов с подозрением на СЗСТ в 474 образце были выявлены АНФ. В данных образцах анализировались результаты выявления АНФ и антител к экстрагируемым ядерным антигенам методом ИФА (тест 01.02.15.160). Хотя оба метода обладают высокой сходимостью, чувствительность определения антител к экстрагируемому ядерному антигену (ИФА ЭНА/АНА-скрин) значительно уступает АНФ (20% против 48%). При этом изолированно антитела к ЭНА с помощью иммуноферментного теста были обнаружены только у 5,5 % (28/507) пациентов, что указывает на роль тестов для их выявления в определении тех разновидностей АНА, которые утрачиваются из ядра клетки в ходе фиксации, либо плохо распознаются при микроскопии. Эта находка подчеркивает необходимость использования АНФ для ранней диагностики СЗСТ.
Для выявления спектра антинуклеарных антител использовался метод лайн-блот (иммуноблот АНА), в котором применялись следующие рекомбинантные антигены: Sm, RNP/Sm, SS-A, SS-B, Scl-70, CENP-B, PCNA, дсДНК, нуклеосомы, гистоны, Jo-1, АМА-М2 (тест 01.02.15.165). В образцах, положительных по антителам к ЭНА, но отрицательных по АНФ антитела к растворимым SS-A/SS-B антигенам отмечались в 64% (18/28) случаев, в образцах положительных по АНФ и анти-ЭНА — в 46 % (136/298) случаев. Кроме того, в двух образцах, изолированно положительных по антителам к ЭНА были обнаружены антитела к Jo-1 антигену, который располагается в цитоплазме клеток и может быть неразличим при микроскопии. Полученные результаты сопоставимы с данными литературы.
Специфичность АНА с помощью метода иммуноблота была установлена в 63 % образцов, положительных по АНФ и в 97 % образцов, положительных по антителам к ЭНА. Таким образом, специфичность АНА с помощью используемых методов не может быть установлена в 37 % АНФ-положительных образцов, что не исключает диагностической ценности выявления АНФ. Иммуноблот оказывается отрицательным у большинства пациентов с низкими титрами АНФ. Таким образом, выполнение иммуноблота антинуклеарных антител у пациентов с отрицательным или низким результатом АНФ и отсутствием антител к ЭНА нецелесообразно. Выявление антител к дсДНК обладает высокой сходимостью с результатами определения АНФ и антител к ЭНА. При выявлении АНФ и/или антител к ЭНА вероятность обнаружения антител к дсДНК составляет около 30%, что позволяет рекомендовать антитела к ДНК в качестве теста «второй линии» при обследовании пациентов с системными заболеваниями, после обнаружения АНФ или антител к ЭНА. Чувствительность ИФА тест-систем по определению антител к дсДНК у различных производителей значительно варьирует, несмотря на то, что для стандартизации данных тестов используется референтная сыворотка Всемирной Организации Здравоохранения (ВОЗ) Wo80. По нашим данным, разница в чувствительности тестов составила 56 % и 38 % в зависимости от производителя.
Наряду с методом ИФА в диагностике антител к дсДНК используется метод нРИФ с использованием клеток Crithidia lucilliae (тест 01.02.15.905). Несмотря на сравнительно низкую чувствительность данного метода, этот тест по-прежнему рекомендуется в качестве подтверждающего теста, позволяющего объективизировать выявление антител к дсДНК. Полученные нами данные позволяют рекомендовать сочетанное выявление АНФ методом нРИФ и теста для определения антител к смеси ЭНА в качестве серологического лабораторного скрининга системных заболеваний соединительной ткани. Отрицательный результат обоих методов указывает на отсутствие АНА и делает диагноз СЗСТ маловероятным и не требует дальнейшего применения тестов второй линии, к которым может относиться определение АНА методом иммуноблота, метод твердофазного ИФА с раздельными антигенами или методами мультиплексного анализа. При выявлении АНФ или антител к ЭНА рекомендуется использование методов определения специфичности АНА, к которым относится метод иммуноблота и определение антител к дсДНК. Проведенный нами финансовый анализ эффективности такого подхода показывает, что использование данного алгоритма сокращает затраты на обследование одного пациента с подозрением на СЗСТ на 33,5 %.
Кроме того, последовательное назначение тестов повышает диагностическую эффективность, поскольку снижает число ложноположительных результатов обследования. Среди СЗСТ по встречаемости антинуклеарных антител системная склеродермия (ССД) даже опережает СКВ, поскольку АНФ отмечается практичеки у всех пациентов с этим заболеванием в очень высоких титрах. К настоящему времени, при ССД описано около 30 антигенных мишеней АНА, причем выявление ряда специфичностей АНА может определять как особенности поражения внутренних органов, так и прогноз заболевания. В большинстве методов ИФА и иммуноблота обычно присутствует ограниченный спектр антигенов, представленный Scl-70 и CENT-B антигенами, определяющий предрасположенность к диффузной и лимитированой форме заболевания. Иммуноблот для выявления антинуклеарных антител при склеродермии (тест 01.02.15.535) кроме антигенов Scl-70 и CENT-А и B, выявляет антитела к РНК-полимеразам (RP11 и RP155) которые отмечаются при тяжелом течении ССД, а также антитела к Th/To, встречающимися при мягкой клинической форме ССД. Также в иммуноблоте представлены антигены, характеризующие перекрестные синдромы, в частности Ku, антитела против которого отмечаются при СКВ с симптоматикой ССД и антигены PM-Scl 75кДа и 100 кДа, являющиеся маркером сочетания ССД и полимиозита. В состав данного блота входят ряд антигенов ядрышка (фибрилларин и NOR90), а также антигены PDGFR и Ro-52. Для выявления АНА нами были обследованы 67 больных ССД проходивших стационарное лечение в условиях специализированного ревматологического отделения. В исследованной группе антинуклеарный фактор (АНФ) был выявлен у 100 % (67/67) пациентов, причем преобладали центромерный и ядрышковый типы свечения ядра. Антитела против Scl-70 и/или анти-CENP-В отмечались в 28 % (19/67) и 34 % (23/67) соответственно, а хотя бы одно из этих антител было обнаружено в 61 % случаев. Использование расширенного иммуноблота, содержащего 12 аутоантигенов, позволило увеличить чувствительность определения АНА в образцах до 94 % (63/67), т. е. позволяет увеличить число положительных серологических находок более чем на треть.
Таким образом, несмотря на тенденции к автоматизации и попыткам упрощения тестов для серологической диагностики СЗСТ на сегодняшний день наилучшей комбинацией лабораторного тестирования для определения АНА является сочетание выявления АНФ на НЕр2 клетках (тест 01.02.15.005) и выявления специфичностей АНА с помощью метода иммуноблота с максимально широким спектром аутоантигенов, к которым относятся иммуноблот АНА (тест 01.02.15.165), иммуноблот АНА при склеродермии (тест 01.02.15.535), иммуноблот при воспалительных миопатиях (тест 01.02.15.320).