- Оценка состояния эпителиального барьера кишечника;
- Прогнозирование течения воспалительных заболеваний кишечника, целиакии.
Зонулин представляет собой гликопротеин массой 48 кДа, который синтезируется во многих тканях, включая тонкий кишечник. Его местный синтез приводит к раскрытию межклеточных контактов тонкого кишенчника, что приводит к парацеллюлярному (межклеточному) пассивному переносу множества веществ из просвета тонкого кишечника, включая токсины бактерий, жиры и жирные кислоты, пищевые аллергены, мелкие молекулы, такие как скатол, бутират и индол. Основным индуктором синтеза зонулина в стенке кишечника являются фрагменты глютена злаковых, а также ряд специфических бактерий. Дефект синтеза зонулина отмечается при ряде обменных и аутоиммунных заболеваний, кроме того повышенный синтез зонулина в стенке кишечника отмечается у 10-15% людей и является причиной повышения проницаемости тонкого кишечника или синдрома «протекающего» или «дырявого» кишечника, обусловленного нецелиакийной непереносимостью глютена.
Зонулин – эндогенный человеческий аналог бактериального токсина холерного вибриона (Zonula occludens toxin), который синтезируется в гепатоцитах и эпителиальных клетках кишечника и оказывает влияние на выработку клаудина и окклюдина, составляющих основу плотных контактов (tight joints, TJ) между энтероцитами. За счет сходства с предшественником гаптоглобина-2, зонулин получил альтернативное название прегаптоглобин-2.Зонулин участвует в повышении проницаемости эпителиального слоя тонкого кишечника за счет обратимой модуляции TJ, правильное функционирование которых регулирует межклеточный транспорт и предотвращает диффузию мембранных белков в кишечнике. Индуктором синтеза зонулина в кишечнике являются пептиды глиадина и бактерии. Было показано, что кроме энтеротоксинов, комменсальная и вирулентная Escherichia coli, Salmonella typhi вызывают высвобождение зонулина из стенки кишечника. Зонулин трансактивирует эпидермальный фактор роста (EGFR) через рецептор, активируемый протеазой-2 (PAR2), что приводит к разобщению TJи росту проницаемости кишечника. Cпецифические неперевариваемые глиадиновые пептиды, независимо от генетической предрасположенности к развитию аутоиммунных реакций, способны связывать хемокиновый рецептор CXCR3 на апикальной поверхности энтероцитов с последующим MyD88-зависимым высвобождением зонулина и провоспалительных цитокинов из макрофагов (рис. 1). В этой ситуации может возникнуть манифестация целиакии или постинфекционного синдрома раздраженного кишечника.Кроме того, рецептор CXCR3 также сверхэкспрессируется на апикальной поверхности пациентов энтероцитов у пациентов с болезнью Крона.
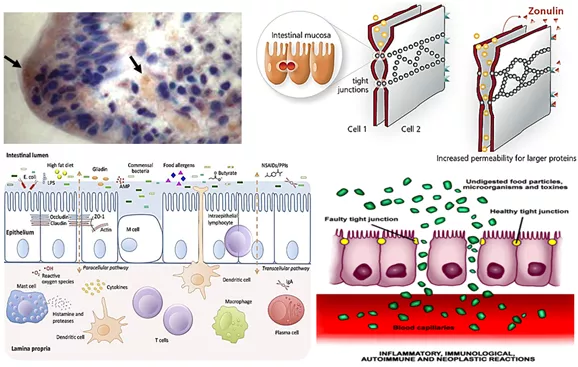
Чрезмерная активация продукции зонулина как по длительности, так и по выраженности может вызывать избыточное и нерегулируемое повышение проницаемости эпителиального пласта, что приводит к прохождению антигенов и макромолекул через стенку кишечника (синдром «протекающего кишечника», “leaky gut”) и инициирует локальное и/или системное воспаление.
Повышение проницаемости кишечника, в свою очередь, может способствовать развитию аутоиммунных, воспалительных, метаболических, нейродегенеративных и опухолевых заболеваний. Чрезмерное потребление в пищу продуктов, с большим содержанием FODMAP (олиго-, ди-, моносахаридов и полиолов) простых углеводов, эмульгаторов, микробной трансглютаминазы (пищевая добавка) и наночастиц также могут быть причиной повышенного высвобождения зонулина.
При проведении дифференциальной диагностики и уточнения причин повышенной проницаемости кишечника может быть рекомендовано определение маркеров кишечного воспаления – фекального кальпротектина (тест 01.02.15.550), гемоглобина и гемоглобин-гаптоглобинового комплекса (тест 01.02.15.720), инфекционного поражения – антигена G. lamblia (тест 01.02.15.1070), токсинов А и В Cl. difficile (тест 01.02.15.685) в кале, аллергического процесса – эозинофильного нейротоксина в кале (тест 01.02.15.1050), нарушений всасывания в кишечнике – остаточной осмолярности стула (тест 01.02.15.489), рН и углеводов в кале (тест 01.02.15.1045), экссудативной энтеропатии –α1-антитрипсина в стуле (тест 01.02.15.502), жировой диареи – стеатокрита (тест 01.02.15.1075), панкреатической эластазы-1 (тест 01.02.15.1060), активности химотрипсина (тест 01.02.15.1055) в стуле, холагенной диареи – желчных кислот (тест 01.02.15.1265), а также специфических сывороточных маркеров заболеваний кишечника, включая комбинированное обследование при воспалительных заболеваниях кишечника – АНЦА (IgG, IgA), ASCA (IgG, IgA), антитела к бокаловидным клеткам кишечника, экзокринной части поджелудочной железы, антигену GP2 (тест 01.02.15.260), целиакии – антитела к тканевой трансглутаминазе (IgG, IgA), дезаминированным пептидам глиадина (IgG, IgA), эндомизию (IgA) (тест 01.02.15.221) и генотипирование HLA DQ2/DQ8 (тест 01.02.15.431) и аутоиммунной энтеропатии – антитела к энтероцитам (тест 01.02.15.1040).
Референсные значения:
- < 86 нг/мл - нормальная концентрация
-
86-110 нг/мл - повышенная концентрация
-
> 110 нг/мл - высокая концентрация
Интерпретация:
Повышенные значения зонулина в кале, свидетельствующие о повреждении слизистой оболочки кишечника, расширении межклеточных контактов энтероцитов с развитием синдрома «протекающего кишечника» отмечаются при:
- заболеваниях кишечника (нецелиакийная непереносимость глютена, эозинофильный энтероколит, синдром раздраженного кишечника, некротизирующий энтероколит, бактериальный зарост кишки);
- аутоиммунных заболеваниях (целиакия, болезнь Крона, язвенный колит, аутоиммунная энтеропатия, сахарный диабет 1 типа, ревматоидный артрит, системная красная волчанка, системный склероз);
- метаболических расстройствах (ожирение, инсулинорезистентность, сахарный диабет 2 типа, синдром поликистозных яичников);
- поражениях легких (синдром острого повреждения легких, бронхиальная астма),
- инфекционных заболеваниях (сепсис, ВИЧ);
- чрезмерном и/или регулярном употребление алкоголя, кукурузного сиропа с высоким содержанием фруктозы и FODMAP;
- курении;
- контакте с токсичными веществами (полихлорбифенилами, гликозилированными белками или жирами, индуцированными современным способом обработки пищи, ртутью, алюминием, пластиком);
- приеме лекарственных препаратов (ингибиторы протонового насоса, нестероидные противовоспалительные препараты, ингибиторы циклооксигеназы 2, антибиотики);
- остром/хроническом психоэмоциональном стрессе.
