Определение
Семейная гиперхолестеринемия (СГХС) является самым распространённым генетическим метаболическим заболеванием и характеризуется аномальным повышенным уровнем холестерина липопротеинов низкой плотности (ХС-ЛПНП) в сыворотке крови с рождения, что со временем может привести к раннему развитию атеросклероза и сердечно-сосудистых осложнений (ССО), высокому риску преждевременной смерти. СГХС - преимущественно моногенное заболевание с преобладающим аутосомно-доминантным типом наследования. Различают гетерозиготную и гомозиготную СГХС.
Лабораторно СГХС характеризуется повышением общего холестерина и ХС-ЛПНП:
-
ОХС > 7.5 ммоль/л или ХС-ЛПНП > 4.9 ммоль/л у взрослых
-
ОХС > 6.7 ммоль/л или ХС-ЛПНП > 4.0 ммоль/л у детей
Чаще всего заболевание длительные годы протекает бессимптомно и зачастую манифестирует в виде ишемической болезни сердца (ИБС), в частности инфаркта миокарда, или внезапной смерти. Однако есть несколько внешних признаков, характерных для СГХС, таких как ксантомы, ксантелазмы и липидная дуга роговицы (см. ниже).
Эпидемиология
Частота гетерозиготной СГХС (геСГХС) составляет 1:250-350 и даже может быть выше (вплоть до 1:76-90 в популяциях с высокой распространенностью близкородственных браков). Частота гомозиготной СГХС (гоСГХС) составляет в среднем 1:300,000 (варьирует от 1:160,000 до 1:1,000,000).
Согласно экспертным данным, до 90% СГХС являются не выявленными и не диагностированными. По всей вероятности, в мире имеется более 15 млн человек с СГХС, но выявлено только 10 % из них и адекватное лечение проводится только у 5 %
Согласно рекомендациям Европейского общества атеросклероза, скрининг на содержание холестерина должен быть проведен всем лицам в популяции до достижения ими возраста 20 лет. В случае семейного анамнеза СГХС или раннего развития ИБС, определение уровня общего холестерина сыворотки проводится, начиная с возраста 2 лет.
Этиология и патогенез
Развитие СГХС обусловлено мутациями генов, участвующих в метаболизме липопротеинов, что приводит к недостаточному захвату ХС-ЛПНП из кровотока, либо повышению деградации ЛПНП-рецептора.
В настоящее время известен ряд генов, являющихся причиной аутосомных форм СГХС, и до 50 локусов с полиморфизмами, способствующими полигенной предрасположенности к повышению уровня ХС-ЛПНП .
Самая частая генетическая причина СГХС – мутация в гене ЛПНП-рецептора (LDLR), который расположен главным образом на поверхности гепатоцитов и играет ключевую роль в связывании и выведении из кровотока циркулирующих ЛПНП-частиц. На сегодняшний день известно более 2000 мутаций LDLR, способных нарушить функцию рецептора и вызывать развитие СГХС. Мутации в гене LDLR обуславливают от 85 до 90% случаев СГХС.
Вторая по частоте причина – мутация в гене аполипопротеина В (APOB), кодирующего аполипопротеин В100, входящий в состав ЛПНП-частиц и ответственный за связывание ЛПНП с LDLR. В результате изменений в гене половина ЛПНП-частиц не способна связаться с LDLR. Мутации гена APOB обуславливают от 5 до 10% случаев СГХС. Показано, что носители мутаций гена LDLR имеют более высокий уровень ОХС и ХС-ЛПНП и более выраженные проявления атеросклероза артерий, чем носители мутаций гена APOB.
Третий ген, мутации в котором способны приводить к развитию СГХС, – это ген PCSK9, кодирующий пропротеин конвертазу субтилизин/кексин тип 9, участвующую в разрушении LDLR. Мутации, приводящие к усилению функциональной активности PCSK9, вызывают ускоренную деградацию LDLR, в результате чего уменьшается количество рецепторов на поверхности клетки и нарушается захват ЛПНП. Мутации гена PCSK9 встречаются менее чем в 5% случаев СГХС.
Мутации в генах LDLRAP1, ABCG5, ABCG8, CYP7A1 имеют рецессивный тип наследования и клинически проявляются только как гомозиготная форма СГХС. Редкие варианты СГХС могут быть вызваны мутациями в генах STAP1, LIPA и PNPLA5.
Таблица 1. Гены, ассоциированные с семейной гиперхолестеринемией
|
ген |
белок |
хромосомная локализация |
MIM |
количество мутаций |
комментарии |
|---|---|---|---|---|---|
|
аутосомно ко-доминантый тип наследования* |
|||||
|
LDLR |
рецептор к ЛНП |
19p13.2 (18) |
143890, 606945 |
>2,000 |
наиболее частая причина СГХС |
|
APOB |
аполипопротеин B100 |
2p24.1 (29) |
144010, 107730 |
32 |
обычно ассоциированы с менее тяжелым фенотипом, чем мутации LDLR |
|
PCSK9 |
пробелок конвертаза субтилизин/ кексин типа 9 |
1p32.3 (13) |
603776, 607786 |
23 |
мутации с приобретением функции вызывают СГХС, тогда как мутации с потерей функции вызывают снижение уровня холестерина ЛНП. |
|
аутосомно-доминантый тип наследования |
|||||
|
APOB |
аполипопротеин B100 |
19q13.32 (6) |
107741 |
1 |
внутрирамочная делеция Leu167 была обнаружена у лиц с фенотипом СГХС |
|
STAP1 |
сигнал-передающий адапторный белок 1 |
4q13.2 (10) |
604298 |
4 |
мутации чрезвычайно редки |
|
аутосомно-рецессивный тип наследования |
|||||
|
LDLRAP1 |
адапторный белок 1 для LDLR |
1p36.11 (15) |
603813, 605747 |
17 |
У лиц с двумя мутациями наблюдается аутосомно-рецессивная ГХС и часто более мягкий фенотип, чем у лиц с двумя мутациями LDLR; гетерозиготы часто ни имеют липидных нарушений |
|
ABCG5 |
стеролин 1 |
2p21 (15) |
210250, 605459 |
2 |
Мутации вызывают ситостеролемию; сложная гетерозиготная мутация была обнаружена у ребёнка с ГХС |
|
ABCG8 |
стеролин 2 |
2p21 (14) |
|
|
|
|
LIPA |
лизосомальная кислая липаза |
10q23.31 (10) |
278000, 613497 |
1 |
Мутации вызывают болезнь накопления эфиров холестерина (болезнь Вольмана); гомозиготные мутации в месте сплайсинга могут вызывать фенотип, похожий на СГХС. |
Семейная гиперхолестеринемия, вызванная мутацией в одном гене, называется моногенной (описана выше). Причинная мутация в генах-кандидатах может быть обнаружена у 60–80% пациентов с клинически доказанной гиперхолестеринемией. У 20-40% пациентов с гиперлипидемией не выявляются моногенные мутации, характерные для СГХС. У значительной части пациентов, у которых на основании лабораторных и клинических данных подозревается семейная гиперхолестеринемия, но не выявлены мутации, вызывающие заболевание, вероятно, имеет место полигенная гиперхолестеринемия. Такие пациенты являются носителями полиморфизмов, затрагивающих несколько локусов, связанных с повышенным уровнем холестерина ЛПНП.
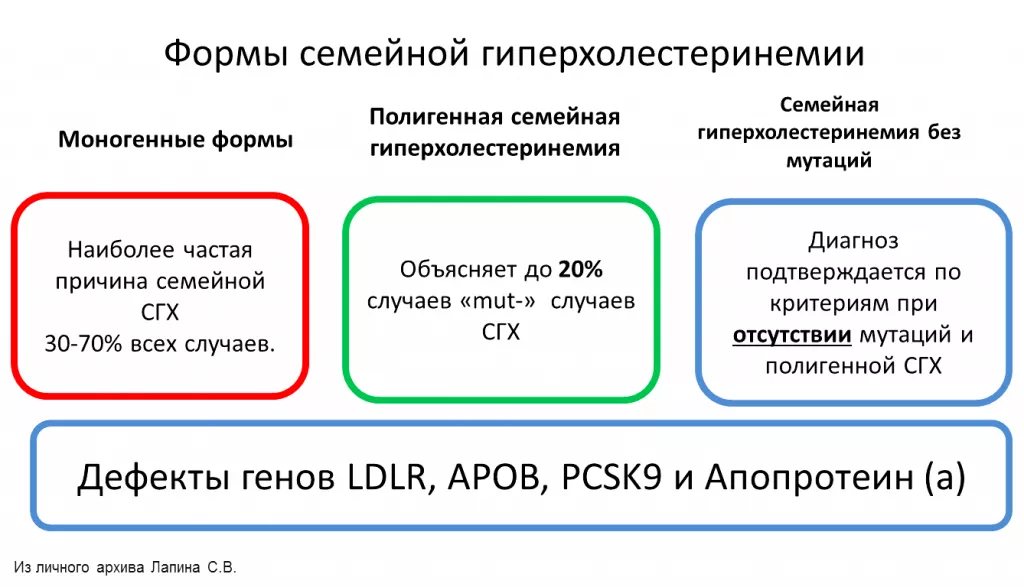
Другие редкие генотипы, которые могут встречаться, - это сложная гетерозиготность (разные мутации в каждом аллеле) или двойная гетерозиготность (мутации в двух аллелях двух разных генов). Эти редкие генотипы обычно приводят к гораздо более тяжелому фенотипу.
Уровень общего холестерина (ОХС) у пациентов с гетерозиготной СГХС обычно составляет 7,5-14 ммоль/л. Развитие ССО происходит преждевременно (<55 лет у мужчин, <60 лет у женщин).
При гомозиготной СГХС, при которой генетический дефект, унаследован от обоих родителей, уровень ОХС - 14-26 ммоль/л. В этом случае тяжелая гиперхолестеринемия приводит к развитию ССО уже в детстве и юности.
Согласно современной концепции развития атеросклероза (липидно-инфильтрационная теория), формирование атеросклеротической бляшки обусловлено поступлением в субэндотелиальное пространство как нативных, так и окисленных (модифицированных) ЛПНП. Чем выше уровень последних в плазме крови, тем интенсивнее протекает этот процесс. Более того, при длительном нахождении ЛПНП в крови вероятность окисления частиц возрастает. Больные СГХС характеризуются длительной экспозицией высокого уровня ЛПНП в кровотоке, что и обусловливает раннее и прогрессирующее развитие атеросклероза.
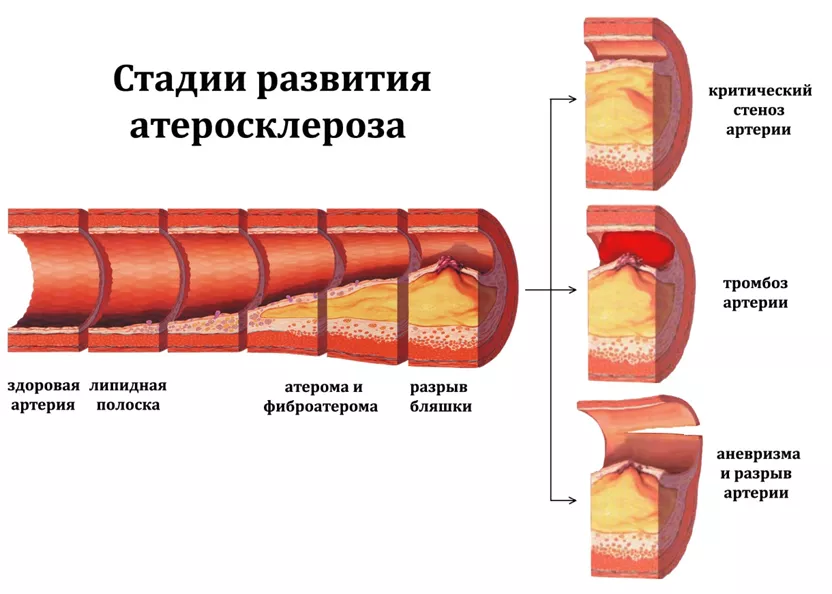
На развитие атеросклероза, в частности ИБС, у больных СГХС оказывают те же факторы риска, что и у лиц без СГХС: модифицируемые (артериальная гипертензия, сахарный диабет, курение, низкая физическая активность, ожирение) и немодифицируемые факторы (мужской пол, возраст, отягощенность семейного анамнеза по сердечно-сосудистым заболеваниям). Дополнительные факторы риска атеросклероза, помимо гиперхолестеринемии, увеличивают смертность при СГХС.
Клиническая картина
Поскольку СГХС является результатом генетического нарушения, ГХС развивается уже в раннем возрасте и приводит к преждевременному развитии ИБС и других ССО. В связи с тем, что ГХС сама по себе не вызывает никаких жалоб, заболевание длительные годы протекает бессимптомно и зачастую манифестирует в виде инфаркта миокарда или внезапной смерти.
Средний возраст клинических проявлений ИБС у пациентов с геСГХС – до 45 лет у мужчин и до 55 лет у женщин. Примерно у 2% пациентов, перенесших инфаркт миокарда в возрасте до 50 лет, была выявлена СГХС.
Если уровень холестерина ЛНП >10 ммоль/л, то ССО возникают уже во второй декаде жизни и включают не только поражение коронарных артерий, но и поражение каротидных, периферических артерий, аортального клапана и супроаортальной надклапанной области.
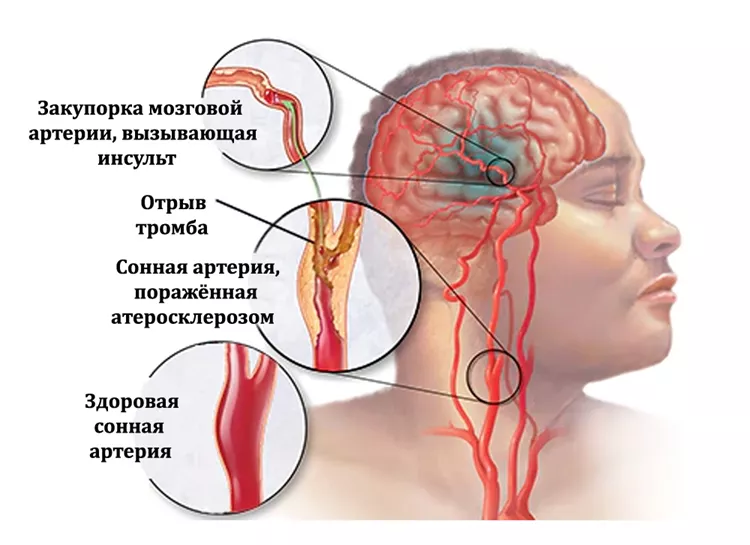
гоСГХС манифестирует в значительно более раннем возрасте, чем геСГХС
Пациенты с СГХС, даже при отсутствии ССЗ атеросклеротического генеза относятся к группе высокого риска, а при их наличии – к группе очень высокого риска развития сердечно-сосудистых осложнений.
У 30-55% больных СГХС выявляются сухожильные ксантомы (рис 1), которые можно обнаружить в любом возрасте. Ксантомы сухожилий могут появляться на тыльной стороне кистей, локтях и коленях, а также на ахилловых сухожилиях. Тем не менее, эти признаки обычно упускают из виду или обнаруживают ретроспективно, после того как документируется повышенный уровень ХС-ЛПНП. Для больных с гоСГХС характерны также кожные ксантомы (рис 2).
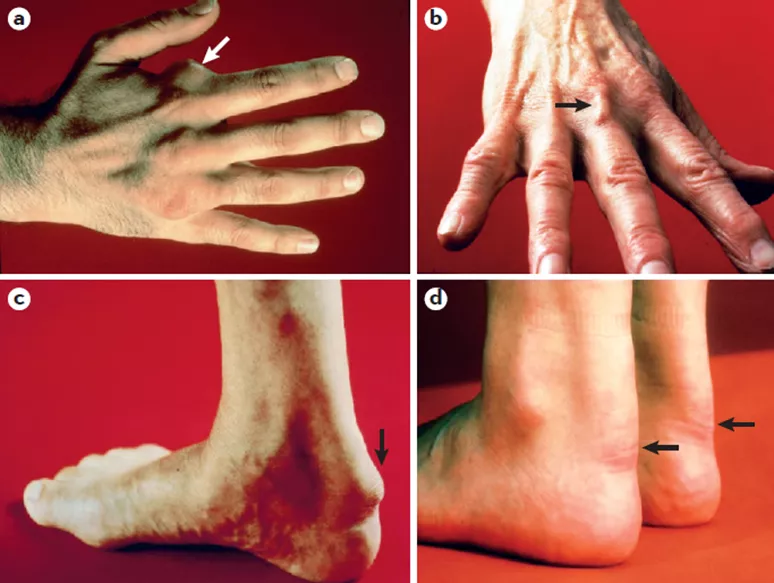
Рис 1. Сухожильные ксантомы кистей (a,b) и ахилловых сухожилий (c,d) у пациентов с гетерозиготной СГХС [2].
![Кожные ксантомы у пациентов с гомозиготной СГХС [4]. Кожные ксантомы у пациентов с гомозиготной СГХС [4].](/upload/dev2fun.imagecompress/webp/medialibrary/492/image-3.webp)
Рис 2. Кожные ксантомы у пациентов с гомозиготной СГХС [4].
Патогномоничным признаком для СГХС являются липоидная дуга роговицы и ксантелазмы (липидные отложения в области век) (рис 3), выявляемая в возрасте до 45 лет.
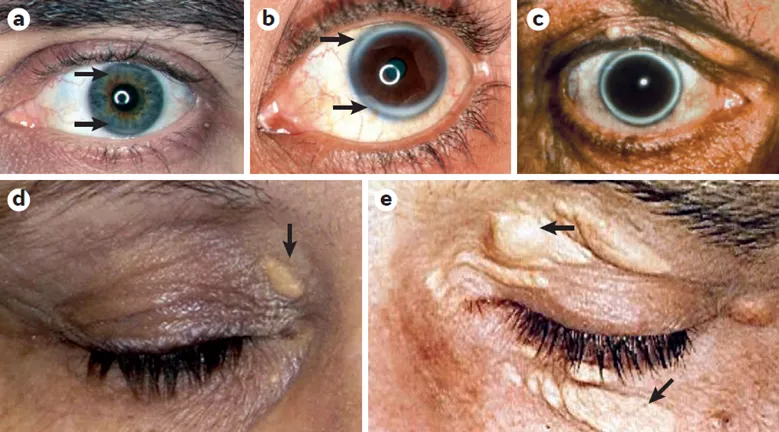
Рис 3. Липоидная дуга роговицы (a,b,c) и ксантелазмы (липидные отложения в области век) (d,e) у пациентов с гетерозиготной СГХС [2].
Диагностические критерии семейной гипрхолестеринемии
Существует несколько вариантов критериев для постановки диагноза СГХС: критерии Саймона Брума [6], критерии Голландской сети липидных клиник (DLCN)[7], критерии ICD-10 [2,4], критерии Канадского сообщества сердечно-сосудистых заболеваний (CCS) [8] и другие. Сравнительный анализ критериев можно найти в статье Berberich AJ, Hegele RA [5].
В качестве основных критериев диагностики геСГХС у взрослых рекомендуется использовать критерии DLCN [1].
Для постановки диагноза геСГХС у детей и подростков в возрасте до 16 лет рекомендуется использовать критерии Саймона Брума и/или модифицированные критерии экспертов Европейского общества по атеросклерозу (EAS, 2015), которые могут быть использованы у детей и подростков до 19 лет [1].
Для диагностики гоСГХС у взрослых и детей рекомендуется использовать критерии, предложенные экспертами Европейского общества по атеросклерозу (EAS, 2014) [1].
Также рекомендуется проведение обследования, направленного на исключение причин вторичных гиперлипидемий, у всех лиц с подозрением на СГХС.
Ниже размещены ссылки на все вышеупомянутые критерии:
- Критерии DLCN (Dutch Lipid Clinic Network) для диагностики семейной гиперхолестеринемии
- Критерии Саймона Брума для диагностики семейной гиперхолестеринемии
- Критерии диагностики гетерозиготной СГСХ у детей и подростков
- Критерии диагностики гомозиготной СГСХ
- Критерии ICD-10 для диагностики семейной гиперхолестеринеми
Вторичные причины повышения ЛПНП
Основные заболевания/состояния, а также лекарственные препараты, которые могу обуславливать вторичное повышение ЛПНП:
|
Нарушение диеты |
|
|---|---|
|
Лекарственные препараты |
|
|
Заболевания |
|
|
Нарушения метаболизма |
|
|
Физиологические состояния |
|
Лабораторная диагностика
Диагностика нарушений липидного обмена начинается с определения уровня общего холестерина. Если он повышен, необходимо выполнение липидограммы (электрофореза липидных фракций) - тест 01.02.15.1165. Комплексная оценка содержания холестерина и триглицеридов в липидных фракциях методом электрофореза (холестерин и триглицериды по фракциям ЛПВП, ЛОНП, ЛПНП, Lp(a), хиломикроны). Только этот тест позволяет провести классификацию дислипидемий в соответствии с МКБ.
Семейная гиперхолестеринемия может быть заподозрена когда уровень ХС-ЛПНП > 4,9 ммоль/ л (190 мг/дл) у взрослых или 4,1 ммоль/л (160 мг/дл) у детей (включая подростков до 18 лет [1]. Важна оценка сопутствующей сердечно-сосудистой патологии и семейного анамнеза.
При подозрении на СГХС необходимо выполнение генетического обследования (выявление мутаций, вставок, делеций в генах LDLR, APOB, PCSK9):
Тест 01.02.05.260. Комплексная диагностика наследственной гиперхолестеринемии (гены LDLR, APOB, PCSK9)
Тест 01.02.15.1235. Диагностика семейной гиперхолестеринемии (ген LDLR)
Тест 01.02.15.865. Исследование 26-го экзона гена APOB100
Тест 01.02.05.285. Исследование 6 экзонов гена PCSK9
Наиболее точным методом генетической диагностики является тест 01.02.05.710. Полногенный NGS анализ при семейной гиперхолестеринемии (гены LDLR, APOB, PSCK9, LDLRAP1)
Причинная мутация в генах-кандидатах может быть обнаружена у 60–80% пациентов с клинически доказанной гиперхолестеринемией. У 20-40% пациентов с гиперлипидемией не выявляются моногенные мутации, характерные для СГХС. У значительной части пациентов, у которых на основании лабораторных и клинических данных диагностирована семейная гиперхолестеринемия, но не выявлены мутации, вызывающих заболевание, вероятно, имеет место полигенная гиперхолестеринемия. Такие пациенты являются носителями полиморфизмов, затрагивающих несколько локусов, связанных с повышенным уровнем холестерина ЛПНП. В этом случае рекомендовано выполнение теста 01.02.05.1740. Полигенный индекс семейной гиперхолестеринемии
Перед назначением статинов для минимизации риска побочных эффектов, связанных с назначением данной группы препаратов, рекомендуется выполнение теста 01.02.05.700 Исследование фармакогенетики статинов c развернутым заключением (гены SLCO1B1, ABCG2, CYP2C9)
Скрининг
Рекомендуется проводить целевой скрининг на СГХС среди следующих лиц [1]:
-
лица с индивидуальным и/или семейным анамнезом ГХС (ОХС > 7,5 ммоль/л или ХС-ЛПНП > 4,9 ммоль/л у взрослых или ОХС > 6,7 ммоль/л или ХС-ЛПНП > 3,5 ммоль/л у детей);
-
лица с индивидуальным анамнезом раннего (у мужчин < 55 лет; у женщин < 60 лет) развития ССЗ атеросклеротического генеза;
-
лица с кожными/сухожильными ксантомами или периорбитальными ксантелазмами
1) Ежов М.В., Бажан С.С., Ершова А.И. и соавт. Клинические рекомендации по семейной гиперхолестеринемии. Атеросклероз. 2019;15(1):58-98
2) Defesche JC, Gidding SS, Harada-Shiba M et al. Familial hypercholesterolaemia. Nat Rev Dis Primers. 2017 Dec 7;3:17093. doi: 10.1038/nrdp.2017.93
3) Al-Rasadi K, Al-Waili K, Al-Sabti HA et al. Criteria for Diagnosis of Familial Hypercholesterolemia: A Comprehensive Analysis of the Different Guidelines, Appraising their Suitability in the Omani Arab Population. Oman Med J. 2014 Mar;29(2):85-91. doi: 10.5001/omj.2014.22
4) Gidding SS, Champagne MA, de Ferranti SD, et al. The Agenda for Familial Hypercholesterolemia: A Scientific Statement From the American Heart Association. Circulation. 2015 Dec 1;132(22):2167-92. doi: 10.1161/CIR.0000000000000297
5) Berberich AJ, Hegele RA. The complex molecular genetics of familial hypercholesterolaemia. Nat Rev Cardiol. 2019 Jan;16(1):9-20. doi: 10.1038/s41569-018-0052-6
6) Risk of fatal coronary heart disease in familial hypercholesterolaemia. Scientific Steering Committee on behalf of the Simon Broome Register Group. BMJ. 1991 Oct 12;303(6807):893-6. doi: 10.1136/bmj.303.6807.893
7) Austin MA, Hutter CM, Zimmern RL, Humphries SE. Genetic causes of monogenic heterozygous familial hypercholesterolemia: a HuGE prevalence review. Am J Epidemiol. 2004 Sep 1;160(5):407-20. doi: 10.1093/aje/kwh236
8) Primary Panel:; Genest J, Hegele RA, Bergeron J et al. Canadian Cardiovascular Society position statement on familial hypercholesterolemia. Can J Cardiol. 2014 Dec;30(12):1471-81. doi: 10.1016/j.cjca.2014.09.028
9) Watts GF, Gidding S, Wierzbicki AS et al. Integrated guidance on the care of familial hypercholesterolaemia from the International FH Foundation. Int J Cardiol. 2014 Feb 15;171(3):309-25. doi: 10.1016/j.ijcard.2013.11.025